将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
| A.两烧杯中铜片表面均无气泡产生 | B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均增大 | D.产生气泡的速度甲比乙慢 |
若以稀硫酸作电解质溶液,则关于铜锌原电池的叙述,正确的是
| A.铜是正极,铜片上有气泡产生 | B.氢离子在锌片表面被还原 |
| C.电流从锌片经导线流向铜片 | D.铜片质量逐渐减少 |
若以稀硫酸作电解质溶液,则关于铜锌原电池的叙述,正确的是
| A.铜是正极,铜片上有气泡产生 | B.氢离子在锌片表面被还原 |
| C.电流从锌片经导线流向铜片 | D.铜片质量逐渐减少 |
利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示。下列说法不正确的是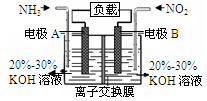
| A.电流从右侧电极经过负载后流向左侧电极 |
| B.为使电池持续放电,离子交换膜需选用阴离子交换膜 |
| C.电极A极反应式为2NH3-6e-=N2+6H+ |
| D.当有4.48LNO2(标准状况) 被处理时,转移电子为0.8mol |
下列叙述中正确的是

| A.图①中正极附近溶液pH降低 |
| B.图①中电子由Zn流向Cu,盐桥中的Cl—移向CuSO4溶液 |
C.图②正极反应是O2+2H2O+4e¯ 4OH¯ 4OH¯ |
| D.图②中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀生成 |
热激活电池可用作火箭、导弹的工作电。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池的总反应方程式为:PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。下列有关说法正确的是

|
A. 正极反应式:Ca +2Cl--2e-=CaCl2
B. 放电过程中,Li+向负极移动下列叙述正确的是
| A.铜锌稀硫酸形成的原电池放电时,溶液中阳离子向铜电极移动 |
| B.燃料电池在使用时发生了燃料的燃烧 |
| C.增大反应物的用量,反应速率一定加快 |
| D.可逆反应达到一定限度后,因各物质的浓度不变,说明反应已经停止 |
某同学根据原电池的构成及其原理,设计了以下几个装置,以证明铁、铜金属性强弱顺序。你认为下列现象符合客观事实的是
| A.装置①中:铁上有气泡 |
| B.装置②中:铜上有气泡 |
| C.装置③中:铁片上析出红色的铜 |
| D.装置④中:AB为导体,反应一段时间后,铁球向下倾斜 |
100mL 4mol/L 稀硫酸与2g锌粒反应,在一定温度下为了减缓反应的速率,但又不影响生成氢气的总量,可向反应物中加入
| A.硫酸钠固体 | B.硫酸铜固体 | C.硝酸钾溶液 | D.氯化钠溶液 |
下列关于原电池的叙述正确的是
| A.构成原电池的正极和负极必须是两种不同的金属 |
| B.原电池是将化学能转变为电能的装置 |
| C.在原电池中,电子流出的一极是负极,该电极被还原 |
| D.原电池放电时,电流的方向是从负极到正极 |
关于下图所示装置的说法中,不正确的是
| A.铜片上发生氧化反应 |
| B.电子由锌片通过导线流向铜片 |
| C.该装置能将化学能转化为电能 |
| D.锌片是该装置的负极,该电极反应为Zn—2e-==Zn2+ |
利用化学反应:Fe +CuSO4 = FeSO4 + Cu,可以设计出一种原电池。该原电池工作时:
| A.Fe 为正极 | B.Cu 为负极 |
| C.负极上发生氧化反应 | D.正极上发生氧化反应 |
试题篮
()