写出下列有机反应的化学方程式:
(1)由1—丙醇制取乙酸丙酯: 。
(2)溴乙烷和KOH的乙醇溶液共热: 。
(3)由CH2Br-CHBr-CH2Br为主要原料制取甘油: 。
写出下列反应的化学方程式
(1)工业上制备氯乙烯_____________。
(2)2-氯丙烷与KOH的乙醇溶液供热_____________。
(3)实验室制乙烯_____________。
(4)甲苯在铁粉催化下与溴单质反应_____________。
某同学设计了由乙醇合成乙二醇的路线如下。
(1)X是 (填名称)。
(2)X→Y的反应类型是 。
(3)写出Y→乙二醇的化学方程式 。
(4)等物质的量的乙醇、乙二醇完全燃烧,消耗氧气的物质的量之比是 。
(9分)有机物A的结构简式为 ,它可通过不同化学反应分别制得B、C和D三种物质.
,它可通过不同化学反应分别制得B、C和D三种物质.
(1)B中含氧官能团的名称是________.
(2)A→C的反应类型是________;A~D中互为同分异构体的是________.
(3)由A生成B的化学方程式是______________________________________.
已知有如下转化关系:①C2H5OH CH3CHO、②C2H4
CH3CHO、②C2H4 C2H5Br、
C2H5Br、
③C2H5OH C2H4则反应①、②、③的反应类型分别为 ① 、② 、③ 。
C2H4则反应①、②、③的反应类型分别为 ① 、② 、③ 。
化学方程式默写
(1)单质钾与水反应
(2)乙醇与金属钠反应
(3)乙醇在铜或银做催化剂下氧化
(4)苯和液溴反应
写出下列反应的化学方程式
(1)乙烯和溴的四氯化碳溶液的反应_______________ ___________ 。
(2)乙醇与红热的铜丝反应得到乙醛 。
(3)乙酸乙酯与氢氧化钠反应_________________________________________ 。
按要求完成下列问题:
(1) 系统命名为 ;
系统命名为 ;
(2)4―甲基―1―戊烯的键线式为 。
(3)写出乙醛与新制氢氧化铜反应化学方程式 ;
(4)丙三醇与硝酸反应能生成三硝酸甘油酯,写出三硝酸甘油酯的结构简式
(5)下列有关实验的说法不正确的是_____________。
| A.制乙烯时,温度计应插入反应混合液中 |
| B.实验室用溴和苯在铁粉存在下反应,得到的溴苯显褐色,原因是溴苯在空气中被氧化 |
| C.检验C2H5Cl中氯元素时,将C2H5Cl和NaOH水溶液混合加热,然后用稀硫酸酸化,再加入AgNO3溶液 |
| D.做过银镜反应的试管用氨水洗涤,做过苯酚的试管用酒精洗涤 |
E.将一定量CuSO4和NaOH溶液混合后加入甲醛溶液,加热未产生砖红色沉淀,原因可能是NaOH量太少
如图是A分子的球棍模型和B分子的比例模型,回答下列问题: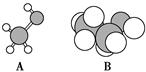
(1)A和B的关系是_____。
(2)写出A分子在催化剂存在条件下加热和氧气反应的化学方程式___________。
(3)写出B分子和金属钠反应的化学方程式_____________________。
(4)B在加热条件下能够和HBr发生反应生成溴乙烷,该反应类型是____________。
(本题共8分)酒后驾车已成为一个社会问题。检测驾驶人员呼气中酒精浓度(BrAC)的方法有多种。
1.早期是利用检测试剂颜色变化定性判断BrAC,曾用如下反应检测BrAC:
3CH3CH2OH+2KMnO4→3CH3CHO+2MnO2+2KOH+2H2O 。
上述反应中发生还原反应的过程是__________ →___________。
2.已知KMnO4在酸性条件下氧化性增强,能得到更多的电子,若在稀硫酸中反应的氧化产物为乙酸,则还原产物为___________;若反应产生了12.0 mg乙酸,则转移的电子数目是________。
3.受上述方法启发,后来用五氧化二碘的淀粉溶液检测BrAC,乙醇被氧化为乙醛,该反应的化学方程式为__________________________________________________。
4.1994年美国首次批准使用唾液酒精含量检测方法,成为血液、呼气之后的第三种检测手段。其原理是在乙醇氧化酶作用下,乙醇与氧气反应生成乙醛和过氧化氢,判断该条件下乙醇、氧气、乙醛和过氧化氢四种物质中氧化性最强的物质是________(填写化学式)。
(1)乙醇俗称__________, 其分子中的官能团是____________ (填序号) 。
①羧基(–COOH) ②醛基(–CHO) ③羟基(–OH)
(2)发酵法制乙醇的过程可简略表示如下:
(C6H10O5)n+nH2O  n C6H12O6
n C6H12O6  ;
;
上述反应中C6H12O6的名称是 ,实验室中常用 或氢氧化铜悬浊液来检验。
已知丙二酸二乙酯能发生以下反应:
有机物A在一定条件下可以发生如下图所示的转化(其他产物和水已省略)。其中相关物质的结构和性质为:A不含甲基,能与金属钠反应生成氢气;B所含碳原子数与A相同,且只含有一种官能团;C能发生银镜反应;1molD与足量碳酸氢钠溶液反应可产生二氧化碳2mol。
请结合图中其它信息回答下列问题:
(1)写出下列物质所具有的官能团的名称:C___________,D___________
(2)①~⑤反应中,属于取代反应的是________________(填序号)。
(3)写出A、G的结构简式:A__________ _, G_______ __________
(4)写出②、④反应的化学方程式:
②________________________________________________________________。
④_________________________________________________________________。
甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景。
⑴工业生产甲醇的常用方法是:CO(g)+2H2(g) CH3OH(g) △H=-90.8 kJ/mol。
CH3OH(g) △H=-90.8 kJ/mol。
已知:2H2(g)+ O2(g)= 2H2O (l) △H=-571.6 kJ/mol
H2(g) +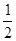 O2(g) = H2O(g) △H=-241.8 kJ/mol
O2(g) = H2O(g) △H=-241.8 kJ/mol
①H2的燃烧热为 ▲ kJ/mol。
②CH3OH(g)+O2(g) CO(g)+2H2O(g)的反应热△H= ▲ 。
CO(g)+2H2O(g)的反应热△H= ▲ 。
③若在恒温恒容的容器内进行反应CO(g)+2H2(g) CH3OH(g),则可用来判断该反应达到平衡状态的标志有 ▲ 。(填字母)
CH3OH(g),则可用来判断该反应达到平衡状态的标志有 ▲ 。(填字母)
| A.CO百分含量保持不变 |
| B.容器中H2浓度与CO浓度相等 |
| C.容器中混合气体的密度保持不变 |
| D.CO的生成速率与CH3OH的生成速率相等 |
⑵工业上利用甲醇制备氢气的常用方法有两种:
①甲醇蒸汽重整法。该法中的一个主要反应为CH3OH(g) CO(g)+2H2(g),此反应能自发进行的原因是 ▲ 。
CO(g)+2H2(g),此反应能自发进行的原因是 ▲ 。
②甲醇部分氧化法。在一定温度下以Ag/CeO2—ZnO为催化剂时原料气比例对反应的选择性(选择性越大,表示生成的该物质越多)影响关系如图所示。则当n(O2)/n(CH3OH)=0.25时,CH3OH与O2发生的主要反应方程式为 ▲ ;在制备H2时最好控制n(O2)/n(CH3OH)= ▲ 。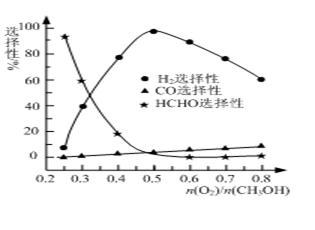
⑶在稀硫酸介质中,甲醇燃料电池负极发生的电极反应式为 ▲ 。
试题篮
()