黄铜矿(CuFeS2)是提取铜的主要原料,其煅烧产物Cu2S在1200℃高温下继续反应:2Cu2S + 3O2 →2Cu2O + 2SO2……① 2 Cu2O + Cu2S →6Cu + SO2……②。则
| A.反应①中还原产物只有SO2 |
| B.反应②中Cu2S只发生了氧化反应 |
| C.将1 molCu2S冶炼成 2mol Cu,需要O2 1mol |
| D.若1molCu2S完全转化为2molCu,则转移电子数为2NA |
化学中常用图像直观地描述化学反应的进程或结果。只改变一个条件,则下列对图像的解读正确的是
| A.图①说明此反应的正反应是吸热反应 |
| B.图②说明NO2的转化率b > a > c |
| C.图③说明t秒时合成氨反应达到平衡 |
| D.图④说明生成物D一定是气体 |
某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的两种或多种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):
关于该固体混合物,下列说法正确的是
| A.一定含有Al,其质量为4.5g |
| B.一定不含FeCl2,可能含有MgCl2和AlCl3 |
| C.一定含有MgCl2和FeCl2 |
| D.一定含有(NH4)2SO4和MgCl2,且物质的量相等 |
用下图所示装置除去含、
废水中的
时,控制溶液
为9~10,阳极产生的
将
氧化为两种无污染的气体,下列说法不正确的是

| A. | 用石墨作阳极,铁作阴极 |
| B. |
阳极的电极反应式为:
|
| C. |
阴极的电极反应式为:
|
| D. |
除去
|
磷酸分子间脱水会形成多种聚磷酸,它们的钠盐是广泛使用的食品添加剂。将48gNaOH与58.8g固态纯H3PO4在一定温度下加热,得到79.8g固体A和27g水,则A可能是
| A.Na3PO4 | B.Na4P2O7 |
| C.Na4P2O7和Na5P3O10 | D.Na3PO4、Na4P2O7和Na5P3O10 |
氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在,在一定条件下,NH4+经过两步反应被氧化成NO3¯,两步反应的能量变化示意图如下:

下列说法合理的是:
| A.该反应的催化剂是NO2¯ |
| B.升高温度,两步反应速率均加快,有利于NH4+转化成NO3¯ |
| C.在第一步反应中,当溶液中水的电离程度不变时,该反应即达平衡状态 |
| D.1 mol NH4+在第一步反应中与1 mol NO2-在第二步反应中失电子数之比为1:3 |
还原沉淀法是处理含铬(含Cr2O72﹣和CrO42﹣)工业废水的常用方法,过程如下: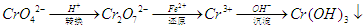 ,已知转化过程中反应为:2CrO42﹣(aq)+2H+(aq)==Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是
,已知转化过程中反应为:2CrO42﹣(aq)+2H+(aq)==Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是
| A.若用绿矾(FeSO4·7H2O)(M=278)作还原剂,处理1L废水,至少需要917.4g |
| B.溶液颜色保持不变,说明上述可逆反应达到达平衡状态 |
| C.常温下转换反应的平衡常数K=1×1014,则转化后所得溶液的pH=6 |
| D.常温下Ksp[Cr(OH)3]=1×10﹣32,要使处理后废水中c(Cr3+)降至1×10﹣5mol/L,应调溶液的pH=5 |
第三周期元素,最高价氧化物对应水化物(浓度均为0.01mol·L-1)的pH值与原子半径的关系如图所示,则下列说法正确的是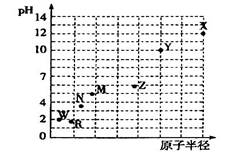
| A.气态氢化物的稳定性:N>R |
| B.Z的最高价氧化物对应的水化物能溶于稀氨水 |
| C.Y的单质是制造汽车、飞机、火箭的重要材料 |
| D.R的单质没有同素异形体 |
下列关系式或离子方程式中,正确的是
| A.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀:NH4++Al3++2SO42-+ 2Ba2++5OH-=AlO2-+NH3·H2O+2BaSO4↓ |
| B.常温下,0.1 mol·L-1 Na2S溶液中存在:c(OH-)=c(H+)+c(HS-)+c(H2S) |
C.常温下,将0.1 mol·L-1 CH3COOH溶液加水稀释,当溶液的pH从3.0升到4.0时,溶液中 的值增大到原来的10倍 的值增大到原来的10倍 |
| D.常温下,0.1 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液恰好完全反应时,溶液中一定存在:c(Na+)=c(A-)>c(OH-)=c(H+) |
pH=1的某溶液X中仅含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种(忽略水的电离及离子的水解),取该溶液进行连续实验,实验过程如下:
下列有关推断不正确的是
| A.沉淀H为Al(OH)3、BaCO3的混合物 |
| B.根据上述连续实验不能确定溶液X中是否含有Fe3+、Cl- |
| C.溶液X中一定含有Al3+、NH4+、Fe2+、SO42-、H+ |
| D.若溶液X为100 mL,产生的气体A为44.8 mL(标况),则X中c(Fe2+)="0.06" mol·L-1 |
25℃时在10 mL 0.1mol·L—1Na2CO3溶液中逐滴加入0.1 mol·L—1HCl溶液20 mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示。下列说法不正确的是
| A.HCl溶液滴加一半时,溶液pH>7 |
| B.当溶液的pH=8时,溶液中NaHCO3的物质的量浓度为0.1mol·L—1 |
| C.0.1 mol·L—1Na2CO3溶液中c(Na+)+c(H+)=c(OH—)+2c(CO32—)+c(HCO3—) |
| D.在M点:c(Na+)>c(CO32—)=c(HCO3—)>c(OH—)>c(H+) |
下列有关的离子方程式书写正确的是
A.向铜片中滴加浓硫酸并加热,有刺激性气味气体产生:Cu + 4H+ + SO42- Cu2+ + SO2↑ + 2H2O Cu2+ + SO2↑ + 2H2O |
B.服用阿司匹林过量出现水杨酸( )中毒反应,可静脉注射NaHCO3溶液: )中毒反应,可静脉注射NaHCO3溶液: +2 HCO3- → +2 HCO3- →  + 2 CO2↑ + 2 H2O + 2 CO2↑ + 2 H2O |
| C.20mL 1.0mol/L的明矾溶液与10mL 3.5mol/LBa(OH)2溶液混合充分反应: 3Ba2+ + 6OH- +2Al3+ +3SO42- ="=" 3BaSO4↓+2Al(OH)3↓ |
| D.向Ca(HCO3)2溶液中加入过量NaOH溶液,有白色沉淀生成:Ca2++2HCO3- +2OH-="=" CaCO3↓+2H2O+CO32- |
碳酸甲乙酯(CH3OCOOC2H5)是一种理想的锂电池有机电解液.生成碳酸甲乙酯的原理为:C2H5OCOOC2H5(g )+CH3OCOOCH3(g) 2CH3OCOOC2H5(g).其他条件相同时,CH3OCOOCH3的平衡转化率(α)与温度(T)、反应物配比( R=n(C2H5OCOOC2H5):n(CH3OCOOCH3)的关系如图所示.三种反应物配比分别为1:1、2:1、3:1.下列说法正确的是
2CH3OCOOC2H5(g).其他条件相同时,CH3OCOOCH3的平衡转化率(α)与温度(T)、反应物配比( R=n(C2H5OCOOC2H5):n(CH3OCOOCH3)的关系如图所示.三种反应物配比分别为1:1、2:1、3:1.下列说法正确的是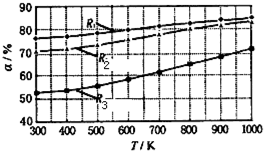
| A.该反应的逆反应△H>0 |
| B.增大反应物中CH3OCOOCH3的浓度能提高碳酸甲乙酯的平衡转化率 |
| C.650℃,反应物配比为1:1时,平衡常数K=6 |
| D.当C2H5OCOOC2H5与CH3OCOOC2H5生成速率比为1:2时,反应达到平衡状态 |
在不同温度下,向VL密闭容器中加入0.5 mol NO和0.5 mol活性炭,发生反应:
2NO(g)+C(s) N2 (g)+CO2 (g) △H= —QkJ·mol-1 (Q>0),达到平衡时的数据如下:
N2 (g)+CO2 (g) △H= —QkJ·mol-1 (Q>0),达到平衡时的数据如下:
| 温度/℃ |
n (C)/mol |
n(CO2)/mol |
| T1 |
|
0. 15 |
| T2 |
0. 375 |
|
下列有关说法正确的是
A.由上述信息可推知:T1>T2
B.T2℃时,若反应达平衡后再缩小容器的体积,c(N2):c(NO)增大
C.T1℃时,若开始时反应物的用量均减小一半,平衡后NO的转化率增大
D.T1℃时,该反应的平衡常数
如图所示是一个燃料电池的示意图,当此燃料电池工作时,下列分析中正确的是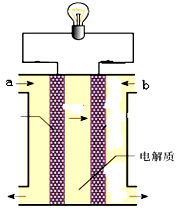
| A.如果a极通入H2,b极通入O2,NaOH溶液作电解质溶液,则通H2的电极上发生的反应为:H2-2e-=2H+ |
| B.如果a极通入H2,b极通入O2,H2SO4溶液作电解质溶液,则通 O2的电极上发生的反应为:O2+4e-+2H2O=4OH- |
| C.如果a极通入CH4,b极通入O2,NaOH作电解质溶液,则通CH4的电极上发生的 反应为:CH4-8e-+10 OH-=CO32-+7H2O |
| D.如果a极通入H2,b极通入O2,NaOH溶液作电解质溶液,则溶液中的OH-离子向b极附近移动 |
试题篮
()