氮元素的化合物应用十分广泛。请回答:
(1)硝化法是一种古老的生产硫酸的方法,同时实现了氮氧化物的循环转化,主要反应为:NO2(g)+SO2(g) SO3(g)+NO(g) △H=-41.8 kJ·mol-1已知:2SO2(g)+O2(g)
SO3(g)+NO(g) △H=-41.8 kJ·mol-1已知:2SO2(g)+O2(g) 2SO3(g) △H=-196.6 kJ·mol-1写出NO和O2反应生成NO2的热化学方程式 。
2SO3(g) △H=-196.6 kJ·mol-1写出NO和O2反应生成NO2的热化学方程式 。
(2)298 K时,在2L固定体积的密闭容器中,发生可逆反应:2NO2(g) N2O4(g) ΔH=-a kJ·mol-1 (a>0)。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题:
N2O4(g) ΔH=-a kJ·mol-1 (a>0)。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题:

①298k时,该反应的平衡常数为 L·mol-1(精确到0.01)。
②下列情况不是处于平衡状态的是 :
A.混合气体的密度保持不变;
B.混合气体的颜色不再变化;
C.气压恒定时
③若反应在398K进行,某时刻测得n(NO2)="0.6" moln(N2O4)=1.2mol,则此时V(正) V(逆)(填“>”、“<”或“=”)。
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。试分析图中a、b、c、d、e五个点。

①b点时,溶液中发生水解反应的离子是______;
②在c点,溶液中各离子浓度由大到小的排列顺序 。
③d、e点对应溶液中,水电离程度大小关系是d e(填“>”、“<”或“=”)。
铝是地壳中含量最高的金属元素,在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中,其单质、合金及其化合物在生产生活中的应用日趋广泛,铝土矿是生产铝及其化合物的重要原料。
(1)铝元素在元素周期表中的位置是 。
(2)铝电池性能优越,铝一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。

①该电池的总反应化学方程式为 ;
②电池中NaCl的作用是 。
③以铝一空气电池为电源电解KI溶液制取KIO3(石墨为电极材料)时,电解过程中阳极的电极反应式为 。
(3)工业上用铝土矿制备铝的某种化合物的工艺流程如下。

在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①检验滤液B中是否还含有铁元素的方法为: (注明试剂、现象)。
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为 (填代号)。
| A.氢氧化钠溶液 | B.硫酸溶液 | C.氨水 | D.二氧化碳 |
③由滤液B制备氯化铝晶体涉及的操作为: 蒸发浓缩、冷却结晶、 、洗涤。
④SiO2和NaOH焙烧制备硅酸钠,可采用的装置为 (填代号)。

B.[实验化学]2-苯基-2-丁醇是重要的有机合成中间体,以溴苯为原料合成该中间体的反应原理如下:

【实验装置】
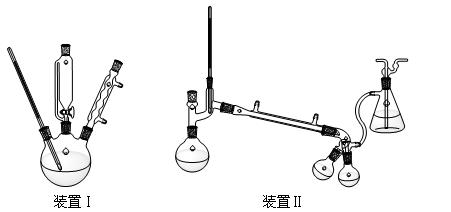
【实验步骤】
步骤1:将镁条置于装置Ⅰ的三颈烧瓶中,加入100 mL乙醚(ρ=0.71g·cm-3),在冷却条件下缓缓滴入溴苯,微热并加入一小块碘引发反应①。
步骤2:滴加14.2 mL丁酮和30 mL乙醚混合物,发生反应②;滴加入20%的NH4Cl水溶液,发生反应③。
步骤3:分出油层,用水洗涤至中性,用无水CaCl2干燥。
步骤4:用装置Ⅱ先蒸出乙醚,再蒸馏出产品。
(1)步骤1中加入碘的作用是 。
(2)装置Ⅰ中滴加液体所用的仪器的名称是 ,反应②需将三颈烧瓶置于冰水中,且逐滴加入丁酮和乙醚,其目的是 。
(3)步骤三中分离出油层的具体实验操作是 。
(4)装置Ⅱ采用的是减压蒸馏,实验时需将吸滤瓶需连接 ;采用这种蒸馏方式的原因是 。
天然气是重要的化石燃料和工业原料,其主要成分为甲烷。
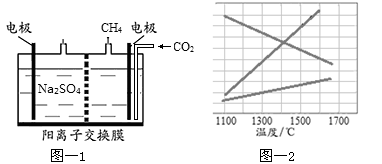
(1)CO2气体排放会产生温室效应,将通入CO2碳化了的水在如图1所示的电解池阴极区进行电解,可以直接产生甲烷,加入硫酸钠为了增加导电性。
①写出电解时阴极的电极反应式 。
②电解时电解池采用阳离子交换膜,若采用阴离子交换膜会对电解产生的影响为 。
(2)将甲烷和硫反应可以制备CS2,其流程如下:
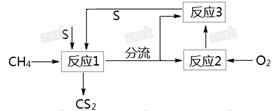
①反应1产生两种含硫的物质,则该反应方程式为 。
②反应当中,每有1molCS2生成时,需要消耗O2的物质的量为 。
③为了将含硫化合物充分回收,实验时需对反应1出来的气体分流,则进入反应2和反应3的气体气体关系为 。
(3)甲烷在高温下分解生成烃和氢气,若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图2所示,甲烷在高温下分解反应的化学方程式为 。
绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
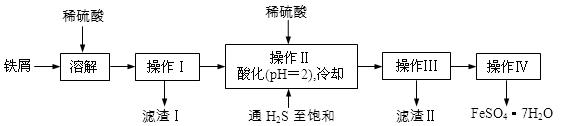
已知:室温下饱和H2S溶液的pH约为3.9,SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5。
(1)通入硫化氢的作用是:
①除去溶液中的Sn2+离子
②除去溶液中的Fe3+,其反应的离子方程式为 ;
操作II,在溶液中用硫酸酸化至pH=2的目的是 。
(2)操作IV的顺序依次为: 、 、过滤、洗涤、干燥。
(3)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:
①除去晶体表面附着的硫酸等杂质;
② 。
(4)测定绿矾产品中Fe2+含量的方法是:
a.称取一定质量绿矾产品,配制成250.00mL溶液;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000 mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。滴定时发生反应的离子方程式为:5Fe2++MnO4—+8H+=5Fe3++Mn2++4H2O)。
①用硫酸酸化的0.01000 mol/LKMnO4溶液滴定时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视 。
②判断此滴定实验达到终点的方法是 。
③若用上述方法测定的样品中FeSO4·7H2O的质量分数偏低(测定过程中产生的误差可忽略),其可能原因有 。
某科研小组在900℃的空气中合成出化学式为La2Ca2MnOx的超导体材料,其中La以+3价存在。为确定x的值,进行如下分析:
步骤1:准确称取0.5250g超导体材料样品,放入锥形瓶中,加25.00mL0.06000mol•L-1Na2C2O4溶液(过量)和25mL6mol•L-1HNO3溶液,在60-70℃下充分摇动,约半小时后得到无色透明溶液A(该条件下,只有Mn元素被还原为Mn2+,Na2C2O4被氧化为CO2)。
步骤2:用0.02000mol•L-1KMnO4溶液滴定溶液A至终点,消耗10.00mL KMnO4溶液。
(1)步骤1反应后溶液中Mn2+的物质的量浓度为0.02000mol•L-1。常温下,为防止Mn2+形成Mn(OH)2沉淀,溶液的pH的范围为 [已知Mn(OH)2的Ksp=2.0×10-13]
(2)步骤2滴定终点的现象是 。
(3)步骤2滴定终点读数时俯视刻度,其他操作都正确,则所测x的值将 (填“偏大”、“偏小”或“不变”)。
(4)求x的值(写出计算过程)。
(15分)氨基甲酸铵(NH2COONH4)是一种白色固体,受热易分解。某小组模拟制备氨基甲酸铵,反应如下(且温度对反应的影响比较灵敏):2NH3(g)+CO2(g)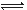 NH2COONH4(s) ΔH<0
NH2COONH4(s) ΔH<0
(1)如用下图I装置制取氨气,可选择的试剂是 。
(2)制备氨基甲酸铵的装置如下图Ⅱ所示,把NH3和CO2通入CCl4中,不断搅拌混合,生成的氨基甲酸铵的小晶体悬浮在CCl4中。 当悬浮物较多时,停止制备。
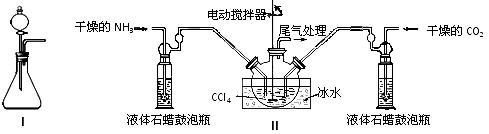
注:CCl4与液体石蜡均为惰性介质。
①发生器用冰水冷却的原因是 ,液体石蜡鼓泡瓶的作用是 。
②从反应后的混合物中分离出产品的实验方法是 (填写操作名称)。为了得到干燥产品,应采取的方法是 (填写选项序号)。
a.常压加热烘干
b.高压加热烘干
c.减压40℃以下烘干
(3)制得的氨基甲酸铵可能含有碳酸氢铵、碳酸铵中的一种或两种。
①设计方案,进行成分探究,请填写表中空格。
限选试剂:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、稀盐酸。
| 实验步骤 |
预期现象和结论 |
| 步骤1:取少量固体样品于试管中,加入蒸馏水至固体溶解。 |
得到无色溶液 |
| 步骤2:向试管中加入过量的BaCl2溶液,静置。 |
若溶液不变浑浊,证明固体中不含碳酸铵。 |
| 步骤3:向试管中继续加入 。 |
,证明固体中含有碳酸氢铵。 |
②根据①的结论:取氨基甲酸铵样品3.95 g,用足量氢氧化钡溶液充分处理后,过滤、洗涤、干燥,测得沉淀质量为1.97 g。则样品中氨基甲酸铵的物质的量分数为 。
(18分)Ⅰ.将广泛应用于航空工业的某合金(两种金属组成)投入过量浓硝酸中,合金与硝酸剧烈反应,放出红棕色气体X和蓝绿色溶液Y。若将少量Y滴入NaCl溶液中,只产生白色沉淀。
(1)氯元素在周期表中的位置 。
(2)组成合金的金属是 (填选项字母)。
| A.Cu,Mg | B.Cu,Al | C.Cu,Fe | D.Cu,Ag |
(3)X是大气污染物之一,利用氨水可以将SO2和X同时吸收处理,原理如下图所示:
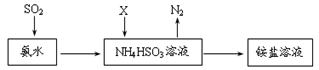
NO2被吸收的离子方程式是 。
Ⅱ.某研究小组为了探究仅一种白色粉末状固体X(仅含四种元素)的组成和性质,称取6.3g固体X,设计并完成了如下实验:
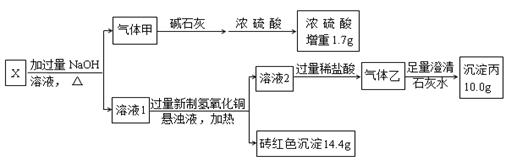
已知:Cu2O+2H+==Cu+Cu2++H2O
请回答下列问题:
(1)画出沉淀丙中金属元素的原子结构示意图 ,写出气体甲的电子式 。
(2)X的化学式是 。
(3)生成砖红色沉淀的原因是 (用化学方程式表示)。
(4)在加热条件下,用氢气还原砖红色沉淀,写出该反应的化学方程式 ,有人提出产物中可能还含有Cu2O,请设计实验方案验证之 。
(15分)Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定。
Ⅰ.制备Na2S2O3·5H2O
反应原理:Na2SO3(aq)+S(s) Na2S2O3(aq)
Na2S2O3(aq)
实验步骤:
①称取20 g Na2SO3加入圆底烧瓶中,再加入80 mL蒸馏水。另取4 g研细的硫粉,用3 mL乙醇润湿,加入上述溶液中。
②安装实验装置(如图所示,部分夹持装置略去),水浴加热,微沸60 min。

③趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O3·5H2O,经过滤、洗涤、干燥,得到产品。
回答问题:
(1)硫粉在反应前用乙醇润湿的目的是__________________________。
(2)仪器a的名称是________,其作用是____________________。
(3)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是 ,检验是否存在该杂质的方法是 。
(4)该实验一般控制在碱性环境下进行,否则产品发黄,用离子反应方程式表示其原因 。
Ⅱ.测定产率
将所得产品配成500mL溶液,取该溶液20mL,以淀粉作指示剂,用0.100 0 mol·L-1碘的标准溶液滴定。反应原理为2S2O32- + I2 ="=" S4O62- + 2I-
(5)滴定至终点时,溶液颜色的变化_______________。
(6)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为______mL,则该实验的产率为 。(保留三位有效数据)

Ⅲ.Na2S2O3的应用
(7)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,常用作脱氯剂,该反应的离子方程式为_____。
甲、乙两个研究性学习小组为测定氨分子中氮、氢原子个数比,设计了如下实验流程:

实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜。反应完成后,黑色的氧化铜转化为红色的铜。
下图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。

甲小组测得:反应前氧化铜的质量m1 g、氧化铜反应后剩余固体的质量m2 g、生成氮气在标准状下的体积V1 L。
乙小组测得:洗气前装置D的质量m3 g、洗气后装置D的质量m4 g、生成氮气在标准状况下的体积V2 L。
请回答下列问题:
(1)写出仪器a的名称____________。
(2)检查A装置气密性的操作是_______________________________________。
(3)甲、乙两小组选择了不同的方法制取氨气,请将实验装置的字母编号和制备原理填写在下表的空格中。
| |
实验装置 |
实验药品 |
制备原理 |
| 甲小组 |
A |
氢氧化钙、硫酸铵 |
反应的化学方程式为 ①___________________________________________。 |
| 乙小组 |
__②__ |
浓氨水、氢氧化钠 |
用化学平衡原理分析氢氧化钠的作用③___________________________________________ |
(4)甲小组用所测数据计算出氨分子中氮、氢的原子个数之比为____________。
(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数比明显小于理论值,其原因是__________。
为此,乙小组在原有实验的基础上增加了一个装有某药品的实验仪器,重新实验。根据实验前后该药品的质量变化及生成氮气的体积,得出了合理的实验结果。该药品的名称是____________。
含有硫元素的物质种类繁多。某学校兴趣小组对其中两类物质进行性质探究。
Ⅰ.已知可溶性硫化物在溶液中能与硫单质反应,生成可溶性的多硫化物(如Na2Sn)。
请回答下列问题:
(1)多硫化物Na2Sn溶于水的电离方程式为___________________________。
(2)在浓Na2S溶液中滴入少量氯水,经振荡,未发现沉淀物生成,其原因是(用离子方程式表示,下同)___________________________________________________。
(3)在足量氯水中,滴入少量Na2S溶液,经振荡,也未发现沉淀物生成,若再加入盐酸酸化的BaCl2溶液,即可产生白色沉淀,其原因是_____________________________。
Ⅱ.浓硫酸具有氧化性,不同浓度的硫酸氧化性不同。为了探究浓度对硫酸氧化性的影响,某学习小组进行了如下探究:称取无锈铁钉(碳素钢)12.0 g放入30.0 mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。为了测定气体Y中SO2的含量,设计如下三种方案:
方案①:取672 mL(标准状况)气体Y通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66 g。
方案②:向V mL c mol/L酸性高锰酸钾溶液中缓慢通入a L(标准状况)气体Y,溶液恰好完全褪色。
方案③:取V mL(标准状况)气体Y缓慢通入足量氢氧化钡溶液中,充分反应后,过滤、洗涤、烘干,称得固体质量为m g。
(1)其中不合理的是方案_____(填序号),理由是___________________________________。
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含有少量的H2和CO2。为此设计了下列探究实验装置(夹持装置已略去)。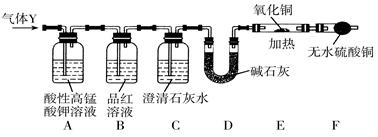
(2)装置A中试剂的作用是__________________________。
(3)简述确认气体Y中含有CO2的实验现象:________________________________。
(4)有同学根据“F干燥管中无水硫酸铜是否变蓝色”确 认气体Y中是否有氢气,你认为是否合理?______(填“合理”或“不合理”),简述理由:___________________________________。
(13分)Cr2O72-和CN-是工业废水中常见的污染物.若利用下列流程可对分别含两种离子的废水进行综合处理: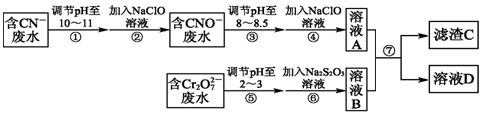
已知:Cr3+也有一定毒性,Cr3+在pH=6.0时开始沉淀,pH=8.0时沉淀完全.
回答下列问题:
(1)已知步骤②中无气体生成,写出反应的离子方程式______________________.
步骤④中NaClO可将CNO-处理为完全无害的溶液,该过程中有两种无毒的不支持燃烧的气体产生,写出这两种气体的化学式____________________________.
(2)步骤⑥的反应为S2O32-+Cr2O72-+H+―→SO42-+Cr3++H2O(未配平),则每处理1 mol Cr2O72-转移________mol电子.
(3)滤渣C的化学式为Cr(OH)3,溶液A和溶液B混合可使废水中的Cr3+沉淀的原因是______________________________________________________.
(4)步骤⑦的操作名称为___________,若该操作在实验室中进行,则所需的玻璃仪器为________.
SO2是一种大气污染物,某兴趣小组欲探究SO2的性质及绿色实验方法,设计如下方案:

(1)B、C、D分别用于检验SO2的漂白性、还原性和氧化性。其中C、D分别为碘水和硫化氢的水溶液,则B中所盛试剂为________,C中反应的离子方程式为____________________________________________。
(2)为了实现绿色实验的目标,某同学重新设计了如图A2的制取装置来代替A1装置,与A1装置相比,A2装置的优点是_______________________________________(任写一点即可)。
(3)E中用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO32-、SO42-、HSO3-等阴离子。已知亚硫酸氢盐一般易溶于水,SO2也易溶于水。现有仪器和试剂为小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2 mol·L-1盐酸、2 mol·L-1HNO3、1 mol·L-1BaCl2溶液、1 mol·L-1Ba(OH)2溶液、品红溶液、蒸馏水。请设计实验证明“吸收液”中存在SO32-和HSO3-,完成下表的实验操作、预期现象与结论:
| 实验操作 |
预期现象与结论 |
| 步骤1:取适量“吸收液”于小烧杯中,用胶头滴管取1 mol·L-1 BaCl2溶液向小烧杯滴加直至过量 |
若出现白色浑浊,则溶液中存在SO32-或SO42- |
| 步骤2:将小烧杯中的浊液过滤、洗涤,再用适量水把附在滤纸上的固体冲入另一小烧杯中;向冲下的固体_______________________________ |
|
| 步骤3:____________________________ ________________________________ |
|
(15分)镁、铝、铁及其化合物在生产、生活中有着广泛的应用
I:实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4,主要流程如下:

(1)已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]=3×10-34,该温度下向浓度均为0.01 mol·L-1的MgCl2和AlCl3混合溶液中逐滴加入氨水,先生成 沉淀(填化学式)。
(2)高温焙烧时发生反应的化学方程式 ,洗涤沉淀时的方法是 。
(3)常温下如果向AlCl3饱和溶液中不断通人HCl气体,可析出AlCl3·6H2O晶体,结合化学平衡移动原理解释析出晶体的原因: 。
Ⅱ:某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体。为此,他们设计了如下装置验证所产生的气体。

(1)G装置的作用是 。
(2)证明有SO2生成的现象是 ,为了证明气体中含有氢气,装置E和F中加入的试剂分别为 、 。
(3)若将铁丝换成铜丝,反应后的溶液没有出现预计的蓝色溶液,而出现了大量白色固体,原因是 。
[实验化学]邻叔丁基对苯二酚(TBHQ) 是一种新颖的食品抗氧剂,其制备原理为:
实验过程中的主要步骤如下:
步骤1.向三口烧瓶中加入5.5g对苯二酚,5.OmL浓磷酸及20mL二甲苯(装置如图所示),启动搅拌器。
步骤2.缓缓加热到100-110°C,慢慢滴加7.5mL叔丁醇和5mL二甲苯组成的溶液,30-60min内滴完。
步骤3.升温到135-140°C,恒温回流2.5h。
步骤4.将反应液冷却到120°C,直到反应完成
步骤5.将反应液倒入烧杯,并用热水洗涤三口烧瓶,洗液并入烧杯中。
步骤6.冷却结晶,抽滤,回收滤液中的二甲苯和磷酸
步骤7.用二甲苯重结晶、脱色、冷水洗涤、干燥
(1)磷酸在实验中的作用是_____。
(2)本实验中二甲苯的作用是_____。
(3)步骤4中反应完成的标志是_____。
(4)步骤7脱色时,可用的脱色剂是_____。
(5)对合成得到的产品表征,还需要的主要现代分析仪器是_____、_____。
试题篮
()