某研究性学习小组,利用固体Na2SO3与中等浓度的H2SO4反应,制备SO2气体并进行有关性质探究实验。该反应的化学方程式为:Na2SO3(固)+H2SO4=Na2SO4 + SO2↑+H2O。除固体Na2SO3和中等浓度的H2SO4外,可供选择的试剂还有:
①溴水 ②浓H2SO4 ③品红试液 ④紫色石蕊试液 ⑤澄清石灰水 ⑥NaOH溶液
回答下列问题:
(1)欲验证SO2的漂白作用,应将SO2气体通入 中(填物质编号),观察到的现象是 ;
(2)欲验证SO2的还原性,应将SO2气体通入 中(填物质编号),观察到的现象是 ;
(3)为说明SO2的氧化性,通常利用的反应是 (写化学反应方程式);
(4)为防止多余的SO2气体污染环境,应将尾气通入 中(填物质编号),
反应离子方程式为 ;
(5)有一实验小组发现,SO2产生缓慢(不考虑SO2在溶液中的溶解,实验中也不存在漏气、反应温度等装置和操作上的问题),请你推测可能的原因(至少填写一种):
① ,② 。
(16分)(1)下图所示都是实验室中制取气体的装置,其中能实现随开随用,随关随停的是____________,其中仪器B的名称是____________。
(2)请简述检验装置III的气密性的方法_________________________________.
(3)实验室利用铜和浓硫酸制取SO2,可选择上述气体发生装置的_________来实现。请写出其反应的化学方程式___________________________.
(4)若要用浓硫酸(质量分数为98%,密度为1.84g/mL)配制1 mol/L的稀硫酸500mL,则需要量取浓硫酸的体积为__________mL,所需的玻璃仪器有量筒、玻璃棒、烧杯、_________。
(5)①若在100 ml 18 mol/L浓硫酸中加入过最铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是__________________。
| A.40.32 L | B.30.24 L | C.20.16 L | D.13.44 L |
②若使上述反应中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程_ 。
下图是实验室制取、提纯氯气及研究氯气性质的装置图。请回答:
(1)上图实验室制备氯气的化学反应方程式为 。
(2)通常用向上排空气法或者排饱和食盐水法收集氯气,若要利用C瓶收集到干燥纯净的氯气,B瓶所装的试剂是 。(填名称)
(3)若D瓶中装有硝酸银溶液,则观察到的现象是 。
(4)E装置用来 ,写出E装置中发生化学反应的离子方程式 。
实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL。根据这两种溶液的配制情况回答下列问题。
(1)在下图所示仪器中,配制上述溶液肯定不需要的是_________(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是_____ 。
(2)在容量瓶的使用方法中,下列操作不正确的是____________
| A.使用容量瓶前检验是否漏水 |
| B.容量瓶用水洗净后,再用待配溶液洗涤 |
| C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。 |
| D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。 |
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(3)根据计算用托盘天平称取的质量为 g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度 0.1mol/L(填“大于”“小于”或“等于”)。
(4)根据计算得知,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为 mL,如果实验室有15mL、20mL、50mL量筒,应选用 mL量筒最好。
某学生做浓硫酸性质的实验:
在一支试管中放入一块很小的铜片,再加入2mL浓硫酸,然后把试管固定在铁架台上。把一小条蘸有品红溶液的滤纸放入带有单孔橡皮塞的玻璃管中。塞紧试管口,在玻璃管口处缠放一团蘸有NaOH溶液的棉花。加热试管,观察现象。
回答下列问题:
(1)写出试管中发生反应的化学方程式 。
(2)试管中的液体反应一段时间后,b处滤纸条的变化为 ,待试管中反应停止后,给玻璃管放有蘸过品红溶液的滤纸处微微加热,滤纸条的变化为 。
(3)蘸有NaOH溶液的棉花团作用是 。
(4)硫酸型酸雨的形成过程可用下列反应中的 来表示。
A:O2+H2O H2SO3
H2SO3
B:O2+2H2SO3=2H2SO4
C:SO2+H2O2=H2SO4
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL。试回答下列问题:
(1)锥形瓶中的溶液从 色变为 色时,停止滴定。
(2)滴定时边滴边摇动锥形瓶,眼睛应观察
A、滴定管内液面的变化 B、锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是 由此造成的测定结果 (偏高、偏低或无影响)
(4)步骤②缺少的操作是
(5)下图,是某次滴定时的滴定管中的液面,其读数为 mL
(6)根据下列数据:
| 滴定次数 |
待测液体积(mL) |
标准盐酸体积(mL) |
|
| 滴定前读数(mL) |
滴定后读数(mL) |
||
| 第一次 |
25.00 |
0.50 |
20.40 |
| 第二次 |
25.00 |
4.00 |
24.10 |
请计算待测烧碱溶液的浓度(保留四位小数) mol/L
某校化学研究性学习小组设计如下实验方案,测定NaHCO3和Na2CO3混合物中NaHCO3的质量分数。
方案一:按下图装置进行实验。并回答以下问题。
①按图组装仪器并检查装置的气密性。
②实验前称取17.90g样品,从分液漏斗滴入6mol·L-1的硫酸,直到不再产生气体时为止, 从导管A处缓缓鼓入一定量的空气。
③实验结束后测得U型管增重 8.80g。
(1)B瓶中装的试剂为______,C装置的作用是 。
(2)从导管A处缓缓鼓入一定量的空气的目的是 。
(3)该样品中NaHCO3的质量分数为 。
方案二:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量Ba(OH)2溶液。过滤洗涤,干燥沉淀,称量固体质量,进行有关计算。
请回答:实验中判断沉淀是否完全的方法是 。
电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
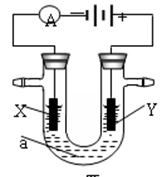
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为 。
在X极附近观察到的实验现象是 。
②Y电极上的电极反应式为 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是 ,电极反应式为 。
②Y电极的材料是 ,电极反应式为 。(说明:杂质发生的电极反应不必写出)
电解一段时间后,CuSO4溶液的浓度将 (填“变大”、“变小”或“不变”)
根据下图所示装置回答问题:

(1)装置A中a电极的电极反应式为 ,b电极的电极反应式为 ;
(2)装置B中C为 极,电极反应式为 。
(3)当铁电极的质量变化为19.2g时,a极上消耗O2在标准状况下的体积为 L。
(4)当装置A中消耗0.05mol氢气时,装置B中溶液的pH为 。(溶液体积为100mL不变)
(5)若将装置B改为电解精炼铜,则粗铜作 极,另一极反应为 。
下图甲池和乙池中的四个电极都是惰性材料,乙池溶液分层,上层溶液为盐溶液,呈中性,请根据图示回答下列问题:

(1)通入乙醇(C2H5OH)的惰性电极的电极反应式为 。
若甲池可以充电,充电时A接电源的负极,此时B极发生的电极反应式为 。
(2)在乙池反应过程中,可以观察到 电极周围的溶液呈现棕褐色,反应完毕后,用玻璃棒搅拌溶液,则下层溶液呈现紫红色,上层接近无色,C极发生的电极反应 。
(3)若在常温常压下,1gC2H5OH燃烧生成CO2和液态H2O时放出29.71kJ热量,表示该反应的热化学方程式为 。
按下图所示装置进行实验,并回答下列问题:
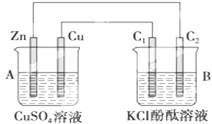
(1)锌极为________极,电极反应式为 ;
铜极为________极,电极反应式为 ;
(2)石墨棒C1为________极,电极反应式为 ;
石墨棒C2附近发生的实验现象为 。
(3)当C2极析出224 mL气体(标准状况)时,锌的质量 (填“增加”或“减少”) g;
CuSO4溶液的质量 (填“增加”或“减少”) g。
工业上SnSO4是一种重要的硫酸盐,广泛应用于镀锡工业,其制备路线如下:
提示:①已知在酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式。
②已知Ksp[Sn(OH)2] =1.0×10-26
回答下列问题:
(1)SnCl2用盐酸而不用水直接溶解的原因是_____,加入Sn粉的作用是____。
(2)反应I生成的沉淀为SnO,写出该反应的离子方程式_______________。
(3)检验沉淀已经“漂洗”干净的方法__________________________。
(4)反应Ⅱ硫酸的作用之一是控制溶液的pH,若溶液中c(Sn2+)=1.0mol•L-1,则应控制溶液pH______。
(5)酸性条件下,SnSO4还可以用作双氧水去除剂,请写出发生反应的离子方程式________。
下图为实验室干馏煤的装置图。请回答下列问题:

(1)指出图中个仪器的名称:a. ;b. ;c. ;d. 。
(2)装置c的作用是 ,d中的液体有 和 。其中无机物里溶有 ,
可用 检测出来,有机化合物可以通过 的方法使其中的重要成分分离出来。在170-230 ℃时可以得到 ,加热到230 ℃,可以得到 。
(3)e处点燃的气体主要是 ,火焰的颜色是 色。
海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
已知:①海水中溴元素(以Br-表示)的浓度0.068g/L;
②Br2的沸点为59 ℃,微溶于水,有毒性和强腐蚀性。

(1)请写出一种海水淡化的方法:_____________。
(2)海水中溴离子的物质的量浓度为_____________ 。
(3)步骤Ⅰ中已获得低溶度的含Br2溶液,步骤Ⅱ中又将Br2还原为Br-,步骤Ⅲ又得到Br2,其目的为________________。
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为 。
(5)工业溴提纯可用蒸馏法,蒸馏时加热方法最好采用 ,蒸馏装置中仪器连接均不能用橡胶塞和橡胶管,其原因是_________________________________。
在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用下面的工艺流程生产单质碘:

试完成下列问题:
(1)乙、丁中溶质的化学式:乙____________;丁____________。
(2)第④步操作中用稀H2SO4浸洗的目的是____________(填写字母编号)。
a.除去未反应的 b.除去未反应的I-
b.除去未反应的I-
c.除去未反应的Fe d.除去碱性物质
(3)第⑦步操作可供提纯I2的一种方法是____________(不要求写具体步骤)。
(4)实验室检验I2的方法是________________________。
(5)甲物质见光易变黑,其原因是______________________________(用化学方程式表示)。
试题篮
()