16.实验室有一瓶混有氯化钠的氢氧化钠固体试剂,经测定NaOH的质量分数约为82.0%,为了验证其纯度,用浓度为0.2mol/L的盐酸进行滴定,试回答下列问题:
(1)托盘天平称量5.0g固体试剂,用蒸馏水溶解于烧杯中,并振荡,然后立即直接转入 500mL容量瓶中,恰好至刻度线,配成待测液备用。请改正以上操作中出现的五处错误。
① ,② ,③ ,
④ ,⑤ 。
(2)将标准盐酸装在25.00mL 滴定管中,调节液面位置在 处,并记下刻度。
(3)取20.00mL待测液,待测定。该项实验操作的主要仪器有 。
用 试剂作指示剂时,滴定到溶液颜色由 刚好至 色时为止。
(4)滴定达终点后,记下盐酸用去20.00mL,计算NaOH的质量分数为 。
(5)试分析滴定误差可能由下列哪些实验操作引起的 。
| A.移待测液至容量瓶时,未洗涤烧杯 |
| B.酸式滴定管用蒸馏水洗涤后,直接装盐酸 |
| C.滴定时,反应容器摇动太激烈,有少量液体溅出 |
| D.滴定到终点时,滴定管尖嘴悬有液滴 |
E.读数(滴定管)开始时仰视,终点时俯视
25.(12分)可用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)。请填空:
(1)试管a中需加入浓硫酸、冰醋酸和乙醇各2mL,正确的加入顺序用操作是 。
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是 。
(3)实验中加热试管a的目的是: ; 。
(4)试管b中加有饱和Na2CO3溶液,其作用是 。
(5)反应结束后,振荡试管b,静置。反应结束后,试管B内的液体分成两层,乙酸乙酯在 层(填写“上”或“下”).若分离10mL该液体混合物需要用到的主要玻璃仪器是 .
(15分)高纯MnCO3是制备电讯器材、颜料、催化剂及高性能磁性材料的主要原料。实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:

(1)制备MnSO4溶液:在三颈烧瓶中加入一定量MnO2和水,搅拌,通入SO2和N2混合气体,反应3h,停止通入SO2,继续反应片刻,过滤。
①依次写出烧瓶中和烧杯中反应的化学方程式为 、 。
②反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定,不改变固液投料的条件下,可采取的合理措施有 。
③若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如图。导致溶液中Mn2+、SO42-的浓度变化产生明显差异的主要原因是 。

(2)制备高纯MnCO3固体:已知MnCO3难溶于水和乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀的pH=7.7。由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤如下[实验中可选用的试剂限制为:Ca(OH)2、NaHCO3、Na2CO3、C2H5OH]。

步骤①中为防止生成Mn(OH)2沉淀,注意 ;选择步骤②中所用试剂的理由是 ;步骤③是 。
(3)MnCO3在空气中加热易转化为不同价态的锰的氧化物,其固体残留率随温度的变化如图所示。

则加热至300℃时,发生反应的化学方程式为 ;图中点D对应固体的成分为 (填化学式)。
(15分)某同学利用下列装置实现铜与浓硝酸、稀硝酸反应,过程如下:
I.取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu2(OH)2CO3]。
Ⅱ.将洗涤后的铜丝做成匝数较多的螺旋状。
III.按如图所示装置连接仪器、检查气密性、装入化学试剂。

(1)写出Cu丝在空气中形成铜绿的化学反应方程式 。
(2)将铜丝绕成螺旋状的原因是__________写出过程III中检查气密性的方法 。
(3)过程III的后续操作如下:
①打开止水夹a和b,轻推注射器,使浓硝酸与铜丝接触,观察到的现象是 ,一段时间后使反应停止的操作是 ,关闭a,取下注射器。
②打开b和分液漏斗活塞,当玻璃管充满稀硝酸后,关闭b和分液漏斗活塞,打开a,观察到有气泡产生。稀硝酸充满玻璃管的实验目是 ,该反应的离子方程式是 。
(4)另取3支盛满NO2气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致。结果如下表所示(忽略温度对气体体积的影响):
| 实验编号 |
水温/℃ |
液面上升高度 |
| 1 |
25 |
超过试管的2/3 |
| 2 |
50 |
不足试管的2/3 |
| 3 |
0 |
液面上升超过实验1 |
①根据上表得出的结论是温度越 (填“高”或“低”),进入试管中的溶液越多。
②假设反应在标准状况下进行,小试管的容积为VL,将小试管倒立在盛有足量水的水槽中,若溶液溶质不扩散,则得到的溶液的物质的量浓度是__________________mol/L,若使液体充满试管,应该充入氧气的体积是______。
(选做)【化学——选修2:化学与技术】
下图是某企业设计的硫酸—磷肥—水泥联产、海水—淡水多用、盐—热—电联产的三大生态产业链流程图。

根据上述产业流程回答下列问题:
(1)该流程①、②、③、④、⑤为能量或物质的输送,请分别写出输送的主要物质的化学式或能量形式:① 、② 、③ 、④ 、⑤ 。
(2)沸腾炉发生反应的化学方程式: 。磷肥厂的主要产品是普钙(磷酸二氢钙和硫酸钙),写出由磷矿石和硫酸反应制普钙的化学方程式 。
(3)用1吨硫铁矿(FeS2的质量分数为36%)接触法制硫酸,制硫酸的产率为65%,则最后能生产出质量分数为98%的硫酸 吨。
(4)热电厂的冷却水是 ,该流程中浓缩盐水除提取盐以外还可提取的物质有 (写出一种即可)。
(5)根据现代化工厂设计理念请提出高炉炼铁厂废气、废渣及多余热能的利用设想。
, (写出两点即可)。
(13分)某学习小组利用下列装置进行CO2与饱和Na2CO3溶液反应制备NaHCO3实验

(1)选取必要的实验装置,正确的连接顺序为______(填序号)
(2)为确定制得的固体样品是纯净的NaHCO3 小组同学提出下列实验方案:
甲方案:将样品溶液与饱和澄清石灰水反应,观察现象。
乙方案:将样品溶液与BaCl2 观察现象。
丙方案:测定PH法
丁方案:热重分析法
①判定甲方案______(填“可行”或“不可行”)
②为判断乙方案的可行性,某同学用分析纯的NaHCO3配制的溶液,与BaCl2溶液等体积混合进行实验,结果如下。
| NaHCO3溶液 BaCl2溶液 |
0.2mol/L |
0.1mol/L |
0.02mol/L |
| 0.2mol/L |
浑浊 |
浑浊 |
少许浑浊 |
| 0.1mol/L |
浑浊 |
少许浑浊 |
无现象 |
| 0.02mol/L |
少许浑浊 |
无现象 |
无现象 |
(i)此实验可说明乙方案是不可行的。请结合以下数据,并通过计算说明产生浑浊的原因。答:______。[已知:0.1 mol·L-1NaHCO3溶液电离出的c(CO32-)为0.0011 mol·L-1,Ksp(BaCO3)=5.1×10-9]
(ⅱ)产生浑浊的离子方程式为_________________。
③使用pH计进行测定的丙方案是______________。
④进行丁方案实验,测得样品在不同升温速率下 的热重曲线如图。

请填空:
(i)样品的纯度为___________。
(ⅱ)升温速率对实验结果_______(填“有较大”、“有较小”或“没有”)影响。
(14分)黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2,现有一种天然黄铜矿(含少量脉石SiO2),为了测定该黄铜矿的纯度,某同学设计了如下实验:


现称取研细的黄铜矿样品1.150 g,在空气存在下进行煅烧,生成Cu、Fe2O3、FeO和SO2气体,实验后取d中溶液的1/10置于锥形瓶中,用0.05000mol·L-1标准碘溶液进行滴定,初读数为0.10 mL,末读数如右图所示。
(1)冶炼铜的反应为8CuFeS2 + 21O2  8Cu + 4FeO + 2Fe2O3 + 16SO2,若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号)。
8Cu + 4FeO + 2Fe2O3 + 16SO2,若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号)。
(2)装置a的作用是 。
| A.有利于空气中氧气充分反应 | B.除去空气中的水蒸气 |
| C.有利于气体混合 | D.有利于观察空气流速 |
(3)上述反应结束后,仍需通一段时间的空气,其目的是 。
(4)滴定时,标准碘溶液所耗体积为 mL。用化学方程式表示滴定的原理: 。
(5)通过计算可知,该黄铜矿的纯度为 。
铝是自然界中含量最高的金属元素,以铝土矿(主要成分为Al2O3,还含有Fe2O3)为原料通过以下途径制备氯化铝晶体和绿矾晶体:

(1)X是__________,操作I是_______。
(2)Z是_____,检验溶液E中含有金属阳离子的实验方法是_______________________。
(3)操作Ⅱ的主要实验步骤是边滴加____(填试剂名称)边蒸发浓缩、冷却结晶、过滤、洗涤。
(4)真空碳热还原—氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
2Al2O3(s)+2AlCl3(g)+6C(s)=6AlCl(g)+6CO(g) △H=a kJ·mol-1
3AlCl(g) =2Al(l)+AlCl3(g) △H=b kJ·mol-1
反应Al2O3(s)+3C(s)=2Al(l)+3CO(g)的△H= kJ·mol-1(用含a、b的代数式表示);
(5)铝电池性能优越,海洋灯塔电池是利用铝、石墨为电极材料,海水为电解质溶液,构成电池的其正极反应式为_______________________________;与铅蓄电池相比.释放相同电量时,所消耗金属电极材料的质量比m(Al):m(Pb)=____________。
(6)测定绿矾产品中Fe2+含量的实验步骤:
a.称取5.7g绿矾产品,溶解,在250mL容量瓶中定容;
b.量取25mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01mol•L-1KMnO4溶液滴定至终点,消耗KMnO4溶液体积为40mL(滴定时发生反应的离子方程式为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O)。
①计算上述产品中FeSO4•7H2O的质量分数为________;
②若用上述方法测定的产品中FeSO4•7H2O的质量分数偏低(测定过程中产生的误差可忽略),其可能原因有___________(只回答一条即可)。
高纯度的单质硅是信息产业的核心资源,没有硅就没有你喜欢的计算机。在地壳中含有大量的硅元素,含量仅次于氧,但自然界中没有游离的硅,硅元素全部是以化合态的形式存在的。工业上主要是利用碳与二氧化硅在高温下反应制备粗硅,某校化学兴趣小组对该反应中气体产物的成分进行探究。
(1)该兴趣小组对气体产物的成分提出如下假设,请你完成假设二和假设三:
假设一:气体产物只有CO;
假设二:____________________;
假设三:_____________________。
……
(2)为探究气体的成分,该兴趣小组设计了如下实验装置:

已知:PdCl2溶液可用于检验CO,反应的化学方程式为:CO+PdCl2+H2O=CO2+2HC1 +Pd↓(产生黑色金属钯粉末,使溶液变浑浊);
为避免空气中的氧气、二氧化碳、水蒸气对实验产生干扰,实验时要求通入足够长时间的氮气。
供选试剂:澄清石灰水、PdCl2溶液、浓硫酸、NaOH溶液。
①装置B的作用是______________;
②请你根据上述装置,设计实验验证假设一,写出实验步骤和结论(解答时要求指明C、D中所选试剂的名称):
| 实验步骤(不要求写出具体操作过程) |
实验预期现象和结论 |
| |
|
(3)有人认为,气体产物的成分与两种反应物的质量之比有关。为了探究炭粉不足时生成物中气体的成分,反应物中炭粉与二氧化硅的质量之比的最大比值是_________。
(4)资料表明,炭粉过量时会生成副产物SiC,若生成物中Si与SiC的物质的量之比为1:2(假定气体产物只有CO),写出该反应的化学方程式:________________________。
氨基甲酸铵是一种用途广泛的化工原料。有关它的资料如下:①常温下,在干燥的空气中稳定,遇水或潮湿空气则生成碳酸铵或碳酸氢铵;②熔点58℃,59℃则可分解成NH3和CO2气体;③在密封管内加热至120℃~140℃时失水生成尿素[CO(NH2)2];④酸性溶液中迅速分解;⑤合成氨基甲酸铵原理为:

(1)写出氨基甲酸铵在密封管内加热至1200C~1400C生成尿素的反应方程式:_______________
(2)滴液漏斗与容器A相连的导管的作用是 ,容器A内可用 (填药品名称)代替NaOH固体,仪器B名称________;盛放药品是:________。
(3)合成氨基甲酸铵的反应在一定条件下能自发进行,该反应的反应热ΔH_____0(填“>” “=”或“<”)(4)有同学建议该CO2发生装置直接改用“干冰”,你认为他的改进有何优点:(回答二点)
①________________;②________________
(5)该实验装置中有明显导致实验失败的隐患有:(指出主要二处)
①________________;②________________
用石灰石代替碱液处理酸性废水可降低成本。大多数情况下,利用石灰石处理含金属离子的酸性废水并不适用,原因在于酸与石灰石反应的限度,使溶液体系的pH不能达到6.0以上的排放标准。当酸性废水中含有Fe3+、Fe2+、Al3+时能利用石灰石处理该酸性废水,可使pH上升到6.0以上,达到满意效果,其研究步骤如下:
Ⅰ、向0.1mol/L 盐酸,加入石灰石粉,当溶液体系 pH 升至5.6 时, 再继续加入石灰石粉无气泡冒出,说明此时已达溶解平衡。
Ⅱ、向含Fe3+、Fe2+、Al3+的酸性废水中加入适量的0.1mol/L 盐酸和30% H2O2溶液,充分反应。
Ⅲ、将Ⅱ中获得的溶液加入到Ⅰ溶液中,得到混合液x,测得混合液pH<2.0。
Ⅳ、向混合液x中加入石灰石粉,有大量气体产生,并逐渐有沉淀生成。pH 升到 6.2时停止加石灰石粉。
(1)HCl的电子式是 。
(2)石灰石与盐酸反应的离子方程式是 。
(3)从化学平衡的角度分析CaCO3与盐酸反应的原理 (用化学用语表示)。
(4)CaCl2溶液显中性,步骤Ⅰ中溶液体系 pH = 5.6的原因是 。
(5)步骤Ⅱ中反应的离子方程式是 。
(6)已知:生成氢氧化物沉淀的pH
| |
Al(OH)3 |
Fe(OH)2 |
Fe(OH)3 |
| 开始沉淀时 |
3.4 |
6.3 |
1.5 |
| 完全沉淀时 |
4.7 |
8.3 |
2.8 |
注:金属离子的起始浓度为0.1mol/L
根据表中数据解释步骤Ⅱ的目的: 。
(7)步骤Ⅳ中,当 pH 上升到 3.3 以上时,会促进Al3+的水解,Al3+水解的离子方程式是 。
(8)步骤Ⅳ中溶液体系的 pH 可上升到6.2,是因为生成Al(OH)3可与溶液中的HCO3-反应使c(CO32-)增大,该反应的离子方程式是 。
运用化学反应原理知识在工业生产中有重要意义。
甲醇是一种可再生能源,具有广泛的开发和应用前景。如甲醇汽油是由10%一25%的甲醇与其他化工原料、添加剂合成的新型车用燃料,可达到国标汽油的性能和指标。
I、(一)甲醇在工业上可用CO和H2合成。
已知:CO(g)+1/2O2(g)=CO2(g) △H=—283 kJ·mol—1
CH3OH(l)+3/2O2(g)=CO2(g) +2H2O(l) △H=—725kJ·mol—1
(二)若要求得CO(g)+2H2(g)=CH3OH(l)的△H,还需要知道反应(用化学方程式表示) 的焓变。
工业上合成甲醇一般采用下列反应:CO(g)+2H2(g) CH3OH(g) △H=akJ/mol
CH3OH(g) △H=akJ/mol
下表是该反应在不同温度下的化学平衡常数(K):
| 温度/0C |
250 |
310 |
350 |
| K |
2.041 |
0.250 |
0.012 |
(1)由表中数据判断△H= a 0(填“>”、“=”或“<”)。
(2)某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)="0.5" mol·L-1,则此时的温度为 ℃。
(3)在容积固定的密闭容器中发生上述反应,各物质的浓度如下表:
| 浓度mol/L 时间/min |
c(CO) |
c(H2) |
c(CH3OH) |
| 0 |
0.8 |
1.6 |
0 |
| 2 |
0.6 |
1.2 |
0.2 |
| 4 |
0.3 |
0.6 |
0.5 |
| 6 |
0.3 |
0.6 |
0.5 |
①反应从0 min到4 min之间,H2的反应速率为 。
②反应达到平衡时CO的转化率为 。
③反应在第2 min时改变了反应条件,改变的条件可能是 (填序号)。
A.使用催化剂 B.降低温度 C.增加H2的浓度
(4)向容积相同、温度分别为T1和T2的两个密闭容器中均充入1 molCO和2 mol H2,发生反应CO(g)+2 H2(g) CH3 OH(g)△H="a" kJ/mol。恒温恒容下反应相同时间后,分别测得体系中CO的百分含量分别为w1和w2;已知T1<T2,则w1 w2(填序号)。
CH3 OH(g)△H="a" kJ/mol。恒温恒容下反应相同时间后,分别测得体系中CO的百分含量分别为w1和w2;已知T1<T2,则w1 w2(填序号)。
A.大于 B.小于 C.等于 D.以上都有可能
II、甲醇在化学电源方面也有着重要应用。写出以甲醇为燃料,氢氧化钠溶液为电解质溶液的原电池中负极的电极反应式: 。
【实验化学】
甲苯氧化法制备苯甲酸的反应原理如下:
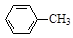 + 2KMnO4
+ 2KMnO4
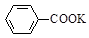 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O
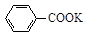 + HCl
+ HCl
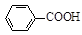 +KCl
+KCl
实验时将一定量的甲苯和KMnO4溶液置于图1装置中,在100 ℃时, 反应一段时间,再停止反应,并按如下流程分离出苯甲酸和回收未反应的甲苯。
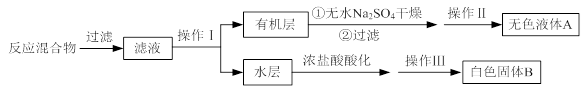
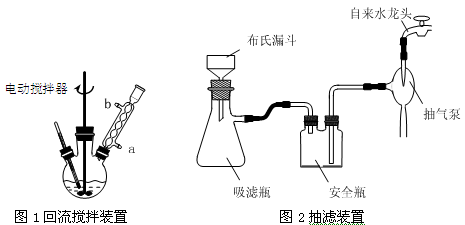
(1)实验室中实现操作Ⅰ所需的玻璃仪器有 、烧杯;操作Ⅱ的名称为 。
(2)如果滤液呈紫色,要先加亚硫酸氢钾,然后再加入浓盐酸酸化,若无此操作会出现的危害是 。
(3)在操作Ⅲ中,抽滤前需快速冷却溶液,其原因是 ;如图2所示抽滤完毕,应先断开 之间的橡皮管。
(4)纯度测定:称取1.220 g产品,配成100 mL溶液,取其中25.00 mL溶液,进行滴定 ,消耗KOH物质的量为2.4×10-3 mol。产品中苯甲酸质量分数为 。
(14分)天然气是重要的化石燃料和工业原料,其主要成分为甲烷。
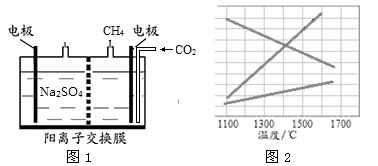
(1)CO2气体排放会产生温室效应,将通入CO2碳化了的水在如图1所示的电解池阴极区进行电解,可以直接产生甲烷,加入硫酸钠为了增加导电性。
①写出电解时阴极的电极反应式
②电解时电解池采用阳离子交换膜,若采用阴离子交换膜会对电解产生的影响为 。
(2)将甲烷和硫反应可以制备CS2,其流程如下:
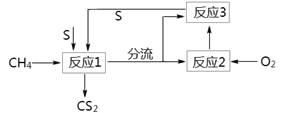
①反应1产生两种含硫的物质,则该反应方程式为
②反应当中,每有1molCS2生成时,需要消耗O2的物质的量为
③为了将含硫化合物充分回收,实验时需对反应1出来的气体分流,则进入反应2和反应3的气体气体关系为
(3)甲烷在高温下分解生成烃和氢气,若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图2所示,甲烷在高温下分解反应的化学方程式为 。
三氯化铁是合成草酸铁的重要原料。
(1)利用工业FeCl3制取纯净的草酸铁晶体[Fe2(C2O4)3·5H2O]的实验流程如下图所示:

①为抑制FeCl3水解,溶液X为 。
②上述流程中FeCl3能被异丙醚萃取,其原因是 ;检验萃取、分液后所得水层中是否含有Fe3+的方法是 。
③所得Fe2(C2O4)3·5H2O需用冰水洗涤,其目的是 。
④为测定所得草酸铁晶体的纯度,实验室称取a g样品,加硫酸酸化,用KMnO4标准溶液滴定生成的H2C2O4,KMnO4标准溶液应置于下图所示仪器 (填“甲”或“乙”)中。下列情况会造成实验测得Fe2(C2O4)3·5H2O含量偏低的是 。

a.盛放KMnO4的滴定管水洗后未用标准液润洗
b.滴定管滴定前尖嘴部分有气泡,滴定后消失
c.滴定前仰视读数,滴定后俯视读数
(2)某研究性学习小组欲从蚀刻镀铜电路板所得废液(溶质为FeCl2、CuCl2、FeCl3)出发,制备单质铜和无水FeCl3,再由FeCl3合成Fe2(C2O4)3·5H2O。请补充完整由蚀刻废液制备单质铜和无水FeCl3的实验步骤(可选用的试剂:铁粉、盐酸、NaOH溶液和H2O2溶液):向废液中加入足量铁粉,充分反应后过滤; ;调节溶液pH,将溶液蒸发浓缩、冷却结晶、过滤、洗涤干燥得FeCl3·6H2O; ,得到无水FeCl3。
试题篮
()