(4分)某趣味实验如图所示。向A中加入固体二氧化锰和过氧化氢溶液后,B中可观察到的现象是(1)___________________________,产生这种现象的原因是(2)________,用(3)_____________替代二氧化锰和过氧化氢也能产生同样现象。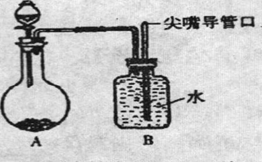
(2分)某工厂捧放的废液中含有少量硫酸和硫酸铜小军同学取适量废液放入盛有一定量锌粉的烧杯中,搅拌,待充分反应后过滤,得少量滤渣和滤液。请回答:
(1)若向滤渣中滴入稀硫酸有可燃性气体生成,则滤液中含有的溶质是_________
(2)若所得滤液的颜色为蓝色,则滤液中一定含有的溶质是_________
除去下列物质中所含杂质(括号内为杂质),所选用试剂及操作方法均正确的一组是( )
| 选项 |
待提纯的物质 |
选用的试剂 |
操作方法 |
| A |
Mn02(KCl ) |
水 |
溶解、过滤、结晶 |
| B |
CO2 (CO) |
氧气 |
点燃 |
| C |
Cu(CuO) |
稀盐酸 |
溶解、过滤、洗涤、干燥 |
| D |
CuSO4 (H2SO4 ) |
氢氧化钠溶液 |
过滤 |
下图是A、B两种固体物质(不含结晶水)的溶解度曲线.下列叙述错误的是( )
A.20℃时,A、B两种物质的溶解度都是40g
B.30℃时.在两种饱和溶液中.溶质的质量B一定大于A
c.30℃时,将B的饱和溶液降温至10℃,其溶质的质量分数减小
D.20℃时.等质量的A、B两种物质的饱和溶液中含溶质一样多
某化工厂用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%。为测定该产品中含碳酸钠的质量分数,进行了以下实验:取12g纯碱样品放入烧杯中,称得烧杯及纯碱样品的总质量为158g,再把100g稀盐酸平均分成四份,依次加入到样品中,每次均充分反应。实验数据记录如下:
| 所加盐酸的次数 |
第一次 |
第二次 |
第三次 |
第四次 |
| 盐酸的质量/g |
25 |
25 |
25 |
25 |
| 烧杯及所盛物质总质量/g |
181.2 |
204.4 |
228.6 |
253.6 |
请计算:(要求计算过程)
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量。
(2)该产品中碳酸钠的质量分数是否合格?
化学实验室有ABCDEF六瓶无色透明溶液,它们分别是碳酸钠、氢氧化钠、氢氧化钙、氯化钠、酚酞、盐酸中的一种。为了区别它们,化学小组同学分别进行下列实验(实验步骤略去):
A B C D E F
Ⅰ.将B分别滴入ACDEF中,A有气泡产生,E显红色,C产生白色沉淀,其余均无明显现象。
Ⅱ.将E分别滴入ABCDF中, BCD均显红色,
根据上述实验现象,完成下列填空:
(1)写出下列物质的化学式或名称:
B ,D ,E , F 。
(2)写出A与 C反应的化学方程式 ,
(3)当E滴入B中显红色后,再将A逐滴滴入混合液中,充分反应后的实验现象是 。
(4)假设所取六种无色溶液相互反应后的所得溶液的pH<7,则溶液中的溶质可能是 。
某校化学兴趣小组的同学对敞口放置的固体烧碱的变质程度开展了探究。
写出烧碱发生变质反应的化学方程式______________________________________。
为确定固体混合物中碳酸钠的质量分数,他们设计了如下几种不同的实验方案:
<方案一>气体分析法。
(1)若用图甲中的收集装置,则所测CO2气体的体积________(填“偏大”、“偏小”、“不变”),理由是 ,你的改进措施是 。
(2)若用乙装置测定CO2的质量(碱石灰是CaO和NaOH的混合物)。该实验设计中的缺陷是 (答一点即可)。
<方案二>沉淀分析法。
资料:部分碱和盐的溶解性表(20℃)
| |
OH– |
Cl- |
CO32- |
SO42- |
| Ca2+ |
微 |
溶 |
不 |
微 |
| Mg2+ |
不 |
溶 |
不 |
溶 |
| Fe3+ |
不 |
溶 |
— |
溶 |
| Cu2+ |
不 |
溶 |
不 |
溶 |

发生反应的化学方程式是 ,溶液M中的溶质是 。
A、B、C、D为初中化学常见的物质,它们之间存在一定的关系,请根据下列叙述回答问题。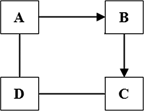
(1)若A为红色固体,C为难溶于水的白色固体,且D能转化为B,则A与D反应的化学方程式为 ,A→B的方程式为 。
(2)若A 为难溶于水的白色固体,且D能转化为B ,C与D反应有气体产生,则C的化学式为 ,D→B反应的化学方程式为 。
(3)若A在空气中易形成致密的氧化膜,且A能转化为C,B与D可相互反应,所有的反应均为置换反应,则B的化学式为 ,C与D反应的化学方程式为 。
) 金属材料在生产、生活中有着广泛的应用。
(1)下列应用中使用金属材料的有 (填字母)。
(2) 化学小组为了验证铁、铜、镁、汞的金属活动性顺序,设计了如下实验方案:
根据实验①判断出镁的金属活动性比铁强,依据的现象是 ;
根据实验②的现象得出的结论是 。
(3)化学小组收集到洗照片用过的硝酸银废液,利用废铁、废锌回收金属银。他们将金属混合物加入到硝酸银废液中,充分反应后过滤,得到固体和浅绿色溶液(忽略其他杂质),为了探究滤液中溶质的可能组成,他们做出以下猜想:
①溶质为硝酸锌 ②溶质为硝酸亚铁和硝酸银
③溶质为硝酸锌、硝酸亚铁 ④溶质为硝酸锌、硝酸亚铁、硝酸银
上述猜想中正确的是 。
(4)小组同学继续实验验证所得银粉固体中是否含有铁粉:
甲同学用简单的物理方法证明了固体中含有铁粉。他的方法是 ,
乙同学设计了如下测定固体中含银的质量分数的实验步骤:
A.取两药匙样品,加入过量稀硫酸;
B.待充分反应后,取出不溶物;
C.不溶物经洗涤、干燥后称量,记录其质量。
请回答:①步骤B中判断已充分反应的依据是 ,
②乙同学设计的实验方案能否达到实验目的,请说明理由 。
下图是常见固体物质的溶解度曲线,根据图示回答:
(1)曲线上M点表示 ,t3℃时,A、B、C三种物质的溶解度由大到小的顺序为 。
(2)t1℃时,将10g A物质放入100g水中,充分溶解后所得的溶液是 (填“饱和”或“不饱和”)溶液。欲使t2℃时C物质的饱和溶液变为不饱和溶液,可采取的方法是 (任填一种方法)。
(3)现有30℃的不饱和KNO3溶液,与该溶液有关的量有:①水的质量 ②溶液中KNO3的质量 ③KNO3的质量分数 ④30℃时KNO3的溶解度 ⑤溶液的质量
Ⅰ.在该不饱和溶液中加硝酸钾至饱和,不变的量有 (填序号,下同)。
Ⅱ.将该不饱和溶液恒温蒸发至饱和,不变的量有 。
锌粉、铝粉、镁粉的混合物3.8g与一定质量的稀硫酸恰好完全反应,将反应后的混合物蒸发水份得固体硫酸锌、硫酸铝、硫酸镁混合物11g,则反应中生成氢气的质量为( )
| A.0.15g | B.0.20g | C.0.30g | D.0.45g |
下列物质的鉴别方法中正确的是( )
| A.MnO2和木炭——观察颜色 |
| B.CO2和N2——燃着的木条分别伸入瓶中 |
| C.Ca(OH)2溶液和稀盐酸——取样,滴加碳酸钠溶液 |
| D.NaOH溶液和Na2CO3溶液——取样,滴加酚酞试液 |
下列四个图象分别表示对应的四种操作过程,其中表示正确的图象是( )
| A.加热高锰酸钾固体至质量不再减轻 |
| B.向pH=1的硫酸溶液中逐滴加入pH=13的氢氧化钠溶液 |
| C.某温度下,向一定量的水中持续加入食盐并不断搅拌 |
| D.等质量的锌、铁与足量的稀硫酸反应,产生氢气的质量M与反应时间t的关系图 |
只用水不能区分下列各组固体物质的是( )
| A.生石灰、氯化钠 | B.苏打、小苏打 |
| C.蔗糖、硝酸铵 | D.碳酸钙、氢氧化钠 |
家庭食用面碱(主要成分为Na2CO3)中往往混有少量NaCl。李童同学为测定食用面碱中碳酸钠的含量,设计并进行了以下实验:
①称取面碱样品3.4g于烧杯中,加入20mL水,搅拌至样品全部溶解;
②向其中加入足量的CaCl2溶液,至不再生成沉淀为止;
③过滤并将所得沉淀干燥后,称得质量为3.0g(不考虑操作中的质量损失)。
请计算:食用面碱中Na2CO3的质量分数是多少?(精确到0.1%)
试题篮
()