高温煅烧贝壳(主要成分是碳酸钙)可以生成氧化钙和二氧化碳,现有10t贝壳煅烧后质量减少了2.2t,可制得氧化钙的质量是多少?(假设其它成分不参加反应)
一定质量的NaOH溶液与8gSO 3恰好完全反应,得到Na 2SO 4溶液l000g,求所得硫酸钠溶液中溶质的质量分数(计算结果精确到0.01%)。(提示:2NaOH+SO 3═Na 2SO 4+H 2O)
将一定质量的NaHCO 3溶液与100g稀盐酸混合,二者恰好完全反应,溶液的总质量减少8.8g.求:稀盐酸中溶质的质量分数.
某品牌洁厕灵的成分是硫酸与盐酸的混合溶液,某课外活动小组想测定该品牌洁厕灵溶液中HCl的质量。取20g该品牌的洁厕灵溶液于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧杯中产生沉淀质量和烧杯中溶液pH值变化的部分数据如表所示:(已知BaCl 2溶液的pH=7)
|
滴加氢氧化钡溶液的质量/g |
5 |
10 |
25 |
30 |
|
烧杯中产生沉淀的质量/g |
1.165 |
2.33 |
4.66 |
4.66 |
求:
(1)完全反应后生成沉淀的质量为 ;
(2)计算该洁厕灵溶液中HCl的质量分数为多少?(计算结果保留至0.1%)

为测定21.2g某变质氢氧化钠固体中碳酸钠的含量,将其配置成500mL溶液,分别取出50mL用两种方法进行测定,已知:Na 2CO 3+BaCl 2═BaCO 3↓+2NaCl
|
加入的试剂 |
测得数据 |
|
|
方法1 |
足量BaCl 2溶液 |
BaCO 3沉淀1.97g |
|
方法2 |
足量稀硫酸 |
CO 2气体0.44g |
请任选1种方法的数据,计算该固体中碳酸钠的质量分数(写出计算过程及结果)
将氯化钠和氯化镁的固体混合物30g放入烧杯中,加入245.6g水使其完全溶解,再加入一定质量分数的氢氧化钠溶液,反应过程中滴加氢氧化钠溶液的质量与生成沉淀的质量关系如图所示。请计算:
(1)m的值为 ;
(2)恰好完全反应时,消耗氢氧化钠的质量 克;
(3)恰好完全反应时,所得不饱和溶液中溶质的质量分数(写出具体计算过程)。

学习小组测定某工业废水(含有H 2SO 4、HNO 3,不含固体杂质)中H 2SO 4的含量。取100g废水于烧杯中,加入100gBaCl 2溶液,恰好完全反应,经过滤得到176.7g溶液。
(可溶性杂质不参加反应,过滤后滤液的损失忽略不计)
(1)充分反应后生成沉淀的质量为 g;
(2)该工业度水中硫酸的质量分数为多少?(写出计算过程)
(3)为避免工业废水污染环境,排放前应对废水进行中和处理,需加入的物质是 。
在150g烧杯中加入100g过氧化氢溶液,再向其中加入2g二氧化锰。充分反应后,称得烧杯和剩余物质总质量为250.4g。请完成下列分析及计算:
(1)二氧化锰在反应中起 作用。
(2)计算过氧化氢溶液中溶质的质量分数。
某混合溶液含一定量的硝酸银、硝酸铜和硝酸钡,为逐一沉淀分离其中的金属元素,从稀盐酸、稀硫酸、氢氧化钠稀溶液、氯化钠溶液、硫酸钠溶液中选择试剂进行实验。
①甲的实验如下表所示:
|
步骤 |
操作 |
现象与解释 |
|
Ⅰ |
向混合溶液中加入过量稀盐酸,充分反应后过滤 |
得到白色沉淀,相应的化学方程式是 |
|
Ⅱ |
向Ⅰ中滤液加入过量稀硫酸,充分反应后过滤 |
得到 色沉淀 |
|
Ⅲ |
向Ⅱ中滤液加入过量氢氧化钠稀溶液,充分反应后过滤 |
得到蓝色沉淀,该沉淀的化学式是 |
在Ⅱ中,需确认钡元素是否完全沉淀。甲在此环节的部分实验记录如图所示:

请根据这部分记录,指出该环节中甲存在的具体问题并说明理由 。
②乙仅调整了甲实验中所加试剂的顺序,既达到了实验目的,理论上又减少了氢氧化钠的消耗量。乙所加试剂依次为 。
③丙设计了一种新的方案,不仅达到了实验目的,而且理论上氢氧化钠的消耗量减到最少。丙所加试剂依次为 。
在一次实验课上,同学们用加热氯酸钾和二氧化锰混合物的方法制取氧气.他们取了24.5g的混合物,其中二氧化锰的质量分数为20%,加热到完全分解.通过计算,得出他们制得氧气的质量是多少?
有关资料介绍,制取氧气有多种方法,其中氧化铜与氯酸钾混合加热,也能很快产生氧气。现将2.0g氧化铜与24.5g氯酸钾的混合物充分加热,残余固体经冷却、称量,质量变为16.9g。然后将固体溶于85.1g水中,充分搅拌,过滤,得到滤液和黑色的滤渣。滤渣又经洗涤、烘干、称量,质量为2.0g。
试回答:
(1)该反应中氧化铜起 作用。
(2)生成氧气的质量为 g。
(3)所得滤液中溶质质量分数为多少?
(4)向所得滤液中加入AgNO 3溶液至恰好完全反应,产生沉淀的质量为多少克?
氧气是人类生产活动的重要资源。
( 1 )下列属于 O 2 的化学性质的是 (填标号)。
| A. |
O 2能支持燃烧 |
| B. |
O 2的密度比空气的密度略大 |
| C. |
O 2在低温、高压时能变为液体或固体 |
( 2 )小圳同学进行实验室制备 O 2 的相关探究。
【 查阅 】 他得知在 KClO 3 分解制 O 2 的反应中, Fe 2 O 3 可作催化剂。
【 实验 】 他用电子秤称取 0.49g Fe 2 O 3 和一定量的 KClO 3 ,充分混合后加热至 KClO 3 完全分解,冷却至室温,称得剩余固体的质量为 1.98g 。
【计算】①剩余固体中KCl的质量是 g。
② 该反应生成 O 2 的质量(根据化学方程式写出完整的计算步骤)。
【 思考 】 他发现制备 O 2 较慢,猜测 KClO 3 和 Fe 2 O 3 的质量比可能会影响反应的快慢。
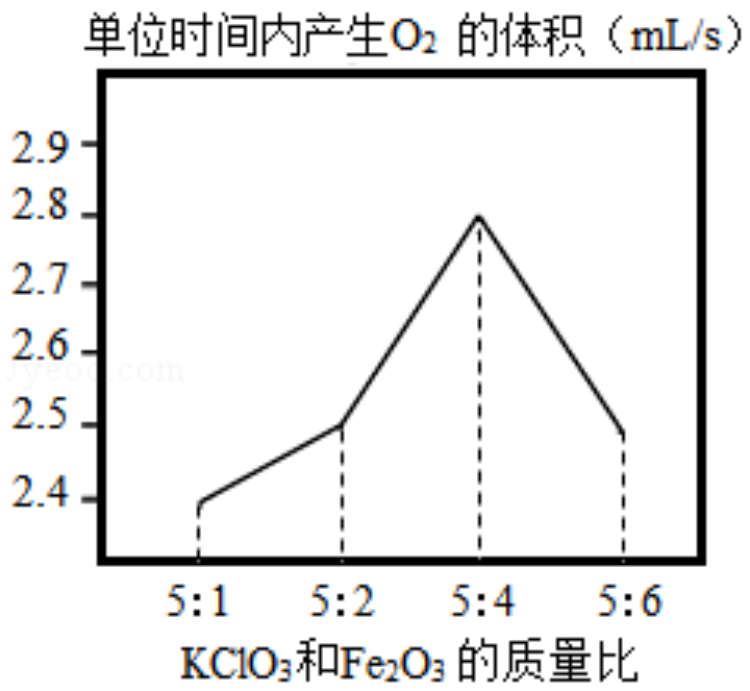
【 探究 】 ③ 他调节 KClO 3 和 Fe 2 O 3 的质量比制备 O 2 ,整理数据绘制出如图,从图中得出 KClO 3 和 Fe 2 O 3 最佳质量比是 。
【 结论 】 ④ 根据质量守恒定律,请你计算出小圳同学在 [ 实验 ] 中称取的 KClO 3 的质量为 g , KClO 3 和 Fe 2 O 3 的质量比是 (填最简比),不是最佳质量比。
某实验小组探究了溶质的质量分数对H 2O 2分解速率的影响。实验装置如图1所示,用注射器加入不同浓度的H 2O 2溶液(见下表),实验中使用传感器装置测算生成O 2的质量(圆底烧瓶内气压变化在安全范围),绘制氧气质量随时间变化的曲线,如图2所示。

| 实验编号 | H 2O 2的质量分数(%) | H 2O 2溶液的体积(mL) | 对应曲线 |
| Ⅰ | 3.4 | 10.0 | a |
| Ⅱ | 2.4 | 10.0 | b |
| Ⅲ | 1.7 | 10.0 | c(待绘制) |
(1)实验前需准备不同浓度的H 2O 2溶液,若要配制100.0g质量分数为2.4%的H 2O 2溶液,需质量分数为30%的H 2O 2溶液 g。
(2)根据实验探究目的,从曲线a、b中,可得出的结论是 。
(3)计算实验Ⅰ条件下H 2O 2完全分解所得氧气的质量,并写出具体计算过程(1.5﹣5.0% H2O2溶液的密度取值1.0g/mL)。
(4)在如图2中画出曲线c的大致位置及趋势。
化学中质量守恒定律是一个非常重要的定量定律.
(1)图1为托盘天平,使用托盘天平称物品的正确操作顺序为 (填序号).
①调游码 ②放称量纸 ③称量物放左盘
④调零点 ⑤加质量大的砝码 ⑥加质量小的砝码
A.①②③④⑤⑥ B.④②③⑤⑥① C.④⑤⑥①②③
(2)如图2装置中,称量小烧杯及其中所有物质的质量m1,然后将小烧杯中的碳酸钠与盐酸完全混合,反应停止后,再称量小烧杯及烧瓶内物质的总质量为m2,则m1 m2(填“=”“>”“<”),其原因是 .根据以上实验探究可知,若用碳酸粉末与盐酸反应验证质量守恒定律,可选择下图中 (少选错选不给分)
(3)请从原子的角度解释质量守恒定律 .
化学课后,化学兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,开展了以下探究:
【提出问题1】该氢氧化钠溶液是否变质了呢?
【实验探究1】
| 实验操作 |
实验现象 |
实验结论 |
| 取少量该溶液于试管中,向溶液中滴加 , 并不断振荡. |
有 产生. |
氢氧化钠溶液一定变质了. |
【提出问题2】该氢氧化钠溶液是全部变质还是部分变质呢?
【猜想与假设】
猜想1:氢氧化钠溶液部分变质.
猜想2:氢氧化钠溶液全部变质.
【查阅资料】
(1)氯化钙溶液呈中性.
(2)氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3=CaCO3↓+2NaCl
【实验探究2】
| 实验步骤 |
实验现象 |
实验结论 |
| (1)取少量该溶液于试管中,向溶液中滴加过量的 溶液,并不断振荡. |
有 生成. |
说明原溶液中一定有碳酸钠. |
| (2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液. |
溶液变红色. |
说明原溶液中一定有 . |
【实验结论】该氢氧化钠溶液 (填“部分”或“全部”)变质.
【反思与评价】
(1)氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式: .
(2)在上述[实验探究2]中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案 (填“可行”或“不可行”).
试题篮
()