下表是KNO3在不同温度下的溶解度(单位:g/100g水)。
| 温度/℃ |
0 |
20 |
40 |
60 |
80 |
100 |
| 溶解度 |
13.3 |
31.6 |
63.9 |
x |
169 |
246 |
(1)表中“63.9”的含义是: 。
(2)40℃时将31克KNO3固体放入50克水中,所得溶液为 溶液(填“饱和”或“不饱和”),若降温到20℃能析出固体 克。
(3)为测定x的值,取4份60℃的水各50克,分别进行实验,并记录数据如下表:
| 实验编号 |
实验1 |
实验2 |
实验3 |
实验4 |
| KNO3质量/g |
40 |
50 |
60 |
70 |
| H2O质量/g |
50 |
50 |
50 |
50 |
| 溶液质量/g |
90 |
100 |
105 |
105 |
① 实验2所得溶液的质量分数为 。
② 上述实验中溶液质量分数相等的实验是 。
③ 由实验可知,60℃时KNO3的溶解度为 。
(4)除去KNO3固体中混有的少量NaCl,提纯的步骤是: 溶解、蒸发浓缩、 ,然后过滤、洗涤、干燥。
图一是甲、乙两种固体物质的溶解度曲线图。现将两支分别装有甲、乙两物质饱和溶液的试管(底部均有少量未溶解的固体)浸入盛有水的烧杯中,再向烧杯中加入一定量浓硫酸。请根据图一回答问题:
① 50℃时,甲物质的溶解度是 ⒂ 。
② 烧杯中加入浓硫酸后,甲、乙两试管中看到的现象是 ⒃ ;除了加浓硫酸外,还可以加 ⒄ 物质,也会发生这样的变化。
③ 图二中,20℃时将20gA物质放入50g水中,所得溶液的质量分数是 ⒅ 。(精确到0.1)
④ 图二中,40℃时将A、B、C物质的饱和溶液各100g降温至20℃,所得溶液的质量分数的关系是 ⒆ (填“﹥”、“﹦”或“﹤”)。
⑤ 图二中,20℃时,A、B、C三物质的溶解度相等,有关这三种物质饱和溶液的性质描述一定正确的是 ⒇ 。(选填编号)
Ⅰ.溶液质量一定相等 Ⅱ.溶质质量一定相等
Ⅲ.溶液的质量分数一定相等 Ⅳ.溶液的密度一定相等
海洋是地球上最大的储水库,蕴含着丰富的化学资源。海水晒盐能够得到粗盐和卤水。
①卤水中含有MgCl2、KCl和MgSO4等物质,下图是三种物质的溶解度曲线。t2℃时,三种物质的饱和溶液中,溶质质量分数最小的是 。
②将t2℃时三种物质的饱和溶液加热到t3℃以上时,
仍然为饱和溶液的是 。
③将饱和氯化镁溶液由t3℃冷却至t1℃,下列四种叙述中,
正确的是 (填序号)。
| Ⅰ.溶液的质量不变 |
Ⅱ.氯化镁的溶解度变小 |
| Ⅲ.溶液中溶质质量不变 |
Ⅳ.溶液中溶质质量分数变小 |
④在t3℃时,60克KCl的饱和溶液与60克MgCl2的饱和溶液中,溶质MgCl2与KCl的质量比为3∶1,则t3℃时MgCl2的溶解度为 。
如图是甲、乙两种物质的溶解度曲线,请结合图回答问题:
(1) ℃时,甲、乙两种物质的溶解度相等。
(2)t2℃时,分别将甲、乙两种物质的饱和溶液降温到t1℃,溶液的溶质质量分数甲 (填“>”、“=”或“<”)乙。
(3)小明同学用甲物质进行以下实验.
①实验过程中,B、C、D对应的溶液为不饱和溶液的是 。
②小华同学将小明同学实验中的水改为酒精,发现固体没有溶解,综合两位同学的实验,可得出结论:影响甲物质溶解度的因素有 .
③向B对应的溶液中再加入20g甲固体的过程中,发现固体全部溶解,一段时间后又有部分固体析出。你认为“全部溶解”的原因是 。
KNO3和KCl在不同温度时的溶解度如下表所示。请回答下列问题:
| 温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
|
| 溶解度/g |
KNO3 |
13.3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
138 |
| KCl |
27.6 |
31.0 |
34.0 |
37.0 |
40.0 |
42.6 |
45.5 |
48.3 |

(1)依据上表数据,绘制KNO3和KCl的溶解度曲线,上图中能表示KNO3溶解度曲线的是 ① 。(填m或n)
(2)由表中数据分析可知, KNO3和KCl在某一温度时具有相同的溶解度x,则x的值是 ① 。
(3)如下图所示,20℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是下列中的___①_____(填字母序号)。
A.氢氧化钠固体 B.生石灰固体 C.冰块 D.硝酸铵固体 E.浓硫酸
(1)下列是初中化学中的一些重要实验。请回答: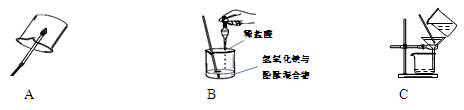
①A是氢气或甲烷的燃烧实验,点燃前必须 ;
②B实验中能够说明盐酸与氢氧化钠发生了反应的现象是 ;
③C是除去粗盐中难溶性杂质实验中的过滤操作,过滤后发现滤液仍然浑浊,其可能的原因是 (答出一种原因即可)。
(2) 如图所示是A、B、C三种物质的溶解度曲线,据此图回答: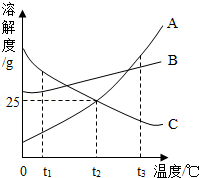
①t1℃时,A、B、C三种物质的溶解度由大到小的顺序是 ;
②t2℃时,将30gA放入100g水中,充分搅拌后,所得溶液的溶质质量分数是 ;
③t3℃时,将等质量A、B两种物质的饱和溶液降温到t2℃时,析出晶体质量较大的是 ;
④t3℃时,将25gC放入100g水中,充分搅拌后得到C的饱和溶液,在不改变溶剂量的前提下,将其变为不饱和溶液的方法是 .
20℃时,将等质量的甲、乙固体(不含结晶水),分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2(不考虑水分蒸发),甲、乙固体的溶解度曲线如图3.
下列说法正确的是( )
| A.图1中乙溶液一定不饱和 | B.图2中两溶液中溶质质量分数一定相等 |
| C.图3中N表示甲的溶解度曲线 | D.图2中两溶液降温至30℃一定都不会析出晶体 |
根据A物质和B物质的溶解度曲线,回答下列问题:
(1)20℃时,将35g A物质和35g B物质分别放入盛有100g水的烧杯中,充分搅拌,溶液达到饱和的是 (填“A”或“B”)。
(2)溶解度曲线A与B的交点P的含义是 。
(3)C物质的溶解度如下表,请在上图中描出C物质的溶解度曲线。
| 温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
| 溶解度/g |
40 |
33 |
27 |
23 |
18 |
14 |
10 |
水和溶液在生命活动和生产、生活中起着十分重要的作用。
(1)自来水厂对天然水进行净化的过程中,通常不采用 (填字母序号)。
| A.过滤 | B.吸附 | C.电解 | D.消毒 |
(2)水常用来配制各种溶液,硝酸钾溶液中的溶质为 。
(3)某同学进行以下实验:在甲乙烧杯中分别放入40g硝酸钾固体,
再分别加入100g冷水和热水,充分搅拌后(保持各自的温度不变),
结果如图所示。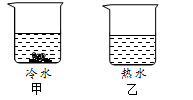
①甲烧杯中溶液是 (填“饱和”或“不饱和”)溶液。
②将乙烧杯中的溶液降温到t1℃时,溶液恰好达到饱和状态,则t1℃时,硝酸钾
的溶解度是 g。
(4)已知:甲物质在20℃和40℃时的溶解度分别为30g和50g。下列有关甲物质的实验中说法正确的是 (填字母序号)。
a.只有A是不饱和溶液 b.B和E中溶质的质量分数相等
c.D中溶质的质量分数最大 d.将E再升温至 40℃时,会析出20g固体
下表是KNO3 、NaCl在不同温度下的溶解度:
| 温度(℃) |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
100 |
|
| 溶解度/g |
KNO3 |
13.3 |
20.9 |
32 |
45.8 |
64 |
85.5 |
110 |
138 |
169 |
202 |
246 |
| NaCl |
35.7 |
35.8 |
36 |
36.3 |
36.6 |
37 |
37.3 |
37.8 |
38.4 |
39 |
39.8 |
(1)将20℃时相同质量的KNO3 、NaCl饱和溶液冷却至0℃,析出晶体多的是 。
(2) 60℃时,将50g硝酸钾固体投入50g水中,充分溶解后可得到硝酸钾 溶液(填“不饱和”或“饱和”或“不能确定”)。将温度降到20℃,计算溶液中溶质的质量分数 (精确到0.1%)。
(3)将20℃时KNO3和NaCl的饱和溶液同时升高一定温度后,所得溶液中溶质的质量分数的大小关系是:硝酸钾 氯化钠(填“>”或“<”或“=”)。
甲、乙两种固体物质的溶解度曲线如图Ⅰ所示。常温下,分别向装有适量甲、乙物质的两支试管里加入等量的蒸馏水,充分振荡后,两支试管底部均有未溶解的固体;再将两支试管放入盛有冰水混合物的烧杯里,如图Ⅱ所示。
(1)t1℃时,乙物质的饱和溶液的溶质质量分数 25%(填“>”、“<”、“=”之一)。
(2)t2℃时,甲物质的溶解度 乙物质的溶解度(填“>”、“<”、“=”之一)。
(3)若甲中含有少量的杂质乙,可采用 方法提纯甲。(填“蒸发结晶”、“降温结晶”之一)
(4)在图Ⅱ实验中看到的实验现象是甲试管中固体增多,乙两试管里固体减少。请你对此现象作出解释。 。
下图为甲、乙两种固体物质的溶解度曲线。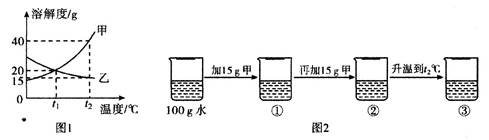
⑴溶解度随温度升高而增大的物质是 (填“甲”或“乙”);
⑵某同学在t1℃时进行如图2实验,充分搅拌得到相应的液体①一③。①一③形成的溶液中属于饱和溶液的是 (填序号);
⑶在溶液③中再加入25g甲,充分搅拌,所得溶液中溶质的质量分数为 (精确到0.1%)。
⑷若固体甲中含少量固体乙,在提纯固体甲时一定要用到的玻璃仪器有 ;
⑸若甲为KNO3,如图3所示,20℃时,将盛有饱和KNO3溶液
的小试管放入盛水的烧杯中,向烧杯中加入某物质后,试管中
有晶体析出。加入的物质可能是下列中的 (填字母序号)。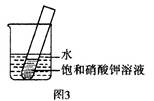
A氢氧化钠固体 B生石灰固体 C冰块
D硝酸铵固体 E.浓硫酸
(8分)(1)下图是A、B、C三种固体物质的溶解度曲线。
①t1℃时,三种物质溶解度的大小关系是 ;
②t2℃时,将30gB固体投入100g水中,充分溶解后可得到的是 溶液(填“不饱和”、“饱和”或“不能确定”)。
③将饱和A溶液变为不饱和溶液,可行的方法之一是升温,还可以用的方法是 。
④A中含少量C,若要提纯A,可采用 结晶的方法。
(2) 生活与化学息息相关。
①下列食物中,能提供大量蛋白质的是 (填字母序号)。
A.牛奶 B.大米 C.蔬菜
②加钙牛奶中的“钙”是指 (填“分子”、“原子”、“离子”或“元素”)。
③下列物品中,所使用的主要材料属于天然纤维的是 (填字母序号)。
A. 橡胶手套 B.棉布围裙 C.塑料保鲜膜
④我们常用洗涤剂清洗餐具上的油污,这是因为洗涤剂具有 功能。
认真分析下列各图,回答相关问题:


图1 图2 图3
(1)根据图1分析,20℃时,将20g NaCl加入50g水中形成溶液的质量为____________。
(2)图2中打开汽水瓶冒出大量气泡,说明气体的溶解度与____________有关。
(3)在图3所示的烧杯中加入一定量的硝酸铵,溶解后甲试管内出现的现象是______________;乙试管内的溶液是____________(填“饱和”或“不饱和”)溶液。
2014年3月22日是第22届“世界水日”,请你根据所学,回答下列问题。
(1)下图是简易净水装置。该净水装置 (填“能”或“不能”)将河水变成纯水。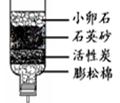
(2)二氧化氯(ClO2)是新一代饮用水的消毒剂,工业上将氯气(Cl2)通入亚氯酸钠(NaClO2)溶液中反应来制取二氧化氯,同时生成氯化钠。写出该反应的化学方程式: 。
(3)小丽收集到一瓶浑浊的河水,她要模拟自来水厂的净水过程,最终制成蒸馏水,
过程如下图所示。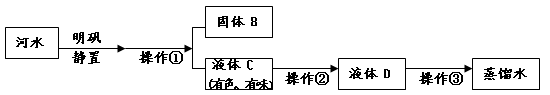
操作①的名称是 ;操作②应选用的装置是下图中的 (填序号,下同);操作③应选用的装置是下图中的 。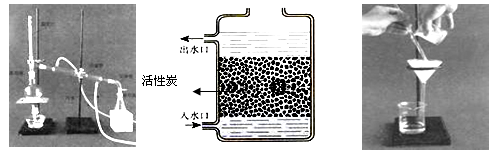
(Ⅰ) (Ⅱ) (Ⅲ)
(4)小丽取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多浮渣产生,说明液体D是 水。(填“硬”或“软”)
(5)如图是甲、乙两种物质的溶解度曲线,回答下列问题: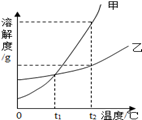
①________℃时,甲、乙两种物质的溶解度相等;
②若固体甲中含有少量乙时可用_____________方法提纯甲(填”蒸发结晶“或”冷却结晶“);
③t2℃用等质量的甲、乙两种物质配制甲、乙的饱和溶液需要水的质量:
甲______乙(填“>”“<”或“=”);
④实验室需要配制50g溶质质量分数为4%的氢氧化钠溶液,所需固体氢氧化钠的质量为___ __g,主要操作步骤是:计算、_______、量取、溶解.在溶解过程中用玻璃棒搅拌,其作用是______ ___.
试题篮
()