(8分)溶液在生产和科研中具有广泛的用途,与人们的生活密不可分。
(1)厨房中的下列物质加入水中,能形成溶液的有 (填编号);
a.面粉 b.食盐 c.白糖 d.牛奶
(2)下图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线。
①t2℃时,甲的溶解度 (填“>”、“<”或“=”)乙的溶解度;
②t1℃时,将50克的甲加入到100克的水中,充分搅拌后所得溶液的质量为 克;
③将t1℃时甲的饱和溶液升高温度到t2℃(假设水分没有蒸发),则与原溶液相比,所得溶液中溶质的质量分数将 (填“变大”、“变小”或“不变”);
④将t2℃时,甲、乙两种物质相同质量的饱和溶液,分别冷却到t1℃,析出晶体最多的是 物质。
(3)气体的溶解度也有一定的变化规律。
①打开可乐瓶,逸出大量气泡。由此可见,压强越小,CO2的溶解度越 。为增大CO2的溶解度,可采用的一种方法是 。
②不同温度下,氧气的溶解度随压强的变化如图所示,
图中t1对应的温度为40℃,则t2对应的温度 (填编号)。
a.大于40℃ b.小于40℃ c.无法确定
水和溶液在生命活动和生活中起着十分重要的作用。根据下面的溶解度表与溶解度曲线,回答下列问题:
(1)A是__________的溶解度曲线。
(2)80℃时,100g水中加入120g硝酸钾,所得溶液是__________(填“饱和”或“不饱和”),当80℃的该溶液降温到20℃时,析出晶体的质量为__________g。
(3)硝酸钾中混有少量的氯化钠,想要得到纯净的硝酸钾的方法是__________。
(4)60℃时,向两个分别盛有50g NaCl和KNO3的烧杯中,各加入100g的水,充分溶解后成为饱和溶液的是__________溶液;将上述烧杯中剩余固体全部溶解,变为不饱和溶液,下列方法能实现的是__________(填字母序号)。
| A.升温 |
| B.加入该溶质 |
| C.加入适量水 |
| D.降温 |
E.加入足量该溶质的不饱和溶液
(5)如下图所示,烧杯A中是饱和的氢氧化钙溶液,向烧杯B中加入生石灰后,烧杯A中变浑浊,原因是____________________________________。
A图为实验示意图,在室温情况下,烧杯中盛装的是甲物质的溶液,试管①中盛装的是乙物质的溶液,试管②中盛装的是丙物质的溶液。当它们由室温升到80℃时,发现烧杯中甲物质没有明显变化,而试管①中盛装的是乙物质全部溶解,试管②中有丙物质析出。B图表示三种物质的溶解度曲线。请你据此现象回答下列有关问题:
(1)室温时, (选填“烧杯”、“试管①”或“试管②”)中 溶液可能是不饱和溶液;
(2)上图能表示甲物质的溶解度曲线的是 (选填a、b或c);
(3)若乙物质溶液中混有少量的甲物质,提纯乙物质可采取的方法是
(4)对于甲、乙两物质饱和溶液,在温度 时,乙物质的溶质质量分数一定比甲物大.
(4分)如图是A、B两种固体物质的溶解度曲线.回答:
(1) 要使接近饱和的A溶液变为饱和溶液,可采取的方法是 ;
(2) 在40℃时,等质量的A、B物质的饱和溶液降温到30℃时溶液质量的关系A B(选填“大于”、“小于”或“等于”);
(3) 30℃时,130gA的饱和溶液,升温到40℃时,需加入A物质的质量为 g才能变成饱和溶液。
(4) 当A中混有少量B时,用__________方法可以得到固体A。
(.4分)、下图是三种固体物质的溶解度曲线。
(1)物质c的溶解度随温度的升高而 ;
(2)将t1℃时a、b、c三种物质的饱和溶液升温至t2℃(溶剂量不变),溶液中溶质质量分数不变的是 。
(3) 将t2℃时a、b、c三种物质的饱和溶液降温至t1℃,析出晶体最多的是 ;
(4)若b为氯化钠,那么从它的饱和溶液中获得较多的氯化钠晶体,应采取 方法。
下图是A、B两种物质的溶解度曲线。 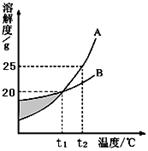
(1)图中阴影部分表示的B溶液为 (填“饱和”或“不饱和”)溶液。
(2)在t2℃时,将等质量的A、B物质配制成饱和溶液,所得溶液
质量较大的是 。
(3)将t2℃时100gA的饱和溶液稀释成10%,需要加水 g。
两种固体物质的溶解度曲线如图所示。

请回答问题:
(1)
时,
物质的溶解度
物质的溶解度;(填">""<"或"=")
(2)将
物质的不饱和溶液变成饱和溶液的方法有;(填一种即可)
(3)
时,将50
物质加入100
水中,充分溶解后,形成溶液的质量为
。
自来水生产中通常用适量的氯气杀菌消毒,以食盐(NaCl)为原料制取氯气的流程如下图所示,根据题意填写下列空白:
(1)上述过程中的涉及的物质属于碱的是__________(写化学式)。
(2)过程②发生反应的化学方程式为
2NaCl+2X通电 2NaOH+H2↑+Cl2↑,其中X的化学式为_________,
在反应前后Cl元素的化合价分别为_______________。
(3)氯化钠和氢氧化钠溶解度曲线如图所示,温度为t2时,过程①要将36g氯化钠配制成饱和溶液,需要水的质量为_____g;过程③要得到氢氧化钠固体所采取的结晶方法为 ____________。
根据下列数型图像回答:

(1)图一是用盐酸和氢氧化钠进行中和反应时,反应过程中溶液的pH变化曲线。向盐酸中加入的氢氧化钠溶液质量为mg时,所得溶液中含有的离子为(填离子符号)
(2)图二是20℃时,取10mL10%的NaOH溶液于烧杯中,逐滴加入10%的盐酸,随着盐酸的加入,烧杯中溶液温度与加入盐酸体积的变化关系
①由图可知中和反应是放热反应,你的依据为②甲同学用氢氧化钠固体与稀盐酸反应也能得到相同结论,乙同学认为不严密,因为
(3)图三是a、d、c三种物质的溶解度曲线。a与c的溶解度相交于P点,据图回答:
①t1℃时,接近饱和的c物质溶液,在不改变溶液质量的条件下,可用的方法达到饱和状态
②将t2℃时,150g a物质的饱和溶液降温到t1℃时。可以析出g a物质。
(4)下图托盘天平两边是等质量的铁和镁分别跟等质量等浓度的稀硫酸反应,反应时间t与生成氢气质量m的变化关系如图四。

试回答:从开始反应到不再产生气体为止,天平指针偏转情况是
和
在不同温度时的溶解度如下表所示。请回答下列问题:
| 温度/ | 0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
|
| 溶解度/ | 13.3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
138 |
|
| 35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
37.8 |
(1)依据上表数据,绘制出
和
的溶解度曲线如图所示:
图中能表示
溶解度曲线的是(填"
"或"
")

(2)由表中数据分析可知,
和
在某一温度时具有相同的溶解度,则温度的范围是;
(3)某兴趣小组做了一下实验:

上述实验过程中得到的溶液一定属于不饱和溶液的是(填数字序号),将⑤继续冷却至10
,过滤,共可回收得到
固体
;
(4)硝酸钾中含有少量氯化钠时,可通过(填"蒸发结晶"或"降温结晶")的方法提纯。
、
两固体物质的溶解度曲线如图所示:

(1)在℃时,
和
的溶解度大小相等。
(2)要将30℃时
物质的不饱和溶液变成该温度下的饱和溶液,可以采取的措施是(答一条即可)。
(3)将30℃时
、
两物质的饱和溶液的温度降到10℃,此时,
、
两种溶液溶质质量分数的大小关系是。
如图所示为①硝酸钾、 ②氯化钠 、③硼酸
(
)的溶解度曲线图。由图可知:

(1)当温度为25℃时,硝酸钾、氯化钠和硼酸三种物质
的溶解度大小关系为(请用序号作答)。
(2)图中P点表示硝酸钾的(填"饱和"或"不饱和")溶液。
(3)从图中可得到的有关硼酸溶解度的信息有:硼酸的溶
解度随着温度的升高逐渐增大、(任写一条)等。
0℃时,分别向盛有10g水的A、B两支试管中加入等质量的甲、乙两种固体,充分溶解后,观察到如图1所示的现象.图2表示的甲乙两种物质的溶解度曲线.
(1)20℃时,(填"A"或"B")试管中的溶液一定是饱和溶液;
(2)图2中(填"M"或"N"),表示乙物质的溶解度曲线
(3)要使B试管中剩余的固体继续溶解可采用的方法是(答一种方法即可).
(4)将10℃时M的饱和溶液升温到20℃(假设水不蒸发),其溶质质量分数(填"增大"、"减小"或"不变").

粗盐中除
外还含有
以及泥沙等杂质。初步提纯粗盐的实验流程如下:

(1)"滤渣"是粗盐中含有的。
(2)实验过程中四次用到玻璃棒,分别是:
第一次:溶解时搅拌;
第二次:;
第三次:;
第四次:将精盐从蒸发皿转移出来。
(3)本实验从滤液得到精盐,采用的是蒸发溶剂的方法而不用降低溶液温度的方法,参考溶解度曲线图分析的原因:.

(4)看图可知,200C时
的溶解度为g,本实验溶解3.6g的粗盐,蒸馏水的最佳使用量约为ml.增加蒸馏水的用量虽然能加快粗盐的溶解,但会引起的不良后果是。
试题篮
()