下列除去杂质所选择牟试剂错误的是:()
| 选项 |
物质 |
杂质 |
所选试剂 |
| A |
|
水蒸气 |
浓硫酸 |
| B |
溶液 |
盐酸 |
|
| C |
稀盐酸 |
||
| D |
溶液 |
溶液 |
溶液 |
如图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论正确的是()

| A. | 反应后溶液的pH大于7 |
| B. | 反应前的溶液均可导电,反应后的溶液不导电 |
| C. | 反应后溶液中存在的粒子只有 和 |
| D. | 反应前后所有元素的化合价均无变化 |
现有氧化铁.稀硫酸.氢氧化钠溶液.氯化钡溶液和碳酸钾溶液五种物质,在常温下它们两两相互发生的化学反应有()
| A. | 4个 | B. | 5个 | C. | 6个 | D. | 7个 |
下列装置或操作能达到实验目的的是

A B C D
| A. | 稀释浓硫酸 |
| B. | 探究燃烧的三个条件 |
| C. | 测定空气中氧气的含量 |
| D. | 探究 的性质 |
某工厂排放的废液中含有少量硫酸和硫酸铜。小军同学取适量废液放入盛有一定量锌粉的烧杯中,搅拌,待充分反应后过滤,得少量滤渣和滤液。关于该实验,下列说法正确的是()
| A. | 反应前后液体的酸性减弱, 变小 |
| B. | 实验所得滤液是纯水,可直接排放 |
| C. | 滤渣中一定含铜和锌 |
| D. | 发生的反应都是置换反应 |
甲、乙两种固体物质(不含结晶水)的溶解度曲线如下图所示。下列说法正确的是()

| A. | 甲物质的溶解度大于乙物质的溶解度 |
| B. | ℃时,甲、乙两物质的溶解度相等,均为40g |
| C. | ℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数 |
| D. | 甲的溶解度受温度影响较小 |
把金属 放入 溶液中, 表面有红色固体析出;若放入 溶液中,无明显现象。则 、 、 三种金属活动性由强到弱的顺序正确的是 ( )
| A. | 、 、 | B. | 、 、 |
| C. | 、 、 | D. | 、 、 |
甲、乙两种固体物质(不含结晶水)的溶解度曲线如下图所示。下列说法正确的是 ( )

| A.甲物质的溶解度大于乙物质的溶解度 |
| B.t1℃时,甲、乙两物质的溶解度相等,均为40g |
| C.t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数 |
| D.甲的溶解度受温度影响较小 |
把金属X放入Cu(NO3)2溶液中,X表面有红色固体析出;若放入Mg(NO3)2溶液中,无明显现象。则X、Cu、Mg三种金属活动性由强到弱的顺序正确的是 ( )
| A.Mg、X、Cu | B.X、Mg、Cu |
| C.Mg、Cu、X | D.Cu、X、Mg |
甲、乙、丙、丁四种金属。甲即使在高温时也不与氧气反应。乙、丙、丁在一定条件下都能与氧气反应。丁盐的水溶液可用丙制的容器盛放,但不能用乙制的容器盛放。这四种金属的活动性由强到弱的顺序是()
| A. | 甲>乙>丁>丙 |
| B. | 丙>丁>乙>甲 |
| C. | 丙>乙>丁>甲 |
| D. | 乙>丁>丙>甲 |
为了探究影响锌与盐酸反应剧烈程度的因素,某学习小组设计了下列实验
下列说法正确的是( )
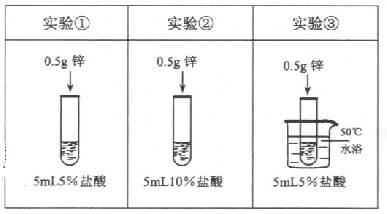
| A. | 对比实验①和②,可研究盐酸的浓度对反应剧烈程度的影响 |
| B. | 对比实验②和③,可研究盐酸的浓度对反应剧烈程度的影响 |
| C. | 对比实验②和③,可研究温度对反应剧烈程度的影响 |
| D. | 对比实验①和②,可研究温度对反应剧烈程度的影响 |
在氯化铜溶液中加入一定量的锌和铁,充分反应后得到一些固体。过滤,向固体中加入少量稀盐酸,有气体放出,则下列叙述中正确的有:
①固体中一定含有锌 ②固体中一定没有铜 ③固体中一定含有铁
④溶质中一定含有氯化锌⑤溶质中一定没有氯化亚铁⑥溶质中肯定没有氯化铜
| A.①③④⑤ | B.②④⑥ | C.③④⑥ | D.③⑤⑥ |
在一密闭容器内有A、B、C、D四种物质,在一定条件下发生化学反应,一段时间后,测得反应前后各物质的质量如下表,则下列说法中正确的是
| 物 质 |
A |
B |
C |
D |
| 反应前物质质量(g) |
10 |
90 |
8 |
2 |
| 反应后物质质量(g) |
38 |
56 |
14 |
X |
A. 根据质量守恒定律,X的值为0
B. 该反应是分解反应
C. 该反应是复分解反应
D. 在这个反应中A、B、C之间的质量比为38∶56∶14
25℃时向一定量不饱和
溶液中逐渐加入
固体,则下列图像中能正确表示此过程溶质质量变化规律的是
| A. |
|
B. |
|
C. |
|
D. |
|
试题篮
()