(1)六盘水市四创主题之一是"创建生活宜居城市",下列符合该主题的是
A.植树造林、美化环境 B.为解决白色污染,将塑料收回利用 C.鼓励使用太阳能热水器
(2)先进的交通工具可以使出行更便捷,沪昆高铁是国家铁路交通额重要组成部分,预计2016年年底建成通车,六盘水市将步入"高铁时代".列出制造离不开下列材料:A.金属材料 B.合成材料 C.复合材料
根据要求选择填空(填序号):
①列车制造中需要大量的钢铁,钢铁属于 .
②高铁座椅需用到耐磨、耐腐蚀的涤纶等材料,涤纶属于 .
(3)水是生命之源,万物之基,是人类宝贵的自然资源,我们每个人都要珍惜水、爱护水、节约用水,请举一例说明生活中你是如何节约用水的: .
金属在生活和生产中有着非常广泛的应用。金属材料已经成为社会发展的重要物质基础,研究其性质十分必要。
(1)海水中含量最多的金属元素是 (填写元素符号)。
(2)人们对金属铝的研究和利用比铜和铁晚,金属大规模开发和利用的先后顺序与金属的 有关。某同学为了验证锌、银、铜三种金属的活动性顺序。设计了五个实验:
①将锌片、铜丝分别放入稀盐酸中;②将银丝放入硝酸铜溶液中;③将铜丝放入硝酸银溶液中;④将铜丝放入硫酸锌溶液中;⑤将锌片放入硝酸银溶液中,下列实验组合能够验证锌、银、铜三种金属活动性顺序的是 (填写字母)。
A.①②B.①③C.②④D.①⑤
(3)我国古代就发明了湿法冶金技术。请你写出用铁和氯化铜为原料进行湿法炼铜的化学方程式 。
某同学设计了如图A﹣F气体制取与性质的组合装置,打开活塞K,很快看到F装置中蜡烛由下至上依次熄灭.请根据如图回答问题.

(1)仪器①的名称为: .
(2)小华用G装置加热高锰酸钾制取氧气时,发现试管位置过高,他调节试管过度需要操作的旋钮是 .
(3)利用A装置制取气体的优点: ;A装置中发生的化学反应方程式为: .
(4)B装置中观察到的现象为 .
(5)D装置中发生的化学反应方程式为: .
(6)E装置中观察到石蕊试液变红,用化学方程式解释产生该现象的原因 .
(7)F装置中蜡烛熄灭的原因是 .
有一包白色固体样品,可能含碳酸钠、硫酸钠、氯化钠、氢氧化钠中的一种或几种。小科同学为探究其成分做了以下试验:
Ⅰ.取少量固体样品于烧杯中,先加足量水溶解,再加入足量的BaCl2溶液,有白色沉淀产生;
Ⅱ.继续向烧杯中滴加稀盐酸并不断搅拌,烧杯内固体质量随加入稀盐酸质量的变化如图所示。
请回答下列问题:
(1)AB段观察到的现象是
(2)C点时,溶液中一定含有的溶质是 。

根据如图回答问题:

(1)装置中标"a"的仪器名称是 ;
(2)实验室制备、收集二氧化碳选用的装置为 (填序号);
(3)实验室用高锰酸钾制取氧气的化学方程式为 .
实验室有一瓶敞口放置的过氧化钠(Na 2O 2)固体,同学们想利用这瓶过氧化钠是否变质,进行如下实验探究:
【查阅资料】2Na 2O 2+2CO 2═2Na 2CO 3+O 2,2Na 2O 2+2H 2O═4NaOH+O 2↑
【提出猜想】①没有变质 ②部分变质 ③全部变质
【实验过程及结论】
(1)取少量样品于试管中,加入足量水,无明显现象,证明猜想 正确(填序号);
(2)取少量(1)中所得溶液于试管中,滴加适量稀盐酸,有无色气体产生,证明原样品中一定含有 ;
(3)请在原有实验的基础上,进一步设计实验证明原样品中还可能含有什么物质。(简写实验步骤、现象和结论)
牛奶含有丰富的蛋白质,《本草纲目》中说牛奶有“返老还童”的功效,“奶茶”是否也具有类似的功效?
【查阅资料】食醋中的酸性物质会使蛋白质凝固和沉淀。
【实验步骤】
①在盛有100毫升某奶茶的烧杯中,加入足量的食醋,充分搅拌后过滤、干燥,称量滤渣的质量。
②选取4种品牌的纯牛奶各100毫升,分别倒入4个烧杯,重复步骤①操作。
【数据记录】如图。请回答下列问题:
(1)从样品的选取上看,该实验存在的缺陷是 。
(2)下列因素会对滤渣质量多少产生影响的是 。
A.倒入食醋的量 B.被测样品的体积 C.烧杯的大小
(3)上述实验只能粗略测定蛋白质的含量,准确检测的方法之一是:先对样品进行氮元素质量的测定,再根据蛋白质中氮元素的含量约16%,折算成蛋白质的质量,已知牛奶、奶茶中的营养成分有蛋白质、脂肪、糖类等,那么,利用这种方法检测牛奶、奶茶中的蛋白质含量,其前提条件是 。
(4)据统计,我国人均乳制品消费量只及世界人均的 ,而白酒的消费量却与牛奶相似,可见,提高健康饮食的意识势在必行,下列观点和做法合理的是 。
,而白酒的消费量却与牛奶相似,可见,提高健康饮食的意识势在必行,下列观点和做法合理的是 。
A.选择食品前,影响研读其标签 B.购买食品时,主要看口味
C.食品价格越贵,对健康越有益 D.根据膳食平衡,选择食品。

某化学兴趣小组同学对家用普通干电池中含有的物质产生了浓厚的兴趣。他们剥开电池时闻到氨味且发现有黑色物质。
[提出问题]为什么有氨味?黑色物质的成分是什么?
[猜想假设]能闻到氨味说明含有铵盐(如NH4Cl);黑色固体可能有铁粉、氧化铜或二氧化锰。
[实验探究]同学们分别设计实验进行探究。
实验I.小聪取适量黑色物质与 混合置于研钵内研磨,嗅到强烈氨味,再用湿润的红色石蕊试纸检测,观察到试纸变蓝,证明黑色物质中含有铵盐。
实验II.小敏将黑色物质加入适量的水中搅拌溶解,静置后 ,取不溶物进行实验。
实验步骤 |
实验现象。实验结论 |
|
1、取适量黑色滤渣装入试管中,再加入过量稀盐酸 |
无气泡生成,溶液不变色 |
|
2、取适量黑色滤渣装入另一支试管中,再加入 溶液,向上述试管中伸入带火星的小木条。 |
|
黑色粉末中含有二氧化锰 |
[交流讨论]
步骤2中发生反应的化学方程式为 。
据下列仪器裝置图,请回答有关问题。
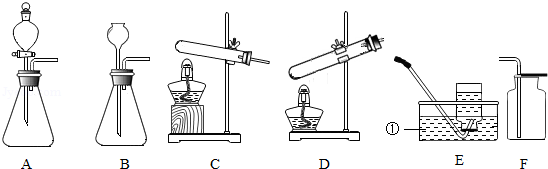
(1)图中仪器①的名称 。
(2)若实验室用高锰酸钾制取氧气,反应的化学方程式为 ,可用于该反应的气体发生装置是 (填字母序号),该装置的试管口还缺少 ,用装置F收集一瓶O2,如何检验O2是否已收集满?
(3)实验室没有大理石和石灰石,只有碳酸钠粉末和盐酸,为了顺利制取一瓶CO2气体,请你选择最佳的装置组合(填字母序号),选择该气体发生装置的理由是 。
结合下列实验装置,回答:
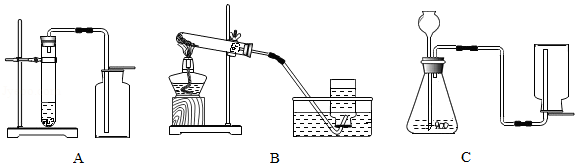
(1)实验室若用分解暗紫色固体制取O2,该固体的名称是 ,可选 (填字母,下同)装置。若用分解H2O2溶液制取O2,可选 装置。
(2)探究CO2性质的装置Ⅰ、Ⅱ如下:
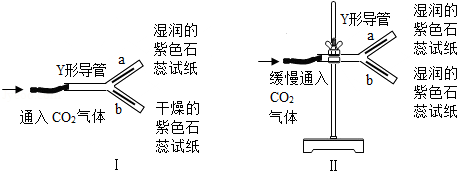
①装装置Ⅰ,将Y形导管平放于桌面上,通入CO2后,观察到a管中试纸变红色,
b管中试纸无明显变化,此现象说明CO2能与 反应,生成的 使紫色石蕊变红色。
②装置Ⅱ,将Y形导管固定在铁架台上,a管在上方,b管在下方,通入CO2后,观察到b管中试纸先变红色且颜色较深,a管中试纸后变红色且颜色较浅,此现象说明CO2具有①所验证的性质外,还说明CO2的 。
(3)实验室制取CO2的化学方程式为 ,应选 (填字母)装置,选择该装置的理由是 。
学习了酸、碱、盐有关知识后,小明在实验室称量氢氧化钠固体,配制了溶质质量分数为10%的氢氧化钠溶液,进行以下探究:

(1)若图Ⅰ中游码标尺读数为1.8,则他称取的氢氧化钠质量是 g.
(2)图Ⅱ中反应的化学方程式是 .
(3)图Ⅲ中玻璃棒的作用是 ,当出现较多固体时,应 .
2022年我国将有6名航天员生活在空间站。氧气、水、食物等是维持航天员驻留空间站的必要物质。为提高物质的利用率,目前空间站通过以下途径实现物质循环利用:
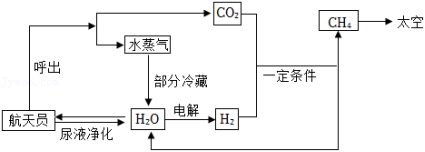
(1)由图可知,目前空间站通过物质循环获得水的途径共有 条,其中尿液净化时必须除去尿液中的 等代谢废物。
(2)为实现氧的循环,目前空间站内利用氢气和航天员呼出的二氧化碳,在一定条件下转化为甲烷和水,化学方程式为 。据测算,正常情况下一位航天员一天呼出的二氧化碳质量约1.1千克,若这些二氧化碳全部与氢气反应,则可生成水多少千克?
海洋是人类宝贵的自然资源,海水“晒盐”和海水“制碱”体现了人类利用和改造自然的智慧,请根据粗盐“制碱”的流程图(如图)回答问题:
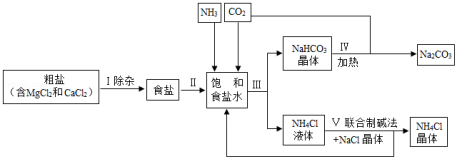
(1)步骤Ⅰ除杂中,常见的方法有两种:一是物理方法,即用NaCl溶液浸洗粗盐,溶解除去其中的可溶性杂质,则浸洗溶液应选用NaCl的 (填“饱和”或“不饱和”)溶液;二是化学方法,操作步骤依次为:加水溶解→加过量试剂①→加过量试剂②→过滤→加适量盐酸,以下试剂①②组合选用合理的是 。
A.①Ca(OH)2②Na2CO3
B.①Na2CO3②Ca(OH)2
C.①KOH②Na2CO3
D.①NaOH②Na2CO3
(2)步骤Ⅲ先向饱和食盐水中通入氨气,再通入二氧化碳,这样做的目的是 ,写出步骤Ⅲ反应的化学方程式 。
(3)步骤Ⅳ发生的反应属于 反应(填基本反应类型)。
(4)我国化学家侯德榜创立的联合制碱法的优点有 。
A.无“索尔维氨碱法”中的废弃物CaCl2生成,有利于保护环境
B.大大提高了食盐的利用率,节约了成本
C.将“制碱”与制氨生产联合起来,同时析出的NH4Cl晶体可用作复合肥
溶液与人类生产、生活密切相关。
(1)把少量下列物质分别放入水中,充分搅拌,能得到溶液的是 (填序号)。
A.硝酸钾
B.植物油
C.面粉
(2)下列有关溶液的说法中,正确的是 (填序号)。
A.凡是均一的、稳定的液体一定是溶液
B.溶液是均一的、稳定的混合物
C.溶液一定是无色的,且溶剂一定是水
(3)如图为甲、乙、丙三种固体物质的溶解度曲线。
①t 1℃时,甲、乙两种物质的溶解度 (填"相等"或"不相等")。
②t 2℃时,甲物质饱和溶液中溶质与溶剂的质量比为 (填最简比)。
③现有t 1℃时甲、乙、丙三种物质的饱和溶液,将这三种溶液分别升温到t 2℃,所得溶液中溶质质量分数大小关系是 (填序号)。
A.甲>乙>丙
B.甲=乙<丙
C.甲=乙>丙
(4)用固体氯化钠和蒸馏水配制50g溶质质量分数为6%的氯化钠溶液,需要氯化钠的质量为 g.若用已配好的50g溶质质量分数为6%的氯化钠溶液配制溶质质量分数为3%的氯化钠溶液,需要加水的质量为 g。

学校化学兴趣小组欲利用下列装置进行相关实验探究,请你分析并填空。
(1)写出图中标号仪器名称② 。
(2)下列哪种方法可以得到平稳的氧气流? (填序号)
①把二氧化锰加入装有过氧化氢溶液的试管中
②把过氧化氢溶液缓缓加入盛有少量二氧化锰的试管中
(3)某同学利用同一套发生装置先后完成实验室制取二氧化碳和实验室制取氧气,他选择的发生装置是 (填字母代号),利用该装置制取氧气的化学方程式为 。
(4)实验室制取二氧化碳,常选用装置 (填字母代号)收集二氧化碳。收集时,将燃着的木条放在瓶口,观察到 ,说明瓶中已集满二氧化碳。
试题篮
()