利用如图所示原电池可测量空气中Cl2含量,其中电解质是Ag+可以自由移动的固体物质。下列分析不正确的是
| A.电子经外电路流向Pt电极 |
| B.电池工作时,电解质中Ag+数目减少 |
| C.正极反应:Cl2+2e—+2Ag+ = 2AgCl |
| D.空气中c(Cl2)越大,Ag极消耗速率越快 |
熔融碳酸盐燃料电池,是由多孔陶瓷阴极、多孔陶瓷电解质隔膜、多孔金属阳极、金属极板构成的燃料电池。其电解质是熔融态碳酸盐。下图是用熔融碳酸盐作电解质,氢气和氧气形成的燃料电池;下列说法正确的是:
| A.该电池放电时,负极的反应式为:H2 - 2e-+CO2 =H2O+ CO32- |
| B.该电池中CO32-的为由左边移向右边移动 |
| C.该电池放电时,正极的反应式为:O2 +2CO2+ 4e- =2CO32- |
| D.该电池放电时,当转移4mol e-时正极消耗1mol O2和1mol CO2 |
Al-AgO电池可用作水下动力电源,其原理如图所示。该电池反应的化学方程式为:2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O,则下列说法正确的是
| A.当电极上析出0.54 g Ag时,电路中转移的电子为0.01 mol |
B.该隔膜是阳离子交换膜 |
| C.Al电极的反应式为:Al-3e-+3OH-=Al(OH)3 |
| D.正极的电极反应式为:AgO+2e-+2H+=Ag+H2O |
铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O= Fe(OH)2+2Ni(OH)2
下列有关该电池的说法不正确的是
| A.电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe |
| B.电池放电时,负极反应为Fe+2OH−−2e−=Fe(OH)2 |
| C.电池充电过程中,阴极附近溶液的pH降低 |
| D.电池充电时,阳极反应为2Ni(OH)2+2OH−−2e−=Ni2O3+3H2O |
镉镍可充电电池在现代生活中有广泛应用,它的充、放电反应按下式进行:Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2由此可知,该电池放电时的负极是( )。
Cd(OH)2+2Ni(OH)2由此可知,该电池放电时的负极是( )。
| A.Cd(OH)2 | B.Ni(OH)2 | C.Cd | D.NiOOH |
锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列叙述正确的是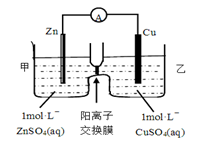
| A.铜电极上发生氧化反应 |
| B.电池工作一段时间后,甲池的c(SO42-)减小 |
| C.电池工作一段时间后,乙池溶液的总质量增加 |
| D.阴阳离子离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡 |
常用的电池是一个液体电解质将两个固体电极隔开。而钠-硫(Na/S8)电池正相反,它是由固体电解质将两个液体电极隔开(如图),一个由钠-β-氧化铝固体电解质做成的中心管,将内室的熔融钠(熔点98℃)和外室的熔融硫(熔点119℃)隔开,并允许Na+通过。下列有关说法不正确的是
| A.a为电池的正极 |
| B.充电时b接电源的正极 |
| C.正极反应为:nS8+16ne-=8Sn2- |
| D.Na+可以穿过固体电解质从而传递电流 |
一种使用阴离子交换膜(只也许阴离子通过)的铜锌电池结构结构如下图:

以下选项两栏内容正确且相关联的是
| 选项 |
操作与现象 |
解释与推论 |
| A |
电池放电时化学能转化为电能 |
Zn(s)+ Cu2+(aq)= Zn2+ + Cu(s) △H>0 |
| B |
该电池充电时铜棒变细 |
两电极区溶液颜色都变深 |
| C |
该电池放电时铜棒是电池正极 |
Cl-通过交换膜从左(铜棒区)向右(锌棒区)移动 |
| D |
该电池充电时a接电源正极 |
电极反应Cu2++2e- = Cu |
用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图所示。下列说法正确的是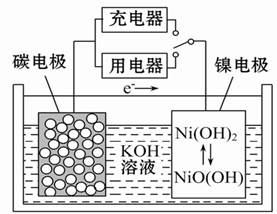
| A.放电时,OH-向镍电极作定向移动 |
| B.放电时,负极的电极反应为:H2-2e-+2OH-="==" 2H2O |
| C.充电时,将电池的碳电极与外电源的正极相连 |
| D.充电时,阴极的电极反应为:Ni(OH)2+OH--e-===NiO(OH)+H2O |
液流电池是一种新的蓄电池,是利用正负极电解液分开,各自循环的一种高性能蓄电池,具有容量高、使用领域(环境)广、循环使用寿命长的特点。如图是一种锌溴液流电池,电解液为溴化锌的水溶液。下列说法正确的是
A.充电时阳极的电极反应式:Zn-2e- Zn2+ Zn2+ |
| B.充电时电极a为外接电源的负极 |
| C.放电时Br-向右侧电极移动 |
| D.放电时左右两侧电解质储罐中的离子总浓度均增大 |
铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2。下列有关该电池的说法不正确的是
| A.电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe |
| B.电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2 |
| C.电池充电时,阳极反应为2Ni(OH)2+2OH--2e-=Ni2O3+3H2O |
| D.电池充电过程中,阴极附近溶液的pH降低 |
利用人工模拟光合作用合成甲酸的原理为:
2CO2+2H2O 2HCOOH+O2,装置如图所示,
2HCOOH+O2,装置如图所示,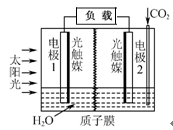
下列说法不正确的是
| A.电极1周围pH增大 |
| B.电子由电极1经过负载流向电极2 |
| C.电极2的反应式:CO2+2H++2e-=HCOOH |
| D.该装置能将太阳能转化为化学能和电能 |
纸电池是一种有广泛应用的“软电池”,右图这种碱性纸电池采用薄层纸片作为载体和传导体,纸的两面分别附着锌和二氧化锰。下列有关该纸电池说法不合理的是
| A.Zn为负极,进行氧化反应 |
| B.电池工作时,电子由MnO2流向Zn |
| C.正极反应:MnO2+e-+H2O=MnO(OH)+OH- |
| D.电池总反应:Zn+2MnO2+2H2O=Zn(OH)2+2MnO(OH) |
某科研小组成功研制出能在“数分钟之内”将电量充满的锂电池,其成本只有传统锂电池的一半。他们把锂锰氧化物(LMO)浸泡在石墨里面,使其变成一个可以导电的密集网络的负极材料,与电 解质和正极材料(石墨)构成可充电电池。若电解液为LiAlCl4-SOCl2,电池的总反应为:
4LiCl+S+SO2 4Li+2SOCl2
4Li+2SOCl2
下列说法正确的是
| A.电池的电解液可为LiCl水溶液 |
| B.放电时负极反应式为:Li-e-+ Cl-=LiCl |
| C.放电时正极反应式为: 2SOCl2+4e-=4Cl-+S+SO2 |
| D.放电时电子从负极经外电路流向正极,再从正极经电解质流向负极 |
铅蓄电池用途极广,电解液为30% H2SO4溶液,电池的总反应式可表示为:Pb(s)+PbO2(s)+2H2SO4(aq)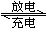 2PbSO4(s)+2H2O(l)
2PbSO4(s)+2H2O(l)
下列有关叙述正确的是
| A.放电时电解液的密度不断增大 |
| B.放电时电子从Pb通过导线转移到PbO2 |
| C.充电时Pb极与外电源的负极相连 |
| D.充电时PbO2电极发生还原反应,Pb电极上发生氧化反应 |
试题篮
()