H3AsO3与SnCl2在浓盐酸中可发生以下反应:3SnCl2+12Cl-+2H3AsO3+6H+=2As+3M+6H2O关于该反应的说法中正确的组合是
①氧化剂是H3AsO3、②还原性:As>SnCl2、
③每生成1 mol As,反应中转移电子的物质的量为3 mol、
④ M为OH-、 ⑤ SnCl62-是氧化产物
| A.①③⑤ | B.①②④⑤ | C.①②③④ | D.只有①③ |
下列参数比较及解释均正确的是( )
| 选项 |
参数 |
比较 |
解释 |
| A |
还原性 |
Br->Cl- |
元素的非金属性越强,简单阴离子的还原性越弱 |
| B |
半径 |
Na+<Mg2+<Al3+ |
同一周期粒子半径随原子序数的递增逐渐减小 |
| C |
酸性 |
H2SO3>H2CO3 |
元素的非金属性越强,其含氧酸的酸性越强 |
| D |
沸点 |
HF<HCl<HI |
组成结构相似的物质,相对分子质量越大沸点越高 |
根据下列化学方程式判断物质氧化性或还原性强弱排序正确的是
① 2FeCl3+Cu=2FeCl2+CuCl2 ②CuCl2+Fe=FeCl2+Cu
| A.还原性:Fe > Cu>FeCl2 | B.还原性:Fe > FeCl2> Cu |
| C.氧化性:CuCl2>FeCl3>FeCl2 | D.氧化性:FeCl3 >FeCl2>CuCl2 |
已知下列氧化还原反应:2BrO3-+Cl2==Br2+2ClO3-,5Cl2+I2+6H2O==2IO3-+10Cl-+12H+,
ClO3-+5Cl-+6H+==3Cl2↑+3H2O。上述条件下,各微粒氧化性由强到弱的排列顺序正确的是
| A.ClO3->BrO3->IO3->Cl2 | B.BrO3->Cl2>ClO3->IO3- |
| C.BrO3->ClO3->Cl2>IO3- | D.Cl2>BrO3->ClO3->IO3- |
已知:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O; Cl2+2FeCl2=2FeCl3; 2KI+2FeCl3=2KCl+I2+2FeCl2。 则下列判断正确的是
| A.氧化性MnO4->Cl2>I2>Fe3+ | B.还原性:Fe2+>I->Cl- |
| C.Fe3+能将I-氧化为I2 | D.Fe2+只有还原性 |
根据反应:①2C-+A2===2A-+C2;②2B-+D2===2D-+B2;③2A-+B2===2B-+A2。推断A-、B-、C-、D-的还原能力由强到弱的顺序是 ( )
| A.A->B->C->D- |
| B.D->B->A->C- |
| C.D->A->B->C- |
| D.C->A->B->D- |
根据下列三个反应的化学方程式,判断有关物质的还原性的强弱顺序为
①I2 + SO2 + 2H2O = H2SO4 + 2HI
②2FeCl2 + Cl2 = 2FeCl3
③2FeCl3 + 2HI = 2FeCl2 + I2 + 2HCl
| A.I-> Fe2+>Cl->SO2 | B.Cl-> Fe2+> SO2>I- |
| C.Fe2+>I->Cl->SO2 | D.SO2>I-> Fe2+>Cl- |
由相同条件下的三个反应:2A +B2 ="2B" +A2;2C +A2 ="2A" +C2;2B +D2 ="2D" +B2;
可判断
| A.氧化性:A2>B2>C2>D2 |
| B.还原性:C->A->B->D- |
| C.2A-+ D2 = 2D-+A2不能进行 |
| D.2C-+B2 =2B-+C2不能进行 |
常温下,下列三个反应均能发生:
X2+2W2+=2X-+2W3+ Z2+2X-=2Z-+X2 2W3++2Y-=2W2++Y2
则在相同条件下,下列三个反应也能发生的是( )
①Y2+2X-=2Y-+X2 ②Z2+2Y-=2Z-+Y2 ③2W3++2Z-=2W2++Z2
| A.只有① | B.只有② | C.①和② | D.②和③ |
向CuSO4溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,溶液变为棕色。再向反应后的混合物中不断通人 SO2气体,溶液逐渐变成无色。下列分析正确的是
| A.滴加KI溶液时,转移2 mol e-时生成 1 mol白色沉淀 |
| B.通入SO2后溶液逐渐变成无色,体现了 SO2的漂白性 |
| C.通入SO2时,SO2与I2反应,I2作还原剂 |
| D.上述实验条件下,物质的氧化性:Cu2+ >I2 > SO2 |
根据下列反应判断有关物质还原性由强到弱的顺序正确的是
(1)H2SO3 + I2 + H2O =" 2HI" + H2SO4
(2)2FeCl3 + 2HI = 2FeCl2 + 2HCl + I2
(3)3FeCl2 + 4HNO3 = 2FeCl3 + NO↑+ 2H2O + Fe(NO3)3
| A.H2SO3>I->Fe2+>NO |
| B.I->H2SO3>Fe2+>NO |
| C.Fe2+>I->H2SO3>NO |
| D.NO>Fe2+>H2SO3>I- |
有下列三个反应:
①Cl2+FeI2===FeCl2+I2
②2Fe2++Br2===2Fe3++2Br-
③Co2O3+6HCl===2CoCl2+Cl2↑+3H2O
下列说法正确的是
| A.反应①②③中的氧化产物分别是I2、Fe3+、CoCl2 |
| B.根据以上方程式可以得到氧化性:Cl2>Fe3+>Co2O3 |
| C.可以推理得到Cl2+FeBr2===FeCl3+Br2 |
| D.在反应③中当1 mol Co2O3参加反应时,2 mol HCl被氧化 |
新型纳米材料MFe2O,(3<x <4)中M表示十2价的金属元素,在反应中化合价不发生变化。常温下,MFe2Ox能使工业废气中的SO2转化为S,转化过程为:
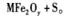 下列判断正确的是
下列判断正确的是
| A.MFe2Ox是还原剂 | B.SO2被氧化 |
| C.x>y | D.氧化性:MFe2Oy>SO2 |
试题篮
()