本题含两小题,共14分。
(1)某反应体系中的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O。
①将Au2O3之外的物质分别填如以下空格内,配平后标出电子转移的方向和数目。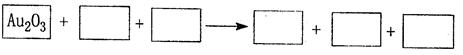
②反应中,被还原的元素是 ,还原剂是 。
③纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白后布匹的“脱氯剂”,Na2S2O3和Cl2反应的产物是H2SO4、NaCl和HC1,,则还原剂与氧化剂物质的量之比为
。
(2)按要求写出有水参与的氧化还原反应的化学方程式
①水是氧化剂:
②水是还原剂:
③水既不是氧化剂也不是还原剂:
以下有水参与的化学反应都属于氧化还原反应,但水既不做氧化剂又不做还原剂的有 。
①2Na2O2+2H2O=4NaOH+O2↑ ②Cl2+H2O="HCl+HClO "
③C+H2O=CO+H2 ④3NO2+H2O=2HNO3+NO
⑤2Na+2H2O=2NaOH+H2↑ ⑥2F2+2H2O=4HF+O2
铜跟稀硝酸可发生反应:3Cu + 8HNO3(稀)=3Cu(NO3)2 + 2NO↑+ 4H2O。在该反应中,铜元素的化合价 (填“升高”或“降低”),被 (填“氧化”或“还 原”);硝酸体现_____________性,若反应中生成转移0.6mole,则生成___ L NO(标况)。
原”);硝酸体现_____________性,若反应中生成转移0.6mole,则生成___ L NO(标况)。
(1)实验室制取Cl2的反应方程式之一为:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O被氧化的盐酸占反应盐酸总量的 ,当标准状况下有11.2L氯气生成时,该反应的电子转移数为 。
(2)用双线桥法标出电子转移情况:3BrF3+5H2O=HBrO3+Br2+O2+9HF,当180g水都做还原剂时,被自身还原的BrF3是 mol。
(3)已知下列两个氧化还原反应:O2+4HI=2I2+2H2O 及Na2S+I2=2NaI+S,则三种单质的氧化性由强到弱的顺序为:
(6分)已知反应:① 2K2CrO4+H2SO4=K2Cr2O7+K2SO4+H2O;② Fe2(SO4)3+2HI=2FeSO4+I2+H2SO4;
③[ ]K2Cr2O7+[ ]FeSO4+[ ] H2SO4 =[ ]Fe2(SO4)3+[ ]Cr2(SO4)3+[ ]K2SO4+[ ]H2O
(1)上述三个反应中,属于氧化还原反应的是 (填序号);
(2)配平反应③的化学方程式 ;
(3)K2Cr2O7、I2、Fe3+三种微粒氧化性由强到弱的顺序: 。
(每空1分,共11分)从下列各组反应对比,判断那种微粒的氧化性最强。
(1)铁钉浸入硫酸铜溶液中后,表面会附有红色物质,铜丝浸入硝酸银溶液后,表面会附有银白色物质。则铜、铁、银中,_____ ___原子的还原性最强;Cu2+、Ag+、Fe2+中, 离子的氧化性最强。
(2)在氯气中Fe锈蚀成棕褐色物质FeCl3,而在盐酸中生成淡绿色溶液FeCl2。则氯气分子、氢离子、氯离子中, 具有氧化性, 氧化性最强。请书写出以上各反应的化学方程式________ 、 。
(3)已知在ⅣA族元素中,Pb2+和Sn4+的化合物较为稳定。
①据此可判断PbO2具有较强的________性,SnCl2具有较强的 性;写出PbO2溶于盐酸的离子方程式__________;写出SnCl2和FeCl3溶液混合的离子方程式__________ ;
②PbO2、Fe3+、Cl2、Sn4+氧化性由强到弱的顺序是__________ 。
(1)写出下列反应的离子方程式:
①氯化铵溶液和氢氧化钠溶液反应 ;
②少量二氧化碳通入澄清石灰水 ;
③三氧化二铁和盐酸反应 。
(2)铜和浓硫酸发生反应的化学方程式为:Cu +2H2SO4(浓) CuSO4+SO2↑+2H2O,其中硫元素被________(填“氧化”或“还原”,下同),发生 反应;浓H2SO4作_________剂,具有 性。
CuSO4+SO2↑+2H2O,其中硫元素被________(填“氧化”或“还原”,下同),发生 反应;浓H2SO4作_________剂,具有 性。
金属铜能被氯化铁浓溶液腐蚀,其化学反应是:Cu+2FeCl3=CuCl2+2FeCl2。现将有铜的印刷线路板浸入120mL氯化铁浓溶液中,有9.6g铜被腐蚀掉。取出印刷线路板,向溶液中加入8.4g铁粉,经充分反应,溶液中还存在4.8g不溶解的物质。(设溶液体积不变,且不考虑金属离子水解)。请回答下列问题:
(1)向溶液中加入铁粉后,发生反应的离子反应方程式为 , 。
(2)充分反应后,溶液中存在4.8g不溶物的成分为 。
(3)充分反应后溶液中一定不存在的金属离子为 。
(4)比较Fe2+、Fe3+、Cu2+的氧化性大小: 。
(5)试计算最后溶液中Fe2+离子的物质的量浓度 mol/L
(1)已知反应MnO2+4HCl (浓) MnCl2+Cl2↑+2H2O中,若二氧化锰与足量的浓盐酸反应制得3.55gCl2,通过计算回答:用双线桥标出反应中电子转移的方向和数目 ,参加反应的HCl的物质的量为 ,其中被氧化的HCl的质量 。
MnCl2+Cl2↑+2H2O中,若二氧化锰与足量的浓盐酸反应制得3.55gCl2,通过计算回答:用双线桥标出反应中电子转移的方向和数目 ,参加反应的HCl的物质的量为 ,其中被氧化的HCl的质量 。
(2)某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、 H3AsO4、H2O和一种未知物质X。
①已知KBrO3在反应中得到电子,则该反应的还原剂是____________________。
②已知0.2 mol KBrO3在反应中得到1 mol电子生成X,则X的化学式为_______,写出一个包含上述七种物质的氧化还原反应方程式(不需配平)_________ ________。
③根据上述反应可推知( )
| A.氧化性:KBrO3>H3AsO4 | B.氧化性:H3AsO4>KBrO3 |
| C.还原性:AsH3>X | D.还原性:X>AsH3 |
下面三个方法都可以用来制氯气:
①4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
②KClO3+6HCl=3Cl2↑+KCl+3H2O
③KMnO4+HCl(浓)—KCl+MnCl2+Cl2↑+H2O(未配平),
根据以上三个反应,回答有关问题:
(1)反应的②的离子方程式为________________。
(2)反应②中,氧化产物与还原产物的质量比为____________。
(3)请将反应③配平:__KMnO4+__HCl(浓)=__KCl十__MnCl2+__Cl2↑+__H2O
(4)若要制得相同质量的氯气,①②③反应中电子转移的数目之比为_________。
(5)已知反应④:4HCl(g)+O2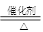 2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为________________。
2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为________________。
某校学生化学实验小组,为验证非金属元素氯的氧化性强于硫和氮,设计了一套实验装置:(部分夹持装置已略去) 
(1)写出A中反应的离子方程式 。
(2)B中出现黄色浑浊现象,产生此现象的离子方程式 。
(3)试从原子结构角度解释氯的氧化性大于硫原因 。
(4)D中干燥管中出现的现象及化学方程式 ; 。
(5)有同学认为D中的现象并不能说明氯的氧化性大于氮,需要在C之前加装洗气装置,该洗气装置中盛装 试剂。
(6)还有什么方法能证明氧化性Cl2 > S,用一种相关事实说明 。
过氧化氢H2O2(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~D涉及H2O2的反应,填写空白:
| A.Na2O2 +2HCl= 2NaCl+H2O2 |
| B.Ag2O+ H2O2=2Ag+O2+ H2O |
| C.2 H2O2="2" H2O+O2 |
| D.3 H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8 H2O |
(1)H2O2仅体现氧化性的反应是(填代号) 。
(2)H2O2既体现氧化性又体现还原性的反应是(填代号) 。
(3)B反应式中的氧化产物是 。
(4)上述反应说明H2O2、Ag2O、K2CrO4氧化性由强到弱的顺序是: 。
分析下列反应:3S+6 KOH = 2K2S+K2SO3+3H2O,据此作答:
(1)用双线桥标出该反应中电子的转移方向和数目:3S +6 KOH = 2K2S+K2SO3+3H2O
(2)该反应的氧化产物是 。
(3)该反应的氧化剂与还原剂的质量比是 。
(4)当消耗0.3 mol S时,则转移的电子数是 。
烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点。
(1)烟气脱硫、脱硝的环境意义是 ;
(2)一种选择性催化脱硝(NO2)的原理为:6NO2+8NH3 7N2+12H2O
7N2+12H2O
①上述反应中被还原的元素是 (填元素符号),反应中每转移2.4mol电子,生成N2的物质的量为 。
②超音速飞机排放的尾气是平流层中NOx的主要来源.它们破坏臭氧层的主要机理为:
Ⅰ、O3 O+O2
O+O2
Ⅱ、NO+O3 →NO2+O2
Ⅲ、 NO2+O→NO+O2
上述反应中NO所起的作用是 ;
(3)下表列出了2种燃煤烟气脱硫方法的原理。
| 方法Ⅰ |
用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4 |
| 方法Ⅱ |
用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫 |
方法Ⅰ中用氨水吸收燃煤烟气中的SO2转化为NH4HSO3,写出该反应的离子方程式: ,是利用了SO2的 性质(选填字母编号)。
A.漂白性 B.氧化性 C.还原性 D.酸性氧化物
试题篮
()