下列做法与盐类水解知识无关的是
| A.实验室盛放碳酸钠溶液的试剂瓶必须用橡胶塞而不能用玻璃塞 |
| B.施肥时,草木灰(有效成分为 K2CO3)不能与碳酸氢铵混合使用 |
| C.Al2S3不能用复分解反应的方法在溶液中制取,而只能用干法制备。 |
| D.配制 FeCl2溶液时常常要在溶液中加入少量铁粉 |
下列有关问题,与盐的水解有关的是
①NH4Cl与ZnCl2溶液可作焊接金属中的除锈剂
②用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂
③草木灰与铵态氮肥不能混合施用
④实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃塞
⑤加热蒸干AlCl3溶液得到Al(OH)3固体
| A.②③④ | B.①②③④⑤ | C.①④⑤ | D.①②③ |
是阿伏加德罗常数的值,下列说法正确的是( )
| A. |
16.25g 水解形成的 胶体粒子数为 |
| B. |
22.4L(标准状况)氩气含有的质子数为 |
| C. |
92.0g甘油(丙三醇)中含有羟基数为 |
| D. |
与 在光照下反应生成的 分子数为 |
下列离子方程式中,属于水解反应的是( )
A.HCOOH+H2O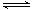 HCOO-+H3O+ HCOO-+H3O+ |
B.HS-+H2O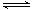 S2-+H3O+ S2-+H3O+ |
C.CO32-+H2O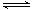 HCO3-+OH- HCO3-+OH- |
D.HCO3-+H2O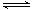 CO32-+H3O+ CO32-+H3O+ |
下面关于水解应用的说法错误的是
| A.用热水溶解纯碱能够提高去油污的效果 |
| B.配制氯化铁溶液时滴加几滴稀盐酸可以防止氢氧化铁形成 |
| C.硫酸铵和草木灰混合施用到农田可以增强肥效 |
| D.盐碱地(含NaCl、 Na2 CO3)施加适量石膏可以降低土壤的碱性 |
下列实验现象以及结论均合理的是
| A.在一块镀锡铁板刻一划痕,滴加酸化的食盐水浸泡及KSCN溶液,溶液颜色没有变化,判断其具有好的耐腐蚀性 |
| B.测定一定物质的量浓度的某NaA溶液的pH,pH>7,可以说明HA是弱酸 |
| C.在氯化银的悬浊液中加入碘化钠溶液,沉淀颜色不变,说明氯化银的溶解度比碘化银大 |
| D.在酸碱中和滴定中,用标准氢氧化钠溶液测定醋酸溶液的浓度时,用甲基橙做指示剂对滴定终点的判断比用酚酞的更准确 |
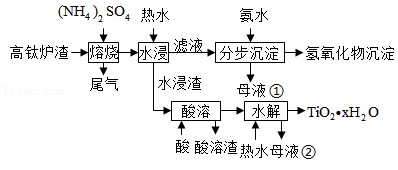
磁选后的炼铁高钛炉渣,主要成分有 、 、 、 、 以及少量的 。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表
| 金属离子 |
|
|
|
|
| 开始沉淀的pH |
2.2 |
3.5 |
9.5 |
12.4 |
| 沉淀完全 的pH |
3.2 |
4.7 |
11.1 |
13.8 |
回答下列问题:
(1)"焙烧"中, 、 几乎不发生反应, 、 、 、 转化为相应的硫酸盐。写出 转化为 的化学方程式 。
(2)"水浸"后"滤液"的 约为2.0,在"分步沉淀"时用氨水逐步调节 至11.6,依次析出的金属离子是 。
(3)"母液①"中 浓度为 。
(4)"水浸渣"在 "酸溶",最适合的酸是 。"酸溶渣"的成分是 、 。
(5)"酸溶"后,将溶液适当稀释并加热, 水解析出 沉淀,该反应的离子方程式是 。
(6)将"母液①"和"母液②"混合,吸收尾气,经处理得 ,循环利用。
关于浓度均为0.1mol/L的四种溶液:①NH3·H2O、②HCl、③NH4Cl 、④(NH4)2CO3,下列说法正确的是
| A.由水电离出的c(H+):④>③>①>② |
| B.①、②和③等体积混合后的溶液:pH=7 |
| C.c(NH4+):③>④>① |
| D.①和②等体积混合后的溶液:c(NH4+)+c(NH3·H2O)=0.1mol/L |
99℃时,Kw=1.0×10-12,该温度下测得0.1mol/LNa2A溶液的pH=6。下列说法不正确的是( )
| A.H2A在水溶液中的电离方程式为H2A=2H++A2- |
| B.该温度下,将0.01mol/L的H2A溶液稀释20倍后溶液的pH=3 |
| C.体积相同,pH均为1的盐酸和H2A溶液分别与足量的Zn反应,产生H2较多的是H2A |
| D.将0.1mol/L的H2A溶液与0.2mol/L的氨水等体积混合后,溶液中浓度最大的离子是NH4+ |
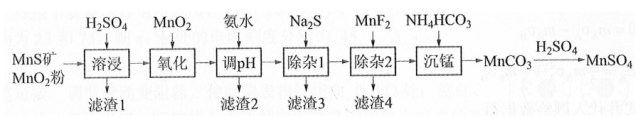
高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
相关金属离子[ ]形成氢氧化物沉淀的pH范围如下:
| 金属离子 |
|
|
|
|
|
|
|
| 开始沉淀的pH |
8.1 |
6.3 |
1.5 |
3.4 |
8.9 |
6.2 |
6.9 |
| 沉淀完全的pH |
10.1 |
8.3 |
2.8 |
4.7 |
10.9 |
8.2 |
8.9 |
(1)"滤渣1"含有S和________;写出"溶浸"中二氧化锰与硫化锰反应的化学方程式________。
(2)"氧化"中添加适量的 的作用是将________。
(3)"调pH"除铁和铝,溶液的pH范围应调节为________~6之间。
(4)"除杂1"的目的是除去 和 , "滤渣3"的主要成分是________。
(5)"除杂2"的目的是生成 沉淀除去 。若溶液酸度过高, 沉淀不完全,原因是________。
(6)写出"沉锰"的离子方程式________。
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为 , 其中Ni、Co、Mn的化合价分别为+2、+3、+4。当 时, z=________。
代表阿伏伽德罗常数的值,下列说法正确的是()
| A. | 常温常压下, 中所含P-P键数目为 |
B. | 溶液中所含 的数目为 |
| C. | 标准状况下,11.2L甲烷和乙烯混合物中含氢原子数目为 |
D. | 密闭容器中, 和 催化反应后分子总数为 |
化学在生活中有着广泛的应用,下列对应关系错误的是( )
| |
化学性质 |
实际应用 |
| A |
和小苏打反应 |
泡沫灭火器灭火 |
| B |
铁比铜金属性强 |
腐蚀Cu刻制印刷电路板 |
| C |
次氯酸盐具有氧化性 |
漂白粉漂白织物 |
| D |
HF与 反应 |
氢氟酸在玻璃器皿上刻蚀标记 |
| A. | A |
B. | B |
C. | C |
D. | D |
化学与社会、生活密切相关,对下列现象或事实的解释正确的是( )
| 选项 |
现象或事实 |
解释或对应的方程式 |
| A |
用热的纯碱溶液洗去油污 |
CO32-+2H2O H2CO3+2OH- H2CO3+2OH-溶液呈碱性 |
| B |
酸雨样品在空气中放置pH减小 |
亚硫酸被氧化为硫酸2SO32-+O2=2SO42- |
| C |
“84”消毒液具有漂白性 |
2ClO-+CO2+H2O=2HClO+CO32- |
| D |
用加热法除去NaOH固体中混有的NH4Cl固体 |
NH4Cl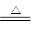 NH3↑+HCl↑ NH3↑+HCl↑ |
常温下,0.1mol/L的氯化铵溶液中,离子浓度最大的是
| A.Cl- | B.OH- | C.H+ | D.NH4+ |
试题篮
()