(每空2分,共12分)焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4C1、FeC13、N2、Fe2O3、Fe和X。
(1)根据题意,可判断出X是 (写化学式)。
(2)写出并配平该反应的化学方程式:
(3)发生氧化反应的物质是 ,反应中4mol的氧化剂能 (填“失去”或
“得到”) mol电子.
(4)反应中被氧化产生了11.2L(标准状况)的气体时,被还原的物质的质量为 。
(每个方程式2分,其余每空1分,共8分)现有下列物质:①KI ②铜 ③稀硝酸 ④NH3 ⑤NaHSO4 ⑥Ba(OH)2 ⑦氢氧化铁胶体 ⑧氨水
(1)按物质的分类方法填写表格的空白处(填物质编号)
| 分类标准 |
电解质 |
盐 |
非电解质 |
混合物 |
| 属于该类的物质 |
|
|
|
|
(2)上述某两种物质在溶液中可发生离子反应:H++OH-= H2O,写出该离子反应对应的化学方程式 。
(3)物质①的稀溶液在空气中被氧化,加入淀粉溶液显蓝色,则反应的离子方程式为 。
A、B、C、D、E、F、G、H、和I是中学化学中常见的气体,它们均由短周期元素组成,具有如下性质:
①A、B、E、F、G能使湿润的蓝色石蕊试纸变红,I能使湿润的红色石蕊试纸变蓝,C、D、H不能使 湿润的石蕊试纸变色;
②A和I相遇产生白烟
③B和E都能使品红溶液褪色
④将红热的铜丝放入装有B的瓶中,瓶内充满棕黄色的烟
⑤ 将点燃的镁条放入装有F的瓶中,镁条剧烈燃烧,生成白色粉末,瓶内壁附着黑色颗粒;
⑥ C和D相遇生成红棕色气体;
⑦ G在D中燃烧可以产生E和H2O
⑧ 将B和H 在瓶中混合后于光亮处放置几分钟,瓶内壁出现油状液滴并产生A。
回答下列问题:
(1)A的化学式是 ,②中白烟的化学式是 ;
(2) ④中发生反应的化学方程式是 ;
(3)⑤中发生反应的化学方程式是 ;
(4)C的化学式是 ,D的电子式是 ;
(5) ⑦中发生反应的化学方程式是 ;
(6) H的结构式是
1.52g铜镁合金完全溶解于50mL密度为1.40g·mL-1、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL(标准状况),向反应后的溶液中加入1.0mol·L-1NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀。
(1)该合金中铜与镁的物质的量之比是 。
(2)NO2和N2O4的混合气体中,NO2的体积分数是 。
(3)得到2.54 g沉淀时,加入NaOH溶液的体积是 mL。
a、b、c、d、e是含有一种相同元素的五种物质,可发生如图所示的转化。其中: a是单质;c、d是氧化物;e是最高价氧化物对应的水化物。
(1)如果a是淡黄色固体、b是臭鸡蛋气味的气体。则a的化学式为 ,b、e的名称分别为 、c变d的化学方程式为 。
(2)如果a是空气中含量最大的气体、b为气态氢化物,d是红棕色气体。则c的化学式为 ;a生成b的化学方程式为 ;d生成e的离子方程式为 。
某氮肥厂氨氮废水中氮元素多以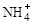 和NH3·H2O的形式存在,该废水的处理流程如下:
和NH3·H2O的形式存在,该废水的处理流程如下: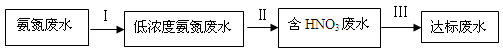
(1)过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30 ℃,通空气将氨赶出并回收。用离子方程式表示加NaOH溶液的作用: 。
(2)过程Ⅱ:在微生物作用的条件下,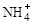 经过两步反应被氧化成
经过两步反应被氧化成 。其中第一步反应的能量变化示意图如下:
。其中第一步反应的能量变化示意图如下: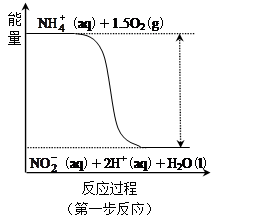
第一步反应是 反应(选填“放热”或“吸热”),判断依据是
(3)过程Ⅲ:一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该反应消耗32 g CH3OH转移6 mol电子,则参加反应的还原剂和氧化剂的物质的量之比是 。
已知X、Y、Z三种元素都属于1~18号元素,它们的核电荷数依次递增,X原子的电子层数与它的核外电子总数相同,而Z原子的最外层电子数是次外层电子数的3倍,Y和Z形成的单质都是自然界循环的两种气体,且Y和Z可以形成两种以上的气态化合物,则;
(1)X、Y、Z的元素名称分别为_______ , ________ , ________
(2)有Y和Z组成,且Y和Z的质量比为7:16的化合物的化学式为________ 或_________
(3)有X、Y、Z中的两种元素组成,且与X2Z分子具有的电子数的两种离子是______和_____
(4)X、Y、Z三种元素可以形成一种盐,此盐中X、Y、Z元素原子的个数比为4︰2︰3,该的化学式是_______
(实验班做,12分)
I. 臭氧层是地球生命的保护神,臭氧比氧气气具有更强的氧化性。实验室可将氧气通过高温放电管来制取臭氧:3O2  2O3 。
2O3 。
(1)若在上述反应中有40%的氧气转化为臭氧,所得混合气体的平均摩尔质量为__________g/mol。(保留一位小数)
(2)将9L氧气通过高压放电管后,恢复到原状况,得到气体6.5L,其中臭氧为________L。
(3)实验室将氧气和臭氧的混合气体1.568L(标准状况)通入盛有20.0g铜粉的反应器中,充分反应后,粉末质量变为23.2g。则原混合气体中臭氧的体积分数为________。(保留一位小数)。
II.将1.28g铜片投入足量硝酸溶液中充分反应,铜片溶解,溶液变蓝,同时收集到一定量混合气体。经测定,该混合气体中含有N2O,NO2,N2O4,NO四种成分,将该混合气体与足量空气混合,同时通入足量NaOH溶液中,氮氧化物完全被吸收,生成NaNO3。则空气中参与反应的O2的物质的量为__________。
完成下列各题:
(1)在18.6g Fe和Zn合金中加入200mL某浓度的稀硫酸恰好完全反应,生成0.3mol H2。则原合金中有 mol Fe,稀硫酸的物质的量浓度为 mol/L。
(2)已知19.2gCu与过量的200ml 5mol/L稀硝酸充分反应,反应方程式如下,请计算(忽略反应前后溶液体积的变化)。
3Cu+8HNO3 加热 3Cu(NO3)2+2NO↑+4H2O
转移电子的个数为 (用NA表示阿伏加德罗常数);标准状况下,产生NO气体的体积为 。
反应后,H+的物质的量浓度为 ,NO3-的物质的量浓度为 。
在下图所示的物质转化关系中(部分反应条件及产物省略),化合物A由短周期元素组成,B是常见的无色液体,C是能使湿润的红色石蕊试纸变蓝色的气体,E是淡黄色粉末,D、F、G均为无色气体。
完成下列问题:
(1)写出A的化学式 。
(2)组成F的元素在周期表中位于 周期 族。
(3)B的电子式是 。
(4)反应①的化学方程式: 。
(5)反应②的离子方程式: 。
A~H等8种物质存在如下转化关系(反应条件、部分产物未标出)。已知A是正盐,B是能使品红溶液褪色的气体,G是红棕色气体。按要求回答问题:
(1)写出下列物质的化学式:A ,B 。
(2)写出下列反应的化学方程式:E→F ;
写出下列反应的离子方程式:A→E ;
H的浓溶液与木炭反应的化学方程式: 。
(3)检验某溶液中是否含D中阴离子的方法是 。
(12分)一定条件下经不同的化学反应,可以实现图示变化,A为酸式盐;B为无色无味气体;无色气体D可使红色石蕊试纸变蓝:X、F和Y为气体单负,且Y为有色气体,F为空气的主要成分之一;G为正盐,G和无色气体M在溶液中可反应生成B。
(1)写出下列物质的化学式:A______________;Y______________
(2)写出反应②的离子方程式______________________________________。
(3)写出反应③的化学方程式______________________________________。
(4)常温下pH=10,体积均为100mL的D、W两溶液与M反应,消耗的M的物质的量关系D____________ W(填“大于”“小于”或“等于”)。
(13分)X、Y、Z、W、G、和H均由短周期元素组成,它们是中学化学中常见的气体,具有如下性质:
①X、Y、G能使湿润的蓝色石蕊试纸变红,H能使湿润的红色石蕊试纸变蓝,Z、W不能使湿润的石蕊试纸变色;
②X和H相遇产生白烟;
③Y是形成酸雨的主要气体且能使品红溶液褪色;
④Z和W相遇生成红棕色气体;
⑤G在W中燃烧可以产生Y和H2O;⑥回答下列问题:
(1) H的化学式是__________,实验室制取H的化学反应方程式是___________________________;
(2)Z的化学式是________,W的化学式是__________________;
(3)⑤中发生反应的化学方程式是___________________________________________;
(4)实验室制备、收集干燥的Y气体,所需仪器如下。装置A产生Y气体,按气流方向连接各仪器接口,顺序为a



 f:装置D的作用是 ,装置E中NaOH溶液的作用是 。
f:装置D的作用是 ,装置E中NaOH溶液的作用是 。
(10分) 1.92gCu片与一定量的浓HNO3作用,当收集到NO2和NO气体共1.12L时(标准状况),金属铜恰好全部作用。则:
(1)反应中消耗HNO3______mol,转移电子______mol。
(2)用排水法收集生成的气体,最后气体的体积为 L。(标况)
(3)向收集到的气体中通入 ml O2(标况)才能使水刚好充满整个集气容器。
1.92gCu片与一定量的浓HNO3作用,当收集到NO2和NO气体共1.12L时(标准状况),金属铜恰好全部作用。则:
(1)反应中消耗HNO3 mol,转移电子 mol
(2)用排水法收集生成的气体,最后气体的体积为 L (标准状况)
(3)向收集到的气体中通入 mL O2(标准状况)才能使水刚好充满整个集气容器。
试题篮
()