(9分)在下列物质转化中,已知A是一种正盐,D的相对分子质量比C的相对分子质量大16,E是酸;当X无论是强酸还是强碱时,都有如下的转化关系:
说明:当X是强酸时A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外同一种元素。(已知H2CO3、H2S、H2SO3、H2SiO3皆为二元弱酸)
请回答下列问题:
(1)A是 ,Y是 ,Z是 (填化学式,下同)。
(2)当X是强酸时,E是 ,写出B生成C的化学方程式: _____ 。
(3)当X是强碱时,E是 ,写出D生成E的离子方程式: _____。
围绕下列七种物质:①铝、②A12O3、③稀硝酸、④H2SO4、⑤Ba(OH)2固体、⑥稀氨水、⑦A12(SO4)3,根据要求回答下列问题。
(1)既能与强酸反应,又能与强碱反应的是 (填序号)。
(2)属于电解质的是 (填序号)。
(3)写出最适宜制取Al(OH)3的离子方程式: 。
(4)两物质间发生反应的离子方程式为H++OH-= H2O,请写出该反应的化学方程式: 。
(5)34.2g⑦溶于水配成500mL溶液,则溶液中SO42-的物质的量浓度为 。
海藻中富含碘元素。某小组同学在实验室里用灼烧海藻的灰分提取碘,流程如下图。
(1)写出操作名称:操作① ,操作③ 。
(2)用NaOH浓溶液反萃取后再加稀酸,可以分离I2和CCl4。有关化学方程式为:
碱性条件,3I2+6NaOH=5NaI+NaIO3+3H2O,
酸性条件,5NaI+NaIO3+3H2SO4=3Na2SO4+3I2+H2O。
以下是反萃取过程的操作,请填写相关空格:
①向装有I2的CCl4溶液的 (填仪器名称)中加入少量1mol·L-1 NaOH溶液;
②振荡至溶液的 色消失,静置、分层,则 (填“上”、“下”)层为CCl4;
③将含碘的碱溶液从仪器的 (填“上”、“下”)口倒入烧杯中;
④边搅拌边加入几滴1 mol·L-1 H2SO4溶液,溶液立即转为棕黄色,并析出碘晶体;
(3)本实验中可以循环利用的物质是 。
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,其中物质E是气体丙的水溶液,物质H是红褐色沉淀。它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:
(1)写出A、C、丙的化学式:
A 、 C 、 丙
(2)写出反应③的化学方程式: ,
反应⑤的离子方程式: 。
甲、乙、丙、X是中学化学中常见的物质,在一定条件下,它们之间的转化关系如下图所示(部分产物已略去)。请回答下列问题: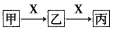
(1)若X是 O2,则甲不可能是______(填代号)
a.Mg b.N2 c.S d.Al
(2)若甲能使湿润的红色石蕊试纸变蓝,丙为红棕色气体。写出甲转化为乙的化学方程式:________________________________________。
(3)若乙是一种常见的温室气体,则X的化学式为__________。
(4)若丙为淡黄色粉末,常用作呼吸面具中的供氧剂,则丙与水反应的离子方程式为______;1mol丙与水发生反应时转移电子的物质的量为______mol。
(5)若X是一种常见的金属单质,常温下甲的浓溶液可盛放在铝制容器中,丙为浅绿色溶液。
①检验乙是否完全转化为丙的试剂为_______(填试剂名称)。
②保存丙溶液常加入少量X,其目的是____________。
如图所示:丁可能是强酸也可能是强碱。
(1)若丙是潜艇的供氧剂,请写出甲与水反应的离子方程式 ;若等物质的量的甲,乙,丙,丁的固体投入到足量且等量的水中完全反应所得溶液的质量分数由大到小的顺序是 (用化学式表示)。
(2)若乙是能使品红溶液褪色的气体,请写出乙→丙的化学反应方程式 ;请写出乙可使氯水褪色的离子方程式__________________________.
(3)若甲可作为制冷剂,请写出甲→乙的化学反应方程式 ;将等量的铜粉分别与过量浓的丁溶液、稀的丁溶液反应,消耗丁的物质的量:前者 后者,反应中转移的电子总数:前者 后者(填“>”、“=”或“<”)
某学生课外活动小组利用下图所示装置分别做如下实验:
(1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是 溶液;加热时溶液由红色逐渐变浅的原因是 。(用化学反应方程式表示)
(2)在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是 溶液;加热时溶液由无色变为红色的原因 。
已知两种相邻周期、相邻主族的短周期非金属元素X、Y,其最高价氧化物的水化物均为强酸。根据下图转化关系(反应条件及部分产物已略去),回答下列问题:
(1)若A、B、C、D均为含X元素的化合物,且A和F的分子均为10电子微粒,则:
①F属于____________(填“离子化合物”或“共价化合物”)。
②反应I的化学方程式为____________________________________________。
③将1.92g铜粉与一定量的D的浓溶液反应,当铜粉完全反应时收集到气体1.12L(标准状况),则反应消耗的D的物质的量为________________mol。
(2)若A、B、C、D均为含Y元素的化合物,其中A由两种元素组成,且A的摩尔质量为34g mol
mol ,则:
,则:
①将铜粉与D的浓溶液反应所得溶液加热蒸干,得到的白色固体物质为_______(填化学式)。
②将少量Na2Y溶液滴加到次氯酸钠溶液中发生反应,无沉淀生成,请写出该反应的离子反应方程式_______________________。在该反应中若有74.5 g NaClO被还原,则转移电子的物质的量为_________mol。
已知甲、乙、丙为常见的单质,A、B、C、D、X、Y、Z为常见化合物,且丙在常温常压下为气体,B为淡黄色固体,Y的摩尔质量数值比Z小16,乙、丙的摩尔质量相同,B的摩尔质量比D小2,B、X的摩尔质量相同。各物质之间的转化关系如图所示(各反应条件略)。
请回答:
(1)在B与二氧化碳的反应中,每有1mol电子转移,生成气体 L(标准状况)。
(2)X与Y的溶液混合后,再加入适量盐酸,会有乙生成,反应的离子方程式是 。
(3)将C通入溴水中,所发生反应的离子方程式是 。D中含的化学键类型为 。
(4)在101KPa时,4.0g乙在一定条件下与丙完全反应生成C,放出37KJ的热量,该反应的热化学方程式 是
(5)比甲元素的原子序数少4的M元素,在一定条件下能与氢元素组成化合物MH5。已知MH5的结构与氯化铵相似,MH5与水作用有氢气生成,则MH5的电子式为 (M要用元素符号表示)。写出MH5与AlCl3溶液反应的化学方程式
A、B、C、D均为中学化学常见的纯净物,A是单质,它们有如图反应关系。根据要求回答问题:
(1)若A是大气中含量最多的气体,C、D是氧化物且会造成光化学污染。写出D转化成C的反应化学方程式 。
(2)若A、B、C分别为C(s)、CO(g)和CO2(g),且通过与O2(g)反应实现图示的转化。在同温同压且消耗含碳物质均为1mol时,反应①、②、③的焓变依次为△H 1、△H 2、△H 3,则它们之间的关系为_______________________(用含△H 1、△H 2、△H 3的代数式表示)
(3)若C为一元强碱且阴、阳离子所含的电子数相同,D为日常生活中常用的调味品,请写出工业上用D制备A的化学方程式__________________________。
(4)若A是应用最广泛的金属。④反应用到A,②、⑤反应均用到同一种气态非金属单质。请简要说明实验室保存D溶液的方法 。
(14分)X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如下图所示(水及部分产物已略去)。
(1)若X为金属单质,W是某强酸的稀溶液。X与过量W反应生成Y的离子方程式为_________。向Z溶液中加入某种试剂_______(填试剂名称或化学式),若出现蓝色沉淀,即可判断Z溶液中阳离子的存在。
(2)若X为非金属单质,W是空气的主要成分之一。它们之间转化的能量变化如图A所示,则X+W→Z的热化学方程式为_______。
(3)若X、Y为正盐,X的水溶液显酸性,W为一元强碱(化学式为MOH),Z的电离方程式为_______。室温下,若用0.1 mol/L的W溶液滴定V mL 0.1 mol/L HA溶液,滴定曲线如图B所示,则a、b、c、d四点溶液中水的电离程度最大的是______点;a点溶液中离子浓度的大小顺序为______________;取少量c点溶液于试管中,再滴加0.1 mol/L盐酸至中性,此时溶液中除H+、OH-外,离子浓度的大小顺序为______________。
(4)若X为强碱,常温下W为有刺激性气味的气态氧化物。常温时,将Z的水溶液露置于空气中,请在图C中画出其pH随时间(t)的变化趋势曲线图(不考虑水的挥发)。
X~R是元素周期表中的短周期元素,其性质或结构信息如下表:
| 元素 |
X |
Y |
Z |
W |
R |
| 性质 信息 |
能形成+7价的化合物 |
日常生活中常见金属,熔化时并不滴落,好象有一层膜兜着 |
通常状况下能形成短周期中最稳定的双原子分子 |
焰色反应为黄色 |
位于第IVA,是形成化合物种类最多的元素 |
请用化学用语回答下列问题:
(1)X在元素周期表中的位置是_________________________。
(2)元素W的离子结构示意图为_______________________。
(3)元素R的最高价氧化物的电子式为_________________。
(4)X的氢化物和Z的氢化物反应形成化合物A,A中含有的化学键类型为① ,② 。
(5)含Y的某化合物可用作净水剂,该物质的水溶液呈酸性,其原因是 。(用离子方程式表示)
(6)W的氢氧化物是重要的基本化工原料。写出工业上制取该氢氧化物的离子反应方程式 。
(1)由CO、CO2组成的混合气体36g,其中含C原子数为NA个,则C、O原子个数比为_______;用过氧化钠吸收CO2制氧气的化学方程式是___________________________;
(2)化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
①当酸足量时,“三酸”与“两碱”之间共可发生六个化学反应,用两个离子方程式即可表达这六个反应的本质,这两个离子方程式是:____________、____________。
②“三酸”常用于溶解金属和金属氧化物。下列块状金属在常温时能全部溶于足量浓硝酸的是________。
A.Fe B.Cu C.Al D.Pt
(3)第三周期元素中,离子半径最小的离子是____(写符号),得电子能力最强的原子是___(写符号)。
除去下列物质中所含有的杂质(括号内为杂质),将选用的试剂及分离方法填在题后的横线上,涉及化学反应的并写出有关反应的化学方程式(是离子反应的,写出其离子方程式)。
(1)Fe2O3[Fe(OH)3]____ ____,______ ____________;
(2)FeCl3溶液(FeCl2)____ ____,_______ _______________;
(3)Fe(Al) ___,__ _____________________。
(4)CO2(SO2) , 。
(5)SiO2(Al2O3) , 。
(6)淀粉溶液(氯化钠) 。
(7)KNO3(NaCl) 。
(8)Br2(H2O) 。
试题篮
()