下列各组物质相互作用,生成物不随反应条件或反应物的用量变化而变化的是( )
| A.Na和O2 | B.NaOH和CO2 | C.NaHCO3和NaOH | D.Na2CO3和HCl |
同物质的量浓度下列溶液 ①  ②Na2CO3③CH3COONa ④NaOH ⑤H2SO4
②Na2CO3③CH3COONa ④NaOH ⑤H2SO4
⑥HCl ⑦Ba(OH)2⑧KCl,这八种溶液对水电离程度的影响由大到小的顺序正确的是:
| A.②>①>③>⑧>④=⑥>⑤=⑦ | B.②>①>③>⑧>④>⑥>⑤>⑦ |
| C.①>②>③>⑧>④=⑥>⑤=⑦ | D.②>①>③>⑧>⑤=⑦>④=⑥ |
将硫酸钾、硫酸铝、硫酸钾铝三种盐混合溶于硫酸酸化的水中,测得c(SO42-)=0.105 mol·L-1、c(Al3+)=0.055mol·L-1,c(H+)="0.01" mol·L-1 (假设溶液中硫酸完全电离为H+和SO42-),则c(K+)为 ( )
| A.0.045mol·L-1 | B.0.035mol·L-1 | C.0.055mol·L-1 | D.0.040mol·L-1 |
在氯化铵溶液中,下列关系式正确的是
| A.C(Cl-)>C(NH4+)>C(H+)>C(OH-) | B.C(NH4+)>C(Cl-)>C(H+)>CC(OH-) |
| C.C(Cl-)=C(NH4+)>C(H+)=C(OH-) | D.C(NH4+)=C(Cl-)>C(H+)>C(OH-) |
用物质的量都是0.1 mol的CH3COOH和CH3COONa配制成1L混合溶液,已知其中C(CH3COO-)>C(Na+),对该混合溶液的下列判断正确的是( )
| A.C(H+)>C(OH-) | B.C(CH3COOH)+C(CH3COO-)=0.2 mol/L |
| C.C(CH3COOH)>C(CH3COO-) | D.C(CH3COO-)+C(OH-)=0.2 mol/L |
在0.1 mol/l的NH3·H2O溶液中,下列关系正确的是
| A.C(NH3·H2O)>C(OH-)>C(NH4+)>C(H+) | B.C(NH4+)>C(NH3·H2O)>C(OH-)>C(H+) |
| C.C(NH3·H2O)>C(NH4+)=C(OH-)>C(H+) | D.C(NH3·H2O)>C(NH4+)>C(H+)>C(OH-) |
某碱性溶液中只有Na+、CH3COO-、H+、OH-四种离子。则下列描述正确的是( )
| A.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈蓝色 |
| B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成 |
| C.在NaOH溶液中加入一定量的CH3COOH溶液,只有当溶液中离子浓度满足: c(Na+)>c(CH3COO-)>c(OH-)>c(H+)时,才符合题意。 |
| D.加入适量氨水,c(CH3COO-)一定大于c(Na+)、c(NH4+)之和 |
下列关于电解质溶液的叙述正确的是 ( )
A.常温下,Ph=7的NH4Cl与氨水的混合溶液中离子浓度大小顺序为:   |
B.将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
C.室温下,CH3COOH分子可存在于pH=8的碱性溶液中 |
D.常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
将等浓度的K2S溶液和NaHSO4溶液等体积混合,得到的溶液中离子浓度关系正确的是
A.c(K+)>c(Na+)>c(H+)>c(OH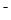 ) ) |
B.c(Na+)+c(K+)+c(H+)=c(SO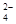 )+c(HS )+c(HS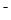 )+c(OH )+c(OH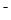 )+c(S2一) )+c(S2一) |
C.c(SO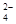 )>c(HS )>c(HS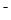 )>c(OH )>c(OH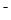 )>c(H+) )>c(H+) |
D.c(K+)=c(S2一)+c(H2S)+c(HS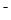 )+c(SO )+c(SO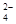 ) ) |
:已知一种c(H+)=1×10-3mol·L-1的酸和一种c(OH— )= 1×10-3 mol· L-1碱溶液等体积混合后,溶液呈酸性。其原因可能是 ( )
A.浓的强酸和稀的强碱溶液反应 B.浓的弱酸和稀的强碱溶液反应
C.等浓度的强酸和弱碱溶液反应 D.生成了一种强酸弱碱盐
分析:题中两溶液中的c(H+)= c(OH— ),采用中和假想法,若是强酸强碱等体积混合,溶液一定呈中性。现溶液呈酸性,说明酸过量,且必须是弱酸。以此得答案B。
注意:中和反应后溶液的酸碱性由两方面决定。该题给出c(H+)= c(OH—),故应从酸碱用量考虑。如未理解题意,极易从盐的水解进行分析,故易错选C、D。
试题篮
()