下列说法正确的是
A.向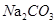 溶液通入 溶液通入 ,可使水解平衡: ,可使水解平衡: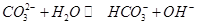 向正反应方向移动,则溶液pH增大 向正反应方向移动,则溶液pH增大 |
B.室温时,0.1mol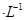 某一元酸HA在水中有0.1%发生电离,则该溶液的pH=4 某一元酸HA在水中有0.1%发生电离,则该溶液的pH=4 |
C.25℃时,pH=13的1.0 L Ba 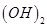 溶液中含有的 溶液中含有的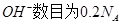 |
| D.用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH |
下列有关溶液中离子浓度的关系,不正确的是
| A.NaHCO3溶液中存在:c(OH-)=c(H2CO3)+c(H+) |
| B.常温下,pH=3的盐酸和pH=ll的氨水等体积混合后,溶液中:c(NH4+)>c(Cl-) |
| C.0.2 mol/LNH4Cl溶液与0.1 mol/L NaOH溶液等体积混合后,溶液中:c(NH4+)>c(Na+) |
| D.0.2 mol/L 的 CH3COOH 溶液中c(H+)小于0.1 mol/L 的 CH3COOH 中c(H+)的两倍 |
25℃时,浓度均为0.2 mol/L的NaHCO3溶液中,下列判断不正确的是 ( )
A.存在电离平衡HCO H++CO32— H++CO32— |
B.存在水解平衡HCO+H2O H2CO3+OH- H2CO3+OH- |
| C.将溶液加热蒸干、灼烧得Na2O2固体 |
| D.加入NaOH固体,恢复到原温度,c(OH-)、c(CO32—)均增大 |
下列电解质溶液的有关叙述正确的是
| A.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7 |
| B.在含有BaSO4沉淀的溶液中加入K2SO4固体,c(Ba2+)增大 |
| C.含l mol KOH的溶液与l mol CO2完全反应后,溶液中c(K+)>c(HCO3-) |
| D.在(NH4)2SO4溶液中加入适量H2SO4,可使c(NH4+)=2c(SO42-) |
25℃时,0.1 mol·L-1的下列溶液中,有关粒子的物质的量浓度关系正确的是( )
| A.CH3COONa溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| B.Na2S溶液:c(OH-)=c(H+)+c(HS-)+c(H2S) |
| C.NH4Fe(SO4)2溶液:c(OH-)+2c(SO42-)=c(H+)+c(NH4+)+3c(Fe3+) |
| D.NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
下列溶液中,各离子浓度的大小顺序正确的是 ( )
| A.10 mL 0.1 mol·L-1盐酸,c(Cl-)>c(OH-)>c(H+) |
B.10 mL 0.1 mol·L-1氨水,c(OH-)>c(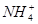 )>c(H+) )>c(H+) |
| C.5 mL 0.2 mol·L-1NaOH溶液,c(Na+)>c(OH-)>c(H+) |
| D.10 mL 0.5 mol·L-1NaOH溶液与6 mL 1 mol·L-1盐酸混合,c(Cl-)>c(Na+)>c(OH-)>c(H+) |
下列说法错误的是
| A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH小于4 |
| B.为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| C.用0.200 mol·L-1 NaOH标准溶液滴定HCl与CH3COOH的混合液(混合液中两种酸的浓度均约为0.1 mol·L-1),至中性时,溶液中的酸未被完全中和 |
| D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol·L-1盐酸、③0.1 mol·L-1氯化镁溶液、④0.1 mol·L-1硝酸银溶液中,Ag+浓度: ④>①>②>③ |
在T ℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g/cm3,溶质的质量分数为w,其中含NH4+的物质的量为b mol。下列叙述中正确的是( )
A.溶质的质量分数为w= ×100% ×100% |
B.溶质的物质的量浓度c= mol/L mol/L |
C.溶液中c(OH-)= mol/L mol/L |
| D.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w |
将pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合后,下列关系式中正确的是
| A.c(Na+)=c(CH3COO-)+c(CH3COOH) | B.c(H+)=c(CH3COO-)+c(OH-) |
| C.c(Na+)>(CH3COO-)>c(OH-)>c(H+) | D.c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
下列关于电解质溶液说法正确的是 ( )
| A.水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应 |
| B.等体积的pH都为3的酸HA和HB分别与足量的Mg反应,HA放出的H2多,说明酸性:HA>HB |
| C.常温下,弱酸酸式盐NaHA溶液的pH=6,说明HA‾的电离程度大于其水解程度 |
| D.pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度相同 |
下列叙述正确的是
| A.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合: 2c(Na+) + c(CH3COOH) = c(CH3COO-) +2c(OH-) |
| B.Ksp(AgCl)>Ksp(AgI)由此可以判断AgCl(S) + I- = AgI(S) + Cl-能够发生 |
| C.氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-) |
| D.中和浓度与体积均相等的盐酸和醋酸溶液,消耗NaOH的物质的量不相等 |
常温下,向0.25 mol·L-1的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液,下列有关说法中正确的是
| A.硫酸溶液的体积为30 mL |
| B.b时刻溶液中SO42-的浓度约为0.125 mol·L-1 |
| C.d时刻溶液的pH约为13 |
| D.溶液的导电能力:c<d=b<a |
下列各项中的两个量,其比例2:1的是( )
| A.硫酸铵固体中n(NH4+)与n(SO42—) |
| B.相同温度下,0.01 mol/L的醋酸溶液与0.02 mol/L 醋酸溶液中的c(H+) |
| C.液面均在“0”刻度时,50 mL酸式滴定管和25 mL酸式滴定管内所盛溶液的体积 |
| D.40℃时pH=7的(NH4)2SO4与NH3·H2O的混合液中,c(NH4+)与c(SO42—) |
试题篮
()