常温下,将一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的 pH如下表:
下列判断正确的是 ( )
| A.a>9 |
| B.在乙组混合液中由水电离出的c(OH-)=10-5mol·L-1 |
| C.c1=0.2 |
| D.丁组混合液:c(Na+)>c(A-)>c(H+)>c(OH-) |
下列关于氯水的叙述正确的是( )
| A.氯水中只存在一种电离平衡 |
| B.向氯水中通入SO2,其漂白性增强 |
| C.向饱和氯水中通入氯气,c(H+)/c(ClO一)减小 |
| D.向氯水中加入NaOH至中性,溶液中c(Na+)=c(Cl一)+c(CIO一) |
将1mol·L-1H2SO4溶液100mL与质量分数为10%的NaOH溶液50g混合均匀后,滴入甲基橙指示剂,此时溶液的颜色是
| A.浅紫色 | B.黄色 | C.红色 | D.无色 |
常温下,pH=3的一元酸和pH=13的氢氧化钠溶液等体积混合后(不考虑混合后溶液体积的变化),恰好完全反应。下列说法不正确的是
| A.两溶液混合反应后的所得的混合溶液呈碱性 |
| B.所用酸溶液的浓度大于所用氢氧化钠溶液的浓度 |
| C.若酸为醋酸,原醋酸溶液中有1%的醋酸已电离 |
| D.若酸为醋酸,反应后的溶液中CH3OO-与CH3COOH的平衡浓度之和约为0.05mol?L-1 |
下列化学原理表述正确的是
| A.氢硫酸溶液加水稀释,电离程度增大,H+浓度增大; |
| B.Na2CO3溶液中满足:c(Na+)=2c( CO32-)+2 c( HCO3-)+ 2c (H2CO3) |
C.NaHCO3溶液不显中性的原因:HCO3-+H2O CO32-+H3O+ CO32-+H3O+ |
| D.同体积同pH的盐酸和醋酸,与足量的锌反应,盐酸的反应速率快,生成H2的物质的量多; |
下列液体均处于25 ℃,有关叙述正确的是( )
| A.Na2CO3溶液中,c(OH-)-c(H+)=c(HCO3-) +2c(H2CO3) |
| B.AgCl在同浓度的MgCl2和KCl溶液中的溶解度相同 |
| C.将稀氨水逐滴加入稀硫酸中,当溶液pH =7时,c(SO42-) >c(NH4+) |
| D.Na2S溶液加水稀释后,恢复至原温度,pH和Kw均减小 |
下列说法正确的是
①常温下,强酸溶液的pH=a,将溶液的体积稀释到原来10n倍,则pH=a+n;
②已知BaS04的Ksp=c(Ba2+)·c(SO42-),所以在BaS04溶液中有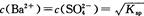
③将O.1 mol/l的NaHS溶液和O.1 mol/lNa2S溶液等体积混合,所得溶液中有2c(OH-)+c(S2-)= 2c(H+)+ c(HS-)+3 c(H2S);
④在O.1 mol/l氨水中滴加O.1 mol/l盐酸,刚好完全中和时pH=a,则由水电离产生的c (OH-)=10-amol·L-1
| A.①④ | B.②③ | C.③④ | D.①② |
从下列事实所引出的相应结论,正确的是
| 选项 |
实验事实 |
结论 |
| A |
等体积pH同为3的酸HA和酸HB与足量Zn反应,酸HA放出氢气多 |
酸性:HA > HB |
| B |
Na2SO4溶液的pH小于Na2CO3溶液的pH |
非金属性:S > C |
| C |
电解同浓度的A2+和B2+硝酸盐的混合溶液,A先析出 |
金属性:A > B |
| D |
由M、N与稀硫酸构成的原电池中,M上产生大量气泡 |
金属性:M > N |
下图为Na2SO4的溶解度曲线,已知硫酸钠晶体(Na2SO4·10H2O)在温度为T3 K 时开始分解为无水硫酸钠。现有142 g温度为T2 K的饱和硫酸钠溶液,当温度降为T1 K或升为T4 K(T4>T3)时析出晶体的质量相等,则温度为T4 K时Na2SO4的溶解度为
| A.小于40g | B.等于40g | C.等于42g | D.大于42g |
下列液体均处于25 ℃,有关叙述正确的是 ( )。
| A.某物质溶液的pH>7,则该物质一定是碱或强碱弱酸盐 |
| B.pH=6.5的牛奶中c(H+)是pH=4.5的H2SO4溶液中c(H+)的100倍 |
| C.pH=3的醋酸与pH=11的NaOH溶液等体积混合后溶液中: c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| D.AgCl在等浓度的CaCl2溶液和NaCl溶液中的溶解度相同 |
化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是( )
A.根据图①可判断可逆反应A2(g)+3B2(g)  2AB3(g)的△H>O 2AB3(g)的△H>O |
B.图②表示压强对可逆反应2A(g)+2B(g)  3C(g)+D(s)的影响,乙曲线表示的压强大 3C(g)+D(s)的影响,乙曲线表示的压强大 |
| C.图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
| D.室温时,CaC03在水中的沉淀溶解平衡曲线如图④所示,c点时有CaC03生成 |
下列说法正确的是( )
| A.向0.1 mol/L Na2CO3溶液中滴加酚酞,溶液变红色 |
| B.Al3+、NO3-、Cl-、CO32-、Na+可大量共存于pH=2的溶液中 |
| C.乙醇和乙酸都能溶于水,都是电解质 |
| D.分别与等物质的量的HCl和H2SO4反应时,消耗NaOH的物质的量相同 |
有关电解质的下列叙述正确的是 ( )
| A.离子化合物熔融状态时都导电,因此离子化合物都是电解质 |
| B.共价化合物熔融状态时都不导电,因此共价化合物都是非电解质 |
| C.易溶于水的化合物都是强电解质 |
| D.强电解质溶液的导电能力一定强 |
将一元碱BOH的溶液与一元酸HA的溶液等体积混合,若所得溶液呈碱性,下列有关判断正确的是
| A.若混合前酸、碱pH之和等于14,则HA肯定是弱酸 |
| B.若混合前酸、碱物质的量浓度相同,则HA肯定是弱酸 |
| C.溶液中水的电离程度:混合溶液>纯水>BOH溶液 |
| D.混合溶液中离子浓度一定满足:c(B+)>c(A—)>c(H+)>c(OH—) |
下列有关说法中正确的是( )
| A.常温下,将1 L pH=12的氨水加水稀释为10 L后溶液的pH=11 |
| B.有甲、乙两醋酸溶液,测得甲的pH=a,乙的pH=a+1,若用于中和等物质的量浓度等体积的NaOH溶液,需甲、乙两酸的体积V (乙)>10V(甲) |
C.向浓度均为0.1 mol·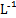 的MgCl2、CuCl2混合溶液中逐滴加入氨水,先生成蓝色沉淀,说明Ksp[Cu(OH)2]>Ksp[Mg(OH)2] 的MgCl2、CuCl2混合溶液中逐滴加入氨水,先生成蓝色沉淀,说明Ksp[Cu(OH)2]>Ksp[Mg(OH)2] |
| D.水的离子积常数KW随着温度的升高而增大,说明水的电离是放热反应 |
试题篮
()