下列说法正确的是
A 向饱和食盐水中通入HCl气体,看不到明显的现象
B将硫酸铜溶液与碳酸钠溶液混合,得到的沉淀以Cu(OH)2为主,说明了在相同条件下Cu(OH)2的溶解度比CuCO3的更小
C 在滴有酚酞溶液的氨水中,加入NH4Cl至溶液恰好无色,则此时溶液的pH=7
D.25℃时NH4Cl溶液的Kw大于100℃时NaCl溶液的Kw
下表是五种银盐的溶度积常数Ksp(25℃),下列说法不正确的是
| 化学式 |
AgCl |
Ag2SO4 |
Ag2S |
AgBr |
AgI |
| 溶度积 |
1.4×10-10 |
1.4×10-5 |
6.3×10-50 |
7.7×10-13 |
8.51×10-16 |
A.25℃时五种银盐的饱和溶液中,c(Ag+)最大的是Ag2SO4溶液
B.在氯化银的悬浊液中加入Na2S溶液可以生成黑色的Ag2S
C.25℃时,在等物质的量浓度的NaCl、CaCl2两溶液中加入足量的AgCl固体形成饱和溶液,则两溶液中AgCl的溶度积相同,且两溶液中c(Ag+)也相同
D.AgBr沉淀可以转化成AgI沉淀,而 AgI沉淀在一定条件下也可以转化成AgBr沉淀
常温下,下列溶液中的微粒浓度关系正确的是
常温下甲、乙两醋酸溶液,测得甲的pH= a,乙的pH= a+1
下列推断中正确的是( )
| A.甲中由水电离产生的H+的物质的量浓度是乙的0.1倍 |
| B.物质的量浓度c(甲)=10c(乙) |
| C.中和等物质的量的NaOH溶液,需甲、乙两酸的体积V(乙)>10V(甲) |
| D.甲中的c(OH-)为乙中的c(OH-)的10倍 |
下列各项中的两个量,其比例2:1的是( )
| A.硫酸铵固体中n(NH4+)与n(SO42—) |
| B.相同温度下,0.01 mol/L的醋酸溶液与0.02 mol/L 醋酸溶液中的c(H+) |
| C.液面均在“0”刻度时,50 mL酸式滴定管和25 mL酸式滴定管内所盛溶液的体积 |
| D.40℃时pH=7的(NH4)2SO4与NH3·H2O的混合液中,c(NH4+)与c(SO42—) |
下列说法正确的是
| A.盐溶液不是促进就是抑制水的电离 | B.弱酸对水的抑制作用就比强酸弱得多 |
| C.催化剂能改变可逆反应达到平衡的时间 | D.硫酸氢钠溶液显酸性,是因为电离大于水解 |
下列溶液中c(Cl-)与50 mL 1mol/L 的AlCl3溶液中氯离子浓度相等的是
| A.150 mL 1mol/L NaCl溶液 | B.75 mL 2mol/L NH4Cl溶液 |
| C.75 mL 1mol/L FeCl3溶液 | D.150 mL 2mol/L MgCl2溶液 |
酸碱完全中和时
| A.酸和碱的物质的量一定相等 |
B.酸所提供的H+与碱提供的 的物质的量相等 的物质的量相等 |
| C.酸和碱的物质的量浓度相等 |
| D.溶液一定呈中性 |
下列溶液中微粒浓度关系一定正确的是 ( )
| A.将水加热到120℃,pH=6:c(OH—)< c(H+) |
| B.醋酸与醋酸钠的pH=7的混合溶液中:c(CH3COO—)> c(Na+) |
| C.0.lmoI·L-1的硫酸铵溶液中:c(NH+4)> c(SO2-4)> c(H+) |
| D.pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH—)= c(H+) |
在0.2mol/L的CH3COOH溶液中分别加入下列物质后,有关判断正确的是
| A.适当升高温度,CH3COOH的电离程度减小 |
| B.加少量NaOH固体,CH3COOH 的电离平衡向正方向移动 |
| C.加少量0.1mol/L的HCl溶液,溶液中c(H+)增大平衡向正方向移动 |
| D.加少量CH3COONa固体,CH3COOH 的电离平衡平衡向正方向移动 |
标准状况下,将V L A气体(摩尔质量为M g/mol)溶于0.1 L水中,所得溶液密度为ρ g/mL,则此溶液物质的量浓度为( )
已知25℃时有关弱酸的电离平衡常数:
| 弱酸化学式 |
CH3COOH |
HCN |
H2CO3 |
| 电离平衡常数(25℃) |
1.8×l0-5 |
4.9×l0-10 |
K1=4.3×l0-7 K2=5.6×l0-11 |
根据上述电离常数分析,下列表述不正确的是( )
A.25℃时,等物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(NaHCO3)>pH(CH3COONa)
B.a mol/L HCN溶液与b mol/L NaOH溶液等体积混合后,所得溶液中c(Na+)=c(CN-),则a一定大于b
C.2 NaCN + H2O + CO2 =2 HCN + Na2CO 3
D.2CH3COOH + Na2CO3 → 2 CH3COONa + H2O + CO2 ↑
室温时,向稀醋酸中逐滴加入NaOH溶液,正确的是:
| A.向原醋酸中滴入NaOH溶液,可促进CH3COOH的电离,溶液的pH降低 |
| B.当滴入的NaOH与CH3COOH恰好反应时,所得溶液呈中性 |
C.当两者恰好完全反应时: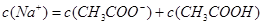 |
D.所得溶液中各离子浓度的关系为: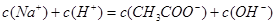 |
下列有关溶液中粒子浓度的关系式中,正确的是
A.pH相同的①CH3COONa、②NaHCO3、③C6H5ONa三份溶液中的c(Na+):③>②>①
B.0.1mol·L-1某二元弱酸强碱盐NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A)
C.下图中pH=7时: c(Na+)>c(CH3COO-) >c(OH-)=c(H+)
D.下图中a点溶液中各离子浓度的关系是:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH)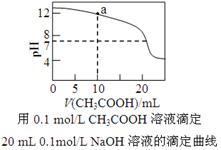
已知25℃时有关弱酸的电离平衡常数:
| 弱酸化学式 |
CH3COOH |
HCN |
H2CO3 |
| 电离平衡常数(25℃) |
1.8×l0–5 |
4.9×l0–10 |
K1=4.3×l0–7 K2=5.6×l0–11 |
则下列有关说法正确的是( )
A、等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B、将a mol·L—1 HCN溶液与a mol·L—1 NaOH溶液等体积混合,混合液中:c(OH–)>c(H+),c(Na+)>c(CN–)
C、冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小
D、NaHCO3和Na2CO3混合液中,一定有c(Na+)+ c(H+)=c(OH–)+ c(HCO3–) +c(CO32–)
试题篮
()