水溶液中存在多种平衡,请回答下列问题。
(1)有下列几种溶液:a. NH3·H2O b. CH3COONa c. NH4Cl d. NaHSO4
常温下呈酸性的溶液有 (填序号)。
(2)已知NaHCO3溶液呈碱性,该溶液中除水的电离外还存在着两个平衡,用电离方程式或离子方程式表示: 、
,该溶液中的离子浓度由大到小的顺序是: 。
(3)有浓度均为0.1 mol•L-1的 ①盐酸②硫酸③醋酸三种溶液,请用序号填空:
三种溶液的c(H+)大小顺序为 ;中和一定量NaOH溶液生成正盐时,需上述三种酸的体积依次的大小关系为 ;若三种溶液的pH都为2,分别取10mL上述溶液加水稀释至1000mL,此时三种溶液的pH的大小关系为 。
(4)25℃时,AgCl的Ksp=1.8×10-10 ,试写出AgCl溶解平衡的表达式: ,现将足量AgCl固体投入100mL0.1mol/L MgCl2溶液充分搅拌后冷却到25℃时,此时c(Ag+)= mol/L(忽略溶液体积的变化)。
下列关于电解质溶液的叙述正确的是
| A.常温下物质的量浓度相等①NH4HSO4、②(NH4)2SO4、③(NH4)2CO3三种溶液中c(NH4+)①<②<③ |
| B.难溶电解质的Ksp越大,其溶解度一定越大 |
| C.常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
| D.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 |
下列溶液中有关粒子的物质的量浓度关系正确的是( )
A.25℃时,pH=4的HCl溶液与pH=4的醋酸溶液中:c(Cl-)=c(CH3COO-)
B.氯水中:2c(Cl2)=c(ClO-)+c(Cl-)+c(HClO)
C.pH=8的0.1mol/L的NaHB溶液中:c(HB-)>c(H+)>c(B2-)>c(H2B)
D.1 mol·L-1的Na2S溶液中: c(OH-)=c(HS-)+c(H2S)+ c(H+)
某溶液中含有Na+、Al3+、NO3-、SO42-(不考虑水中的H+、OH-)四种离子,已知Na+、Al3+、NO3-的个数比为3:2:1,则溶液中Al3+与SO42-的个数比为 [ ]
| A.1∶2 | B.1∶4 | C.3∶4 | D.3∶2 |
在200 mL某硫酸盐溶液中,含有1.5 NA个硫酸根离子(NA表示阿伏加德罗常数的值),同时含有NA个金属离子。则该硫酸盐的物质的量浓度为( )
A.2 mol·L-1 B.2.5 mol·L-1 C.5 mol·L-1 D.7.5 mol·L-1
对于常温下pH为3的NH4Cl溶液,下列叙述不正确的是
| A.c(H+) + c(NH4+)= c(Cl-)+ c(OH-) |
| B.c(Cl-)> c(NH4+)> c(OH-)> c(H+) |
| C.升高温度NH4+ 浓度变小 |
| D.加入少量NaOH溶液后,n(NH3·H2O)变小 |
下列有关化学原理表达正确的是
| A.分散系中分散质粒子的大小:Fe(OH)3悬浊液<Fe(OH)3胶体<FeCl3溶液 |
| B.反应2CO(g)=2C(s) + O2(g)的△H>O、△S<0,可利用该反应来消除CO污染 |
| C.室温下pH=3的盐酸与pH=11的MOH溶液等体积混合后溶液呈碱性,说明MOH为弱碱 |
| D.NH4NO3溶液和HNO3溶液中滴加石蕊都变红色,是因为它们均能电离出H+ |
关于浓度均为0.1mol·L-1的三种溶液:①醋酸溶液 ②NaOH溶液 ③醋酸钠溶液,下列说法不正确的是( )
| A.C(CH3COO-):③>① |
| B.水电离出的C(OH-):②>① |
| C.①和②等体积混合后的溶液:C(OH-)=C(H+)+C(CH3COOH) |
| D.①和③等体积混合后的溶液显酸性:C(CH3COO-)>C(Na+)>C(H+)>C(OH-) |
下表是不同温度下水的离子积常数:
| 温度/℃ |
25 |
t1 |
t2 |
| 水的离子积常数 |
1×10-14 |
KW |
1×10-12 |
试回答以下问题:
(1)若25℃<t1<t2,则KW__________1×10-14(填“>”、“<”或“=”),判断的理由是
。
(2)25℃ 下,将pH=13的氢氧化钠溶液与pH=1的稀盐酸等体积混合,所得混合溶液的pH=__________。
(3)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈 (填“酸性”、“中性”或“碱性”),溶液中c(Na+) c(CH3COO-)(填“>”、“=”或“<”)。
(4)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈 性(填“酸”、 “中”或“碱”),溶液中c(Na+) c(CH3COO-)[填“>”、“=”或“<”] 。
下列表述中,合理的是
| A.将水加热,Kw增大,pH不变 |
| B.NaHCO3溶液中存在6种分子或离子 |
| C.用25 mL碱式滴定管量取20.00mL高锰酸钾溶液 |
| D.用惰性电极电解足量的AgNO3溶液时,当有0.2 mole-转移时会析出21.6g银 |
下表是不同温度下水的离子积数据:
| 温度 / ℃ |
25 |
t1 |
t2 |
| 水的离子积常数 |
1×10-14 |
α |
1×10-12 |
试回答下列问题:
(1)若25<t1<t2,则α________1×10-14(填“>”“<”或“=”),作出此判断的理由是________________________________________________________。
(2)已知25℃时饱和NaHCO3溶液的PH>7,则此温度下饱和NaHCO3溶液中各离子浓度关
系正确的是______________
A.c(Na+)>c(HCO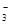 )>c(OH-)>c(H+)>c(CO
)>c(OH-)>c(H+)>c(CO )
)
B.c(Na+)+c(H+)=c(HCO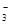 )+c(CO
)+c(CO )+c(OH-)
)+c(OH-)
C.c(Na+)=c(HCO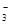 )+c(CO
)+c(CO )+c(H2CO3)
)+c(H2CO3)
D.c(OH-)=c(HCO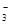 )+c(H2CO3)+c(H+)
)+c(H2CO3)+c(H+)
(3)t2℃下,将pH=11的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1∶V2=___________。此溶液中各种离子的浓度由大到小的排列顺序是____________________。
常温下,某溶液中由水电离出的c(H+)与c(OH-)的乘积为10-10,该溶液可能是( )
| A.pH等于5的醋酸溶液 | B.一定浓度的NaOH溶液 |
| C.一定浓度的NaHSO4溶液 | D.一定浓度的NH4Cl溶液 |
下列说法不正确的是( )
| A.相同物质的量浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3·H2O; c(NH4+)由大到小的顺序是:①>②>③>④ |
| B.某物质的溶液中由水电离出的c(H+)=1×10-a mol/L,若a>7时,则该溶液的pH一定为14-a |
| C.pH=8的CH3COONa溶液中:CH3COOH浓度为9.9×10-7mol/L |
| D.pH=3的HA与pH=11的NaOH等体积混合,pH一定不会大于7 |
常温下,将3种一元酸分别和NaOH溶液等体积混合,实验数据如下:
| 组别 |
一元酸 |
NaOH |
混合溶液的pH |
| 甲 |
c(HX)="0.1" mol/L |
c(NaOH)=0.1mol/L |
pH = a |
| 乙 |
c(HY)=c1 mol/L |
c(NaOH)=0.1mol/L |
pH = 7 |
| 丙 |
c(HZ)="0.1" mol/L |
c(NaOH)=0.1mol/L |
pH = 9 |
| 丁 |
pH=2 HZ |
pH=12 NaOH |
pH = b |
(1)甲组实验中HX为弱酸,a 7(填“<”,“=”或“>”),
混合溶液中离子浓度由大到小顺序为 。
(2)乙组实验中HY为强酸,则HY溶液的pH= 。
(3)丙组实验发生反应的离子方程式为 ,
所得溶液中由水电离出的c (OH-) = mol/L。
(4)丁组实验中b 7(填“<”,“=”或“>”)。
常温下a mol·L-1 CH3COOH稀溶液和bmol·L-1KOH稀溶液等体积混合,下列判断一定错误的是
| A.若c(OH-)>c(H+),a=b | B.若c(K+)<c(CH3COO-),a<b |
| C.若c(OH-)=c(H+),a>b | D.若c(K+)>c(CH3COO-),a>b |
试题篮
()