下列变化规律不正确的是 ( )
| A.温度升高,水的电离平衡向右移动 |
| B.加水稀释时,醋酸钠的水解平衡向左移动 |
| C.增大压强,对醋酸的电离平衡影响不大 |
| D.向氯化铁溶液中加入氧化钠,水解平衡向右移动 |
下列叙述正确的是( )
| A.含1 mol溶质的任何溶液,物质的量浓度一定相等 |
| B.配制1 mol·L-1 NaCl溶液1 L,其方法是:将58.5 g NaCl溶于1 L水中即可 |
| C.体积相同、物质的量浓度相同的同种溶液所含溶质的粒子数一定相同 |
| D.1 L 0.5 mol·L-1 CaCl2溶液中,Ca2+与Cl-的物质的量浓度都是0.5 mol·L-1 |
某溶液中只含有Na+、Al3+、Cl-、SO42- 四种离子,已知前三种离子的个数比为3∶2∶1则溶液中Al3+和 SO42-的离子个数比为( )
| A.1∶2 | B.1∶4 | C.3∶4 | D.3∶2 |
某温度下,100g饱和氯化钠溶液中含有氯化钠26.5g。若向此溶液中添加3.5g氯化钠和6.5g水,则所得溶液的溶质质量分数是
| A.30% | B.100% |
| C.26.5% | D.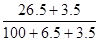 ×100% ×100% |
下列各物质溶液中,指定微粒浓度之间的关系不正确的是( )
| A.饱和NH4Cl溶液中:c(H+)+ c(NH4+)= c(Cl―)+ c(OH―) |
| B.0.1mol/LNaHCO3溶液中:c(HCO3―)+ c(CO32―)+ c(H2CO3)=0.1mol/L |
| C.饱和NaHS溶液中:c(Na+)> c(HS―)> c(H+)> c(OH―) |
| D.0.1mol/LCH3COONa溶液中:c(CH3COO―)> c(OH―) |
食盐中的抗结剂是亚铁氰化钾,其化学式为K4[Fe(CN)6] •3H2O。
42.2g K4[Fe(CN)6] •3H2O样品受热脱水过程的热重曲线(样品质量随温度的变化曲线)如下图所示。试回答下列问题: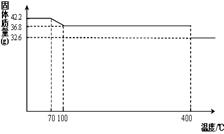
(1)试确定150℃时固体物质的化学式为_______________。
(2)查阅资料知:虽然亚铁氰化钾自身毒性很低,但其水溶液与酸反应放出极毒的氰化氢(HCN)气体;亚铁氰化钾加热至一定温度时能分解产生氰化钾(KCN)。据此判断,烹饪食品时应注意的问题为___________________________________。
(3)在25℃下,将a mol•L-1的KCN(pH>7)溶液与0.01mol•L-1的盐酸等体积混合,反应平衡时,测得溶液pH=7,则KCN溶液的物质的量浓度a_______0.01mol•L-1(填“>”、“<”或“=”)。
(4)在25℃下,KCN溶液pH=9,c(K+)-c(CN_)="_______" mol•L-1(用数字表示但不需近似计算)。
(5)已知Fe(OH)3的溶度积常数Ksp=1.1×10-38。室温时在FeCl3溶液中滴加NaOH溶液,当溶液中Fe3+沉淀完全时,控制pH应不小于 。
(提示:当某离子浓度小于10-5 mol•L-1时可以认为该离子沉淀完全了;)
向20 mL NaOH溶液中逐滴加入0.1 mol/L醋酸溶液,滴定曲线如右图所示。下列判断正确的是( )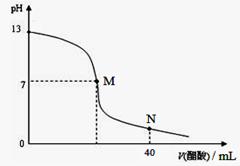
| A.在M点,两者恰好反应完全 |
| B.滴定前,酸中c(H+) 等于碱中c(OH-) |
| C.NaOH溶液的物质的量浓度为0.1 mol/L |
| D.在N点,c(CH3COO-)>c(Na+)>c(H+)>c(CH3COOH) |
Ⅰ:(4分)若取4.00mol/L的氨水30.0mL与70.0mL2.00mol·L-1的AlCl3溶液相混合,产生白色沉淀的质量是 g
Ⅱ:实验室用4.35gMn02与l00 mL11mol/L的浓盐酸(足量)反应制取氯气。 试计算:
(1)在标准状况下,生成氯气的体积。(不考虑氯气在溶液中的溶解)
(2)将反应后的溶液加水稀释到500mL,向从其中取出的50mL溶液中加入足量AgN03溶液,生成沉淀的物质的量。(要求写出计算过程)
已知在酸性溶液中,下列物质氧化KI时,自身发生如下变化:
Fe3+→Fe2+;MnO4-→Mn2+;Cl2→2Cl-;HNO3→NO。 如果分别用相同物质的量的这些物质氧化足量的KI,得到I2最多的是
| A.Fe3+ | B.MnO4- | C.Cl2 | D.HNO3 |
向100ml0.1 mol·L-1的Al2(SO4)3溶液中,加入0.5mol·L-1的氢氧化钠溶液得到1.17克沉淀,则需加入的氢氧化钠溶液的体积是多少?(强调要有解题过程)
下列对溶液叙述正确的是
| A.向冰醋酸中加水至配成醋酸稀溶液的过程中H+的浓度逐渐减小 |
| B.对于物质的量浓度相同的氢氧化钠和氨水,加水稀释至m倍、n倍后,若稀释后溶液的PH相等,则m<n |
| C.常温下,5ml0.02mol/LHCl溶液与5ml0.02mol/LBa(OH)2溶液混合,经充分反应后,如果溶液体积为10mL,则溶液的PH=12 |
| D.常温下将稀NaOH溶液与醋酸溶液混合,可能出现PH>7的情况,且c(OH-)>c(Na+)>c(CH3COO-)>c(H+) |
(1)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
A.c(NH4+)>c(Cl-)>c(OH-)>c(H+) B.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) D.c(Cl-)>c(NH4+)>c(H+)>c(OH-)
①若溶液中只溶解了一种溶质,该溶质的名称是 ,上述离子浓度大小顺序关系中正确的是(选填序号) 。
②若上述关系中C是正确的,则溶液中溶质的化学式是 。
③若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)(填“>”、“<”、或“=”,下同) c(NH3·H2O),混合后溶液中c(NH4+)与c(Cl-)的关系c(NH4+) c(Cl-)。
(2)在25℃条件下将pH=11的氨水稀释100倍后溶液的pH为(填序号) 。
A.9 B.9~11之间 C.11~13之间 D.13
(3)25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是(填序号) 。
A.氨水与氯化铵发生化学反应;
B.氯化铵溶液水解显酸性,增加了c(H+);
C.氯化铵溶液水解显碱性,降低了c(H+);
D. 氯化铵溶于水,电离出大量铵根离子,抑制了氨水的电离,使c(OH-)减小;
能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的操作是( )
| A.向水中投入一小块金属钠 | B.将水加热煮沸 |
| C.向水中通入二氧化碳气体 | D.向水中加食盐晶体 |
试题篮
()