在一定温度下,在体积可变的容器中,进行可逆反应A(g) + B(g) C(g) + 2D(g);下列能说明该反应达到平衡状态的是
C(g) + 2D(g);下列能说明该反应达到平衡状态的是
①反应混合物的密度不再改变 ②混合气体的平均相对分子质量不再改变 ③C和D的物质的量之比为1:2 ④体系压强不再改变 ⑤C的质量分数不再改变 ⑥υ(A) : υ(C) =" 1:" 1
A.①②④⑤ B.①②⑤ C.②⑤⑥ D.①②③④⑤⑥
在2L的密闭容器中发生化学反应:2NO(g)+2CO(g) N2(g) +2CO2 (g) △H= -746.4kJ/mol。起始反应时NO和CO各为4mol,10秒后达到化学平衡,测得N2为1mol。下列有关反应速率的说法中,正确的是
N2(g) +2CO2 (g) △H= -746.4kJ/mol。起始反应时NO和CO各为4mol,10秒后达到化学平衡,测得N2为1mol。下列有关反应速率的说法中,正确的是
| A.反应前5秒钟内,用NO表示的平均反应速率为0.1mol/(L·s) |
| B.达到平衡后,升高温度,可以提高反应物的转化率 |
| C.达到平衡后,反应速率的关系有:υ正(CO) =2υ逆(N2) |
| D.保持容器体积不变,往容器中充入1molO2,正、逆反应速率都不改变 |
反应2A(g) 2B(g) + C(g) △H < 0 ,现欲使正反应速率减小,C的浓度增大,可行的措施是
2B(g) + C(g) △H < 0 ,现欲使正反应速率减小,C的浓度增大,可行的措施是
| A.加压 | B.增大C的浓度 | C.减少C的浓度 | D.降温 |
下列说法正确的是
| A.在化学反应中,化学能只可以转化为热能 |
B.合成氨反应N2+3H2 2NH3,当N2、H2、NH3浓度相等时该反应达到了最大限度 2NH3,当N2、H2、NH3浓度相等时该反应达到了最大限度 |
C.合成氨反应N2+3H2 2NH3中,升高温度,该反应速率减小 2NH3中,升高温度,该反应速率减小 |
| D.化学键的断裂和形成是化学反应中能量变化的主要原因 |
在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)  2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是


| A.图Ⅰ研究的是t0时刻增大O2的物质的量浓度对反应速率的影响 |
| B.图Ⅱ研究的是t0时刻通入氦气增大体系压强对反应速率的影响 |
| C.图Ⅲ研究的是催化剂对化学平衡的影响,且甲的催化效率比乙高 |
| D.图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高 |
在密闭容器中,mA(g)+bB(g) pC(g) 反应平衡时,测得 c(A)为 0.5mol•L‾1,在温度不变的情况下,将容器体积增大一倍,当达到新的平衡时,测得 c(A)为 0.3mol•L‾1,则下列判断中正确的是
pC(g) 反应平衡时,测得 c(A)为 0.5mol•L‾1,在温度不变的情况下,将容器体积增大一倍,当达到新的平衡时,测得 c(A)为 0.3mol•L‾1,则下列判断中正确的是
A.平衡向正反应方向移动 B.物质C的质量分数增加
C.化学计量数:m+b<p D.物质B的转化率减小
下列事实不能用勒夏特列原理解释的是
| A.由H2、I2蒸气、HI组成的平衡体系加压后颜色变深 |
| B.开启啤酒瓶后,瓶中立刻泛起大量泡沫 |
| C.向氯水中加CaCO3后,溶液漂白性增强 |
| D.在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去 |
(1)反应N2O4(g) 2NO2(g);DH>0的平衡体系中,在298K时,平衡常数为K1,在273K时,平衡常数为K2,在373K时平衡常数为K3,K1、K2、K3之间的数量大小关系是 。
2NO2(g);DH>0的平衡体系中,在298K时,平衡常数为K1,在273K时,平衡常数为K2,在373K时平衡常数为K3,K1、K2、K3之间的数量大小关系是 。
(2)在298K时,将0.40 mol的N2O4气体充入2 L已经抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间/s n/mol |
0 |
20 |
40 |
60 |
80 |
100 |
| n(N2O4) |
0.40 |
a |
0.20 |
c |
d |
e |
| n(NO2) |
0.00 |
0.24 |
b |
0.52 |
0.60 |
0.60 |
20~40 s内用N2O4表示的平均反应速率为________mol·L-1·s-1;298K时该反应的平衡转化率=________;反应进行至100 s后将反应混合物的温度降低,混合气体的颜色________(填“变浅”、“变深”或“不变”);
(3)298K时,反应2NO2(g) N2O4(g);DH<0达到平衡后,根据下列图像判断引起平衡移动的因素及平衡移动的的方向:
N2O4(g);DH<0达到平衡后,根据下列图像判断引起平衡移动的因素及平衡移动的的方向:

图(2)平衡将向_______方向移动;图(3)引起平衡移动的因素是_____________,图(4)引起平衡移动的因素是______________。
对可逆反应:X(g)+Y(g) 2Z(g)+W(s) ΔH<0,下列叙述正确的是
2Z(g)+W(s) ΔH<0,下列叙述正确的是
| A.平衡常数K值越大,X的转化率越大 |
| B.达到平衡时,反应速率v正(X)=2v逆(Z) |
| C.降低温度,正向反应速率减小的倍数大于逆向反应速率减小的倍数 |
| D.升高温度或增大压强都有利于该反应平衡向逆反应方向移动 |
一定条件下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),的化学平衡常数K=1,相同条件下,当C(CO2)=0.5mol·L-1、C(H2)=0.5mol·L-1、C(CO)=1mol·L-1、C(H2O)=1mol·L-1时,下列说法正确的是
CO(g)+H2O(g),的化学平衡常数K=1,相同条件下,当C(CO2)=0.5mol·L-1、C(H2)=0.5mol·L-1、C(CO)=1mol·L-1、C(H2O)=1mol·L-1时,下列说法正确的是
| A.处于平衡状态,正逆反应速率相等 |
| B.平衡逆移,正反应速率小于逆反应速率 |
| C.CO2的转化率为50% |
| D.该条件下,学平衡常数K=4 |
在密闭容器中,一定条件下,进行如下反应:2NO(g)+2CO(g) N2(g)+2CO2(g) DH<0,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
N2(g)+2CO2(g) DH<0,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
| A.加催化剂同时升高温度 |
| B.加催化剂同时增大压强 |
| C.升高温度同时充入N2 |
| D.降低温度同时增大压强 |
在一定温度下,向a L密闭容器中加入1 mol X气体和2 mol Y气体,发生如下反应:X(g)+3Y(g) 4Z(g),此反应达到平衡的标志是
4Z(g),此反应达到平衡的标志是
| A.容器内压强不随时间变化 |
| B.容器内各物质的浓度不随时间变化 |
| C.容器内X、Y、Z的浓度之比为1∶3∶4 |
| D.单位时间消耗0.1 mol X同时生成0.4mol Z |
乙苯催化脱氢制苯乙烯反应: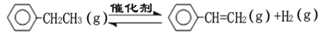
(1)已知:
| 化学键 |
C-H |
C-C |
C=C |
H-H |
| 键能/kJ·molˉ1 |
412 |
348 |
612 |
436 |
计算上述反应的△H=__________。
(2)维持体系总压强p恒定,在温度T时,物质的量为n的乙苯蒸汽发生催化脱氢反应。已知乙苯的平衡转化率为α,则在该温度下反应的压强平衡常数Kp=___________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)工业上,通常在乙苯蒸汽中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1︰9),控制反应温度600℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)示意图如下:
① 掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实___________。
② 控制反应温度为600℃的理由是____________。
(4)某研究机构用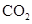 代替水蒸气开发了绿色化学合成工艺——乙苯-二氧化碳耦合催化脱氢制苯乙烯。保持常压和原料气比例不变,与掺水蒸汽工艺相比,在相同的生产效率下,可降低操作温度;已知该工艺中还能够发生反应:
代替水蒸气开发了绿色化学合成工艺——乙苯-二氧化碳耦合催化脱氢制苯乙烯。保持常压和原料气比例不变,与掺水蒸汽工艺相比,在相同的生产效率下,可降低操作温度;已知该工艺中还能够发生反应: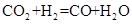 ,
,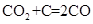 ,据此可推知新工艺的特点有_________(填编号)。
,据此可推知新工艺的特点有_________(填编号)。
①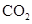 与
与 反应,使乙苯脱氢反应的化学平衡右移
反应,使乙苯脱氢反应的化学平衡右移
② 不用高温水蒸气,可降低能量消耗
③ 有利于减少积炭
④ 有利用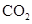 资源利用
资源利用
试题篮
()