在温度、容积相同的2个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下
(已知N2(g)+3H2(g) 2NH3(g) △H=-92.4 kJ·mol-1)
2NH3(g) △H=-92.4 kJ·mol-1)
| 容器 |
甲 |
乙 |
| 反应物投入量 |
1 mol N2、3 mol H2 |
4 mol NH3 |
| NH3的浓度(mol·L-1) |
c1 |
c2 |
| 反应的能量变化 |
放出a kJ |
吸收b kJ |
| 气体密度 |
ρ1 |
ρ2 |
| 反应物转化率 |
α1 |
α2 |
下列说法正确的是
A.c1<c2<2 c1 B.a+b>92.4 C.α1 +α2=1 D.ρ2=2ρ1
T℃,向5.0 L恒容密闭容器中充入1.0 molSO3气体,发生反应:2SO3(g)  2SO2(g)+O2(g)
2SO2(g)+O2(g)
△H="+196" kJ/mol,一段时间后达到平衡,测得此过程中从外界共吸收了19.6 kJ的热量。当温度度不变时,改变某一条件,下列结论正确的是
下列图示与对应的叙述相符的是
A.图I可表示N2+3H2 2NH3的速率时间图像,t1时刻改变的条件是升高温度 2NH3的速率时间图像,t1时刻改变的条件是升高温度 |
| B.图Ⅱ可表示用0.1 000 mol/L醋酸滴定40.00 mL0.1000 mol/LNaOH溶液得到的滴定曲线 |
| C.图Ⅲ可表示NO2平衡转化率与温度、压强的变化关系,由图可知:△H<0、P1<P2 |
| D.图Ⅳ可表示pH相同的NaOH溶液与氨水稀释过程的pH变化.其中曲线a对应氨水 |
如图所示,隔板I固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:A(g) + 2B(g) xC(g)ΔH=-192kJ·mol-1,向M、N中都通入1molA和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是 ( )
xC(g)ΔH=-192kJ·mol-1,向M、N中都通入1molA和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是 ( )
| A.若x=3,达到平衡后A的体积分数关系为:φ(M)>φ(N) |
| B.若x>3,达到平衡后B的转化率关系为:α(M)>α(N) |
| C.若x<3,C的平衡浓度关系为:c(M)>c(N) |
| D.x不论为何值,起始时向N容器中充入任意值的C,平衡后N容器中A的浓度均相等 |
物质(t-BuNO)2在正庚烷或CCl4中均可以发生反应:(t-BuNO)2 2(t-BuNO)。在20℃时,向1 L正庚烷中加入(t-BuNO)2 0.50 mol,10 min时反应达平衡,此时(t-BuNO)2的平衡转化率为65%(假设反应过程中溶液体积始终为1 L)。下列说法正确的是
2(t-BuNO)。在20℃时,向1 L正庚烷中加入(t-BuNO)2 0.50 mol,10 min时反应达平衡,此时(t-BuNO)2的平衡转化率为65%(假设反应过程中溶液体积始终为1 L)。下列说法正确的是
| A.反应在前10 min内的平均速率为ν(t-BuNO)=0.0325mol·L-1·min-1 |
| B.保持其他条件不变,若此时再向溶液中加入0.50 mol (t-BuNO)2,重新达平衡时(t-BuNO)2的百分含量减小 |
| C.保持其他条件不变,若该反应在CCl4中进行,其平衡常数为1.9,则(t-BuNO)2的平衡转化率小于65% |
| D.保持其他条件不变,升高温度, (t-BuNO)2的平衡转化率大于65%,则其能量关系可用下图表示 |

900℃时,向2.0L恒容密闭容器中充入0.40mol乙苯,发生反应: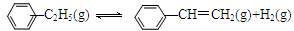 ΔH=a kJ·mol—1。经一段时间后达到平衡。反应过程中测定的部分数据见下表:
ΔH=a kJ·mol—1。经一段时间后达到平衡。反应过程中测定的部分数据见下表:
| 时间/min |
0 |
10 |
20 |
30 |
40 |
| n(乙苯)/mol |
0.40 |
0.30 |
0.24 |
n2 |
n3 |
| n(苯乙烯)/mol |
0.00 |
0.10 |
n1 |
0.20 |
0.20 |
下列说法正确的是
A.反应在前20 min的平均速率为v(H2)=0.008mol·L-1·min-1
B.保持其他条件不变,升高温度,平衡时,c(乙苯)=0.08mol·L-1,则a<0
C.保持其他条件不变,向容器中充入不参与反应的水蒸气作为稀释剂,则乙苯的转化率为50.0%
D.相同温度下,起始时向容器中充入0.10mol乙苯、0.10mol苯乙烯和0.30molH2,达到平衡前v正>v逆
N2(g)+3H2(g) 2NH3(g) △H=-92.4 kJ·mol-1。恒容时,体系中各物质浓度随时间变化的曲线如图示。下列说法错误的是
2NH3(g) △H=-92.4 kJ·mol-1。恒容时,体系中各物质浓度随时间变化的曲线如图示。下列说法错误的是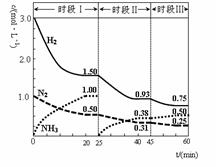
| A.前20分钟反应内放出的热量为46.2kJ |
| B.第25分钟改变的条件是将NH3从反应体系中分离出去 |
| C.若第60分钟时反应又达到了平衡,则时段Ⅲ改变的条件是降低温度 |
| D.时段Ⅰ仅将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数不变 |
为减小CO2对环境的影响,在倡导“低碳”的同时,还需加强对CO2创新利用的研究。T10C 时,将9molCO2和12molH2充入3L密闭容器中,发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH<0,容器中CH3OH的物质的量随时间变化如曲线I所示,平衡时容器内压强为P。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线II所示。下列说法错误的是
CH3OH(g)+H2O(g) ΔH<0,容器中CH3OH的物质的量随时间变化如曲线I所示,平衡时容器内压强为P。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线II所示。下列说法错误的是
| A.曲线II对应的条件改变是增大压强 |
| B.T2°C时,上述反应平衡常数为0.42,则T2> T1 |
| C.在T10C,若起始时向容器中充入5 mol CO2、5 mol H2、5 mol CH3OH(g)和5 mol H2O(g),则达平衡前v(正)>v(逆) |
D.在T10C,若起始时向容器由通入4,5 molCO2、6mol H2 ,平衡时容器内压强 |
某温度下在容积不变的密闭容器中,发生aX(g)+bY(g) cW(g)反应,当充入1 mol X和lmol Y,达到平衡时,W的浓度为0.2 mol/L。下列说法错误的是
cW(g)反应,当充入1 mol X和lmol Y,达到平衡时,W的浓度为0.2 mol/L。下列说法错误的是
| A.达到平衡时,消耗b mol Y的同时消耗c moI W |
| B.若升高温度,W的物质的量浓度减小,则该反应△H<0 |
| C.若起始投入X、Y的物质的量分别为amol和bmol,则平衡时X、Y的转化率相等 |
| D.在相同条件下,再充人l mol X和1 mol Y,达新平衡时,W的浓度为0.4 mol/L,则a+b>c |
一定温度下,在甲、乙、丙、丁四个恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。
| |
甲 |
乙 |
丙 |
丁 |
|
| 密闭容器体积/L |
2 |
2 |
2 |
1 |
|
| 起始物质的量 |
n(SO2)/mol |
0.4 |
0.8 |
0.8 |
0.4 |
| n(O2)/mol |
0.24 |
0.24 |
0.48 |
0.24 |
|
| SO2的平衡转化率/% |
80 |
α1 |
α2 |
α3 |
下列判断中,正确的是
A.甲中反应的平衡常数小于乙
B.该温度下,甲和乙中反应的平衡常数K均为400
C.SO2的平衡转化率:α1>α2=α3
D.容器中SO3的物质的量浓度:丙>甲=丁
难挥发性二硫化担(TaS2)可采用如下装置提纯。将不纯的TaS2粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中。反应如下:
下列说法正确的是
| A.该反应的△H>0 |
| B.在提纯过程中,S2的量不断增加 |
| C.该反应的平衡常数与I2的浓度成正比 |
| D.经过足够长时间后,石英管右端将得到纯净的TaS2 |
碘钨灯比白炽灯使用寿命长。灯管内封存的少量碘与使用过程中沉积在管壁上的钨可以发生反应:W(s)+I2(g) WI2(g) ΔH<0(温度T1<T2)。下列说法正确的是
WI2(g) ΔH<0(温度T1<T2)。下列说法正确的是
| A.灯管工作时,扩散到灯丝附近高温区的WI2(g)会分解出W,W重新沉积到灯丝上 |
| B.灯丝附近温度越高,WI2(g)的转化率越低 |
C.该反应的平衡常数表达式是 |
| D.利用该反应原理可以提纯钨 |
在一定条件下,固定容积的密闭容器中反应:2NO2(g) 2NO (g) +O2 (g) △H>0,达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是
2NO (g) +O2 (g) △H>0,达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是
| A.当X表示温度时,Y表示NO2的物质的量 |
| B.当X表示压强时,Y表示NO2的转化率 |
| C.当X表示反应时间时,Y表示混合气体的密度 |
| D.当X表示NO2的物质的量时,Y表示O2的物质的量 |
二氧化硫的催化氧化原理为2SO2(g)+O2(g) 2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如下图所示。下列说法错误的是
2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如下图所示。下列说法错误的是
A.在D点时v E<v逆
B.反应2SO2(g)+O2(g) 2SO3(g)的△H<0
2SO3(g)的△H<0
C.若B、C点的平衡常数分别为KB、KC,则KB>KC
D.恒温恒压下向平衡体系中通入氦气,平衡向左移动
在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g) Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表:
Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表:
下列说法正确的是( )
| A.上述生成Ni(CO)4(g)的反应为吸热反应 |
B.25℃时反应Ni(CO)4(g)  Ni(s)+4CO(g)的平衡常数为0.5(mol·L-1)3 Ni(s)+4CO(g)的平衡常数为0.5(mol·L-1)3 |
| C.在某条件下达到平衡,测得Ni(CO)4、CO浓度均为0.5mol/L,则此时温度高于80℃ |
| D.80℃达到平衡时,保持体积不变,往体系中充入一定量的CO,再次达到平衡后CO的体积分数减小 |
试题篮
()