表是五种银盐的溶度积常数(25℃)。下列说法错误的是( )
| 化学式 |
AgCl |
Ag2SO4 |
Ag2S |
AgBr |
AgI |
| 溶度积 |
1.8×10-10 |
1.4×10-5 |
6.3×10-50 |
7.7×10-13 |
8.5×10-16 |
A.五种物质在常温下溶解度最大的是Ag2SO4
B.将AgCl溶解于水后,向其中加入Na2S则可以生成黑色沉淀
C.AgCl 、AgBr、AgI三种物质在常温下的溶解度按氯、溴、碘的顺序减小
D.向100ml0.1mol/LNa2SO4溶液中加入1mL0.1mol/L AgNO3溶液,有沉淀生成
已知某温度下CH3COOH和NH3•H2O 的电离常数相等,现向10mL浓度为0.1mol•L‾1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中下列说法正确的是
| A.水的电离程度始终增大 |
| B.当加入氨水的体积为10mL时,c(NH4+)=c(CH3COO‾) |
| C.c(CH3COOH)与c(CH3COO‾)之和始终保持不变 |
| D.c(NH4+)/c(NH3•H2O)先增大再减小 |
25℃时,重水(D2O)的离子积为1.6X10-15,也可用PH值一样的定义来规定其酸碱度:PD=-lg[D+],下列有关PD的叙述,正确的是()
①中性D2O的PD="7"
②在1L D2O中,溶解0.01molNaOD,其PD值为12
③1L0.01mol/L的DCl的重水溶液,PD="2"
④在100mL 0.25mol/L DCl的重水溶液中,加入50mL 0.2mol/L NaOD的重水溶液,反应后溶液的PD="1"
| A.①② | B.③④ | C.①③④ | D.①②③④ |
下列有关沉淀溶解平衡的说法正确的是
A.Ksp(AB2)小于Ksp(CD),则AB2的溶解度小于CD的溶解度
B.在AgCl的沉淀溶解平衡体系中,加入蒸馏水,AgCl的Ksp增大
C.在AgI的沉淀溶解平衡体系中,加入K2S固体,AgI沉淀可转化为Ag2S沉淀
D.在CaCO3的沉淀溶解平衡体系中,通入CO2气体,溶解平衡不移动
下列有关Ksp的叙述中正确的是
| A.Ksp越大说明电解质的溶解度越大 |
| B.Ksp只与电解质的本性有关,而与外界条件无关 |
| C.Ksp表示难溶强电解质在水中达到沉淀溶解平衡时,溶液中离子浓度幂之积 |
| D.Ksp的数值只与难溶电解质的性质有关,和温度无关 |
25℃时,Ksp(AgCl)=1.56×10﹣10,Ksp(Ag2CrO4)=9.0×10﹣12,下列说法正确的是( )
| A.向同浓度的Na2CrO4和NaCl混合溶液中滴加AgNO3溶液,AgCl先析出 |
| B.向AgCl饱和溶液中加入NaCl晶体,有AgCl析出且溶液中c(Ag+)=c(Cl﹣) |
C.AgCl和Ag2CrO4共存的悬浊液中,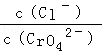 = =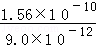 |
| D.向Ag2CrO4的悬浊液中加入NaCl浓溶液,Ag2CrO4不可能转化为AgCl |
下列说法中正确的是
| A.物质的溶解性为难溶,则该物质不溶于水 |
| B.不溶于水的物质溶解度为0 |
| C.某离子被沉淀完全是指该离子在溶液中的浓度为0 |
| D.绝对不溶解的物质是不存在的 |
在2mlNaCl溶液中加入1滴AgNO3溶液,有白色沉淀生成;再加入1滴KI溶液沉淀转化为黄色,然后再加入1滴Na2S溶液,沉淀又转化为黑色(以上所用的溶液物质的量浓度均相同),下列表示各沉淀物溶解度由大到小的顺序正确的是
| A.Ag2S AgI AgCl | B.AgCl AgI Ag2S |
| C.AgI AgCl Ag2S | D.AgCl Ag2S AgI |
水是最常用的溶剂,许多化学反应都需要在水溶液中进行。请仔细分析并回答下列各题。
(1)用0.1mol/LNaOH溶液滴定体积均为20.00mL、浓度均为0.1mol/L盐酸和醋酸溶液,得到如下所示滴定曲线图: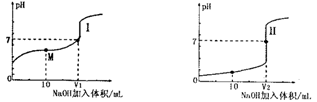
①用NaOH 溶液滴定醋酸溶液通常所选择的指示剂为________,符合其滴定曲线的是_______(填“I”或“II”);
②滴定前的上述三种溶液中,由水电离出的c(H+)最大的是_________溶液(填化学式);
③图中v1和v2大小的比较:v1_______v2 (填“>”、“<”或“=”);
④图I中M 点对应的溶液中,各离子的浓度由大到小的顺序是______________。
(2)某同学为了研究难溶电解质的溶解平衡,设计了如下实验(相关数据测定温度及实验环境均为25 ℃ ):
| 操作步骤 |
现象 |
| 步骤1:向20mL0.05mol/LAgNO3溶液中加入20mL0.05mol/LKSCN溶液,充分反应后过滤 |
出现白色沉淀 |
| 步骤2:向滤液中加少量2mol/LFe(NO3)3溶液 |
溶液变红色 |
| 步骤3:向步骤2所得溶液中,加入少量3mol/LAgNO3溶液 |
现象a |
| 步骤4:取步骤1所得少量滤渣加入到适量的3mol/LKI溶液中 |
出现黄色沉淀 |
查阅资料:AgSCN是白色沉淀:Ksp(AgSCN)=1.0×10-12;Ksp(AgI)=8.5×10-17.
① 请结合化学用语和必要的文字解释步骤2 现象出现的原因:____________________。
②该同学根据步骤3中现象a推知,加入的AgNO3与步骤2所得溶液发生了反应,则现象a为______________(任写一点即可)。
③ 写出步骤4 中沉淀转化反应平衡常数的表达式:K=__________。
25℃时,水的电离达到平衡:H2O H+ + OH-,下列叙述正确的是
H+ + OH-,下列叙述正确的是
| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| C.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| D.将水加热,Kw增大,pH不变 |
下列关于甲、乙、丙、丁四个图像的说法中,正确的是

| A.图甲表示向盐酸溶液中通入NH3过程中溶液导电性的变化 |
| B.由图乙可知,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量CuO至pH在4左右 |
| C.图丙表示25 ℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1氨水,溶液的pH随加入盐酸体积的变化 |
| D.图丁表示向Al2(SO4)3溶液中滴入NaOH溶液,生成Al(OH)3沉淀的量随NaOH溶液体积的变化 |
向饱和食盐水中滴加一定浓度的盐酸,对出现现象的预测可能正确的是
| A.白色沉淀 | B.液体分层 | C.无明显现象 | D.黄绿色气体 |
溴酸银(AgBrO3)的溶解度随温度变化曲线如右上图所示,下列说法正确的是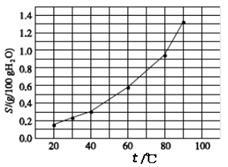
| A.温度升高不利于溴酸银的溶解 |
| B.溴酸银的溶解是放热过程 |
| C.若硝酸钾中含有少量溴酸银,可用重结晶方法提纯 |
| D.60 ℃时,将0.04g溴酸银加入到10g水中,形成的分散系中存在沉淀溶解平衡 |
在一定温度下,当Mg(OH)2固体在水溶液中达到下列平衡时:Mg(OH)2(s) Mg2+(aq)+2OH-(aq),若使固体Mg(OH)2的量减少,而且c(Mg2+)不变,可采取的措施是
Mg2+(aq)+2OH-(aq),若使固体Mg(OH)2的量减少,而且c(Mg2+)不变,可采取的措施是
| A.加MgCl2 | B.加H2O | C.加NaOH | D.加HCl |
下列有关说法正确的是
| A.AlCl3溶液蒸干、灼烧至恒重,最终剩余固体是AlCl3 |
| B.反应Hg(1)+H2SO4(aq) = HgSO4(aq)+H2(g)在常温下不能自发进行,则△H>0 |
| C.将纯水加热至较高温度,K变大、pH变小、呈酸性 |
| D.锅炉中沉积的CaSO4可用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除去 |
试题篮
()