已知AgCl的溶解度为1.5×10-4g , AgBr的溶解度为8.4×10-6g ,如果将AgCl和 AgBr的饱和溶液等体积混合,再加入足量浓AgNO3溶液,发生反应的结果为
| A.只有AgBr沉淀生成 | B.AgCl和AgBr沉淀等量生成 |
| C.AgCl沉淀多于AgBr沉淀 | D.AgCl沉淀少于AgBr沉淀 |
下列叙述Ⅰ和Ⅱ均正确且有因果关系的是
| 选项 |
叙述Ⅰ |
叙述Ⅱ |
| A |
往AgNO3溶液中滴加氨水至过量,先有沉淀后溶解 |
AgOH是两性氢氧化物 |
| B |
常温下,H2CO3的K1=4.4×10-7,HClO的K=2.98×10-8 |
用CO2与NaClO溶液制备HClO |
| C |
硅的熔点高硬度大 |
晶体硅可用做半导体材料 |
| D |
NO2溶于水生成HNO3 |
NO2是酸性氧化物 |
对于难溶盐MX,其饱和溶液中M+和X-的物质的量浓度之间的关系类似于c(H+)·c(OH-)=Kw,存在等式c(M+)·c(X-)=Ksp。现将足量的AgCl分别放入下列物质中,AgCl的溶解度由大到小的排列顺序是
①30 mL0.03 mol·L-1 AgNO3溶液 ②30 mL 0.02mol·L-1CaCl2溶液
③30 mL 0.03mol·L-1HI溶液 ④30 mL蒸馏水
| A.①>②>③>④ | B.③>④>①>② |
| C.②>①④>>③ | D.④>③>②>① |
下列说法正确的是
| A.制备硫酸亚铁晶体时,最后在蒸发皿中蒸发浓缩溶液时,只需小火加热至溶液被全部蒸干 |
| B.向1 mL浓度均为0.05 mol·L-1的NaCl、NaI混合溶液中滴加2滴0.01 mol·L-1的AgNO3溶液,振荡,沉淀呈黄色。结论:Ksp(AgCl)<Ksp(AgI) |
| C.0.1mol·L-1的NaOH溶液分别中和pH、体积均相等的醋酸和盐酸,所消耗NaOH溶液的体积:前者小于后者 |
| D.水的电离过程是吸热过程,升高温度,水的离子积增大、pH减小 |
下列有关电解质溶液中粒子浓度关系正确的是
| A.pH相同的①CH3COONa、②NaHCO3、③NaClO三种溶液的c(Na+):①>②>③ |
| B.含有AgCl和AgI固体的悬浊液:c(Ag+)>c(Cl-)=c(I-) |
| C.CO2的水溶液:c(H+)>c(HCO3-)=2c(CO32-) |
| D.含等物质的量的NaHC2O4和Na2C2O4的溶液:3c(Na+)=2[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] |
下列说法中,正确的是
| A.AgI、AgCl与水混合后形成的分散系中:c(Ag+)=c(I-)>c(C1-) |
| B.25℃时,在pH相等的NH4C1溶液和盐酸中,水的电离程度也相等 |
| C.25℃时,将pH=11的NaOH溶液与pH=3的某弱酸HA的溶液等体积混合,混合后的溶液呈碱性 |
| D.25℃时,在pH=2的H2C2O4(一种二元弱酸)溶液与pH=12的NaOH溶液以任意比例混合后形成的溶液中,一定存在:c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-) |
下列叙述I和II均正确且具有因果关系的是
| 编号 |
叙述I |
叙述II |
| A |
Ksp(CaCO3) < Ksp(CaSO4) |
用Na2CO3溶液和盐酸除水垢CaSO4 |
| B |
金属钠有还原性 |
用金属钠检验无水乙醇中是否含有少量水 |
| C |
金属活动性铜比铁弱 |
镀铜铁制品表层划损后仍然受到保护 |
| D |
Cl2具有漂白性 |
用氯气制盐酸 |
向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成。经查资料得知:Ag++2NH3 H2O
H2O [Ag(NH3)2]
[Ag(NH3)2] +2H2O。下列分析不正确的是
+2H2O。下列分析不正确的是
A.浊液中存在沉淀溶解平衡:AgCl(s) Ag+ (aq) Ag+ (aq) Cl-(aq) Cl-(aq) |
| B.实验可以证明NH3结合Ag+能力比Cl-强 |
| C.实验表明实验室可用氨水洗涤银镜反应后的试管 |
| D.由资料信息可推知:加浓硝酸后生成的沉淀为AgCl |
还原沉淀法是处理含铬(含Cr2O72﹣和CrO42﹣)工业废水的常用方法,过程如下: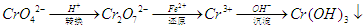 ,已知转化过程中反应为:2CrO42﹣(aq)+2H+(aq)==Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是
,已知转化过程中反应为:2CrO42﹣(aq)+2H+(aq)==Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是
| A.若用绿矾(FeSO4·7H2O)(M=278)作还原剂,处理1L废水,至少需要917.4g |
| B.溶液颜色保持不变,说明上述可逆反应达到达平衡状态 |
| C.常温下转换反应的平衡常数K=1×1014,则转化后所得溶液的pH=6 |
| D.常温下Ksp[Cr(OH)3]=1×10﹣32,要使处理后废水中c(Cr3+)降至1×10﹣5mol/L,应调溶液的pH=5 |
已知常温下AgCl的Ksp=1.8×10-10,AgI的Ksp=8.5×10-17。若向5mL含有KCl和KI各为0.01mol/L的混合溶液中加入8mL 0.01mol/L AgNO3溶液,此时溶液中所含溶质的离子浓度大小关系正确的是
| A.c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-) |
| B.c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-) |
| C.c(NO3-)>c(K+)>c(Ag+)>c(Cl-)>c(I-) |
| D.c(K+)>c(NO3-)>c(Ag+)=c(Cl-)+c(I-) |
硫化汞(HgS)难溶于水,在自然界中呈红褐色,常用于油画颜料、印泥及朱红雕刻漆器等。某温度时,HgS在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
| A.向硫化汞的浊液中加入硫化钠溶液,硫化汞的Ksp减小 |
| B.图中a点对应的是饱和溶液 |
| C.向c点的溶液中加入Hg(NO3)2,则c(S2-)减小 |
| D.升高温度可以实现c点到b点的转化 |
下列有关说法正确的是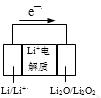
| A.25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)将减小 |
B.一定温度下,反应“2HI(g)  H2(g)+I2(g) △H>0”能自发进行,则该反应△S>0 H2(g)+I2(g) △H>0”能自发进行,则该反应△S>0 |
| C.向滴有酚酞的Na2CO3溶液中滴加BaCl2溶液,红色逐渐褪去,说明BaCl2溶液显酸性 |
| D.上图电池放电时的正极反应式:2Li++Li2O2+2e—=2Li2O |
25℃时,下列叙述正确的是
| A.NH4HSO4溶液中滴加NaOH溶液至pH=7,则c(Na+)=2c(SO42-) |
| B.0.1 mol·L-1CH3COOH溶液与0.1 mol·L-1CH3COONa等体积混合pH<7,则c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) |
| C.AgCl在水中溶解度与在稀盐酸中溶解度相同 |
| D.KNO3溶液和CH3COONH4溶液pH均为7,则两溶液中水的电离程度相同 |
常温下,下列关系正确的是
| A.新制氯水中加入固体NaOH:c(Na+) = c(Cl−) + c(ClO−) + c(OH−) |
| B.pH = 8.3的NaHCO3溶液:c(Na+)>c(HCO3−)>c(CO32−)>c(H2CO3) |
| C.0.2mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合:2c(H+) – 2c(OH−) = c(CH3COO−) – c(CH3COOH) |
| D.向硝酸银溶液中逐滴滴加物质的量浓度相等的氯化钾和铬酸钾的混合溶液,若先产生白色的氯化银沉淀,则有:Ksp(AgCl)<Ksp(Ag2CrO4) |
在含有Ag+的酸性溶液中,以铁铵矾NH4Fe( SO4)2作指示剂,用KSCN的标准溶液滴定Ag+。已知:AgSCN(白色s) Ag++SCN-,Ksp=1.0×10-12;Fe3++SCN-
Ag++SCN-,Ksp=1.0×10-12;Fe3++SCN- [Fe(SCN)]2+(红色),K=138
[Fe(SCN)]2+(红色),K=138
下列说法中不正确的是
| A.边滴定,边摇动溶液,溶液中首先析出AgSCN白色沉淀 |
| B.当溶液出现红色且半分钟不褪色时即为滴定终点 |
| C.上述实验可用KC1标准溶液代替KSCN的标准溶液滴定Ag+ |
| D.滴定时,必须控制溶液的pH,防止Fe3+水解,影响终点的观察 |
试题篮
()