图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4/H2O2燃料电池,则下列说法正确的是
A.图2电池放电过程中,Na+从正极区向负极区迁移
B.图2电池负极区的电极反应为BH4-― 8e-+ 8OH-=BO2-+ 6H2O
C.若用硫酸钠和酚酞的混合溶液浸湿滤纸,用导线将a、b直接相连,则铅笔芯C点处出现红色
D.若用KI淀粉溶液浸湿滤纸,用导线将a、b与A、B电极相连,铅笔芯C点处出现蓝色,则b接的是A电极
下列说法正确的是( )
| A.燃料电池是一种高效但是会污染环境的新型电池 |
| B.锌锰干电池是二次电池 |
| C.化学电池的反应基础是氧化还原反应 |
| D.电池工作时电流由负极流向正极 |
把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a、b相连时,a为负极;c、d相连时,电流由d到c;a、c相连时,c极上产生大量气泡,b、d相连时,b上有大量气泡产生,则四种金属的活动性顺序由强到弱的为
| A. a > b > c > d | B. c > a > b > d |
| C. a > c > d > b | D. b > d > c > a |
“嫦娥一号”卫星上使用的一种高能电池——银锌蓄电池,其电池的电极反应式为:
Zn-2e-+2OH―=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-。据此判断氧化银是
| A.负极,被氧化 | B.正极,被还原 | C.负极,被还原 | D.正极,被氧化 |
观察下图,下列说法正确的是
| A.断开S1,闭合S2,C电极上发生的反应为O2+4e-+4H+=2H2O |
| B.断开S1,闭合S2,Fe电极作原电池的负极,发生还原反应。 |
| C.闭合S1,断开S2,溶液中的Cl- 向C电极方向移动。 |
| D.闭合S1,断开S2,阳极本身失电子,被氧化。 |
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验中,不考虑两球的浮力变化)
| A.杠杆为导体或绝缘体时,均为A端高B端低 |
| B.杠杆为导体或绝缘体时,均为A端低B端高 |
| C.当杠杆为导体时,A端低B端高;杠杆为绝缘体时,A端高B端低 |
| D.当杠杆为导体时,A端高B端低;杠杆为绝缘体时,A端低B端高 |
一种新型燃料电池,用两根金属Pt作电极插入KOH溶液中,然后向两极分别通入甲烷和氧气,其电极反应式为X极:CH4+10OH--8e-=CO32—+7H2O; Y极:4H2O+2O2+8e-=8OH-。下列关于此燃料电池的说法中,错误的是
| A.X为负极,Y为正极 |
| B.该电池工作时,X极附近溶液的碱性增强 |
| C.在标准状况下,通入 5.6 L O2完全反应后,有1 mol电子发生转移 |
| D.工作一段时间后,KOH的物质的量减少 |
下列各组材料中,不能组成原电池的是
| |
A |
B |
C |
D |
| 两极材料 |
锌片、铜片 |
锌片、石墨 |
铜片、银片 |
铁片、铜片 |
| 插入溶液 |
乙醇溶液 |
硫酸溶液 |
硝酸银溶液 |
稀盐酸 |
某研究组设想以如图所示装置用电化学原理生产硫酸。关于该装置的叙述正确的是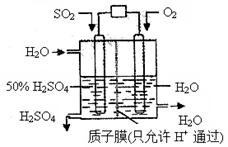
| A.该装置为原电池,通入O2的电极是负极 |
| B.该装置中,通入SO2的电极的电极反应式为:SO2+O2-+H2O -2e- =2H++SO42- |
| C.该装置中,H+通过质子膜向左侧移动 |
| D.在标准状况下,理论上每消耗11.2L SO2,则可产生0.5mol H2SO4 |
如图是锌片和铜片同时插入稀硫酸中所组成的原电池装置,c、d为两个电极。则下列有关的判断不正确的是( )
| A.d为负极,发生氧化反应 |
| B.c为锌片,电池工作时,溶液中SO42-向c移动 |
| C.电池工作的过程中,d电极上产生大量的气泡 |
| D.电池工作的过程中,溶液中SO42-浓度基本不变 |
有A、B、C、D四种金属,常温下只有C能和水反应生成氢气,B与A用导线相连插入稀硫酸形成原电池时,A电极附近有气泡产生,A能从D的硝酸盐溶液中能把D置换出来,则四种金属活泼性从强到弱的顺序是( )
A. C>B>A >D B. C>D>A>B C. C>A>B>D D. D>C>B>A
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列“水” 电池在海水中放电时的有关说法正确的是( )
| A.正极反应式:Ag+Cl--e-=AgCl | B.每生成1 mol Na2Mn5O10转移2 mol电子 |
| C.Na+不断向“水”电池的负极移动 | D.AgCl是还原产物 |
试题篮
()