下表是氯化钠和硝酸钾在不同温度时的溶解度,根据此表回答:
| 温度(℃) |
20 |
30 |
40 |
50 |
60 |
|
| 溶解度(g/100g水) |
NaCl |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
| KNO3 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
(1)20℃时,NaCl的溶解度是 g/100g水;
(2)t℃时,NaCl和KNO3的饱和溶液溶质质量分数相同,该温度范围是 。
a、20℃~30℃ b、30℃~40℃ c、40℃~50℃ d、50℃~60℃
(3)某同学进行了如下实验,溶液a的质量分数是 ,在此过程中一定是饱和溶液的是 (填溶液编号),x的取值范围是 。
水是重要的资源。
(1)活性炭常用于净水,其作用是 。
(2)海水晒盐得粗盐,粗盐提纯的实验步骤为:溶解、 、蒸发结晶。
(3)水是一种重要的溶剂,(如图1)是硝酸钾和氯化钠的溶解度曲线。
①图中A点表示的含义是 。
②20℃,向50g水中加入25g NaCl,得到 溶液(填“饱和”或“不饱和”);若要增大该溶液中溶质的质量分数,其方法是 。
(4)水在化学实验中具有重要作用,将光亮的铁丝固定在U型管左端的塞子上(如图2),几天后,观察到的实验现象为 ;从实验中可以得出铁生锈的条件是 。
某化学兴趣小组的同学在20℃时进行了如图l所示实验.已知,图2是KNO3的溶解度曲线.
(1)50℃时,l00g水最多可溶解硝酸钾的质量为 g.
(2)充分搅拌后,可观察到:A中无剩余固体,B中 .
(3)A﹣E的溶液中,属于不饱和溶液的是 (填字母,下同).A﹣E的溶液中,溶质质量分数相等的是 .
溶解度是物质溶解性的定量表示,溶解度曲线可表示物质在不同温度下的溶解度。甲、乙两种物质的溶解度曲线如图所示,根据图示回答下列问题:

(1)甲、乙两种物质中溶解度受温度影响较大的是 物质。
(2)若甲物质中混有少量的乙物质,提纯甲物质最好采取的方法是 (填“降温结晶”或“蒸发结晶”)。
(3)t2℃时,乙物质的溶解度为 g;t2℃时,若将30g乙物质加入到50g水中,所得溶液的溶质质量分数是 (计算结果精确到0.1%)。
(4)将t1℃的甲、乙两物质的饱和溶液(均无固体物质剩余)升温到t2℃时,所得甲物质溶液的溶质质量分数 乙物质溶液的溶质质量分数(填“大于”“小于”“等于”之一)。
下表是KNO3 、NaCl在不同温度下的部分溶解度数据(单位:g/100g水),请回答问题:
| 温度(℃) |
10 |
20 |
40 |
60 |
80 |
| KNO3 |
20.9 |
31.6 |
63.9 |
110 |
169 |
| NaCl |
35.8 |
36 |
36.6 |
37.3 |
38.4 |
(1)10℃时,KNO3 溶解度是 g/100g水。
(2)以上两种物质溶解度变化受温度影响较小的是 。
(3)40℃时,将70gKNO3固体加入100g水中,充分搅拌,形成的溶液质量为 g。
(4)60℃时,KNO3的饱和溶液中含有少量NaCl,通过 方法获得较纯净的KNO3晶体。
(5)根据表中数据,请在坐标图中描点、绘制符合KNO3溶解度变化规律的曲线 。
(6)向20mL水中溶解一定量KNO3固体的操作如右图:请根据实验现象和溶解度数据回答:A、B、C中
溶液一定是饱和溶液的是 ,一定是不饱和溶液的是 。当x = g
时,B中恰好没有固体剩余。
请根据以下实验,回答问题。
| 步骤 |
实验操作 |
实验结果 |
| 1 |
取50克水,加入10gKNO3,搅拌,恢复到20℃ |
全部溶解,得溶液a |
| 2 |
再加5.8g KNO3,搅拌,恢复到20℃ |
恰好饱和,得溶液b |
| 3 |
再加10gKNO3,搅拌,恢复到20℃ |
得溶液c |
| 4 |
加热 |
全部溶解,得溶液d |
| 5 |
冷却到20℃ |
析出晶体,得溶液e |
①上述所得溶液c的质量为 (15) g;
②20℃时,KNO3的溶解度为 (16) g/100g水;
③上述溶液a~e中,无法判断是否饱和的是 (17) (填溶液序号,下同),溶质质量分数一定相等的是(18) ;
④步骤5中,析出晶体的质量为 (19) g。
向装有等量水的A、B、C三个烧杯中分别加入10g、25g、25g NaNO3固体,充分溶解后,现象如图1所示.
(1)烧杯中的溶液一定属于饱和溶液的是 (填序号).
(2)在图2中,能表示NaNO3溶解度曲线的是 (填“甲”或“乙”).
(3)要使烧杯B中剩余固体继续溶解,可采用的方法是 (填一种即可).
(4)依据图2的分析判断,若分别将100g甲、乙的饱和溶液从 t2℃降温到 t1℃,对所得溶液的叙述正确的是 (填序号).
A.甲、乙都是饱和溶液 B.所含溶剂的质量:甲<乙
C.溶液的质量:甲>乙 D.溶质的质量分数:甲>乙.
海水淡化可采用膜分离技术.如图一所示,对淡化膜右侧的海水加压,在其左侧得到淡水.其原理是海水中的水分子可以透过淡化膜,而其他各种离子不能透过。
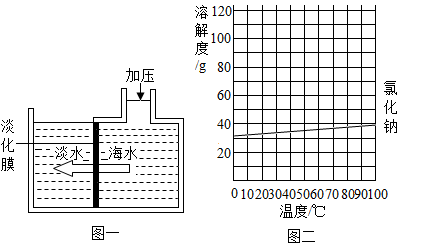
请回答:
(1)采用膜分离技术淡化海水的原理,与化学实验中常见的操作相似。
(2)对淡化膜右侧的海水加压后,海水中溶质的质量分数会(填"增大"、"减小"或"不变")。
(3)海水中含有大量的氯化钠,图二是氯化钠的溶解度曲线,据此可知盐场从海水中得到食盐晶体利用的方法是结晶(填"降温"或"蒸发")。
2012年3月22日是第二十届“世界水日”。水与人类的生活和生产密切相关。
(1)下列做法有助于保护水资源的是 。
A.禁止向河流中排放废水 B.禁止向乱扔垃圾 C.节约用水
(2)水的硬度过大会影响生产和生活,区分软水和硬水常用的物质是 。生活中可以通过________的方法来降低水的硬度。
(3)自来水厂净水过程为:天然水→加絮凝剂→沉降→过滤→吸附→加消毒剂→自来水。通常使用的絮凝剂是 ;X是一种新型的自来水消毒剂,制取X的化学方程式为:C12+2NaClO2=2NaCl+2X,则X的化学式为 。
(4)下图为甲、乙(均不含结晶水)两种固体物质在水中的溶解度曲线。
①溶解度随温度升高而增大的物质是 (填“甲”或“乙”);t1℃时甲的溶解度 乙的溶解度(填“大于”或“小于”或“等于”)。
②某同学在t1℃时开始如下实验,得到相应的溶液A、B、C。
在溶液A、B、C中,属于饱和溶液的是 ;与溶液C质量相等的是 。
在溶液C中再加入25g甲后,充分搅拌,恢复到t2℃,所得溶液的质量为 。
水是生命的源泉,下列变化与水相关。请回答:
①二氧化碳溶于水发生反应的化学方程式是 (1) 。
②自来水厂净水过程中常用到活性炭,其作用是 (2) 。
③铁丝在氧气中燃烧时,集气瓶内放少量水的目的是 (3) 。
④除去粗盐中泥沙等难溶性杂质的实验步骤:

I. 操作a的名称是 (4) ;
II. 三个步骤都用到的玻璃仪器是 (5) 。
⑤甲和乙两种固体物质(不含结晶水)的溶解度曲线如下图所示,回答下列问题:
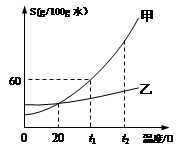
I.在 (6) ℃时,甲和乙两种物质的溶解度相等。
II.t1℃时,将50g固体甲加到50g水中,充分搅拌后所得溶液的质量为 (7) g。
III.甲的饱和溶液中含有少量的乙,由该液体得到固体甲采用的方法是 (8) 。
IV.若将甲物质的不饱和溶液变为饱和溶液,下列说法正确的是 (9) 。
A.溶剂的质量一定变小 B.溶质的质量可能不变
C.溶质的质量分数一定变大 D.溶液的质量变大
⑥下图是对20℃一定质量的丙溶液进行恒温蒸发结晶的实验过程,请回答:
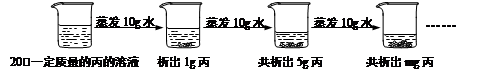
I.蒸发前原溶液是 (10) (填“饱和”或“不饱和”)溶液;m的数值是 (11) 。
II.依据上述实验,你认为丙的溶解度随温度变化的趋势是 (12) (填字母)。
A.随温度升高而增大 B.随温度升高而减小 C.无法判断
甲、乙、丙三种物质的溶解度曲线如图所示.据图回答:

30℃时,甲、乙、丙三种物质的溶解度由大到小的顺序为 ;要使接近饱和的丙物质溶液变为饱和,可采取的一种措施是 ;50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃时,析出晶体最多的是 ,所得溶液中溶质质量分数最小的是 [50℃时,30g乙物质加入到50g水中不断搅拌,所得溶液的质量是 .
如图是
,
,
三种固体物质的溶解度曲线,请回答下列问题:

(1)
点的含义是;
(2)若
点混有少量
时,可采用的方法提纯
;
(3)
℃时,能不能配制溶质的质量分数为40%的
溶液?(填"能"或"不能");
(4)
℃时,将
,
,
三种固体物质各30
加入到100
水中,充分溶解,形成不饱和溶液的是;
(5)将
℃时
,
,
三种固体物质的饱和溶液升温到
℃,其溶质的质量分数由大到小的顺序是。
20℃时,将等质量的甲、乙两种固体(不含结晶水),分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1所示,加热到50℃时现象如图2所示,甲、乙两种物质的溶解度曲线如图3所示。

请回答下列问题:
(1)图1中一定是饱和溶液的是溶液(填"甲"或"乙");图2中乙溶液一定是溶液(填"饱和"或"不饱和")。
(2)图3中表示乙的溶解度曲线的是(填"M"或"N");图2中乙溶液降温至30℃析出晶体(填"会"或"不会")。
(3)50℃时甲的饱和溶液中溶质质量分数为(计算结果精确到0.1%)。
分析处理图表中的信息是学习化学的一种重要方法。
(1)表3是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答:

① 40
时,氯化钠的溶解度为g。
②碳酸钠的溶解度随温度的升高而(填"增大"或"减小")。在20
时,将100g的水加入30 g碳酸钠中,充分搅拌后得到的是(填"饱和溶液"或"不饱和溶液"),将上述溶液升温到30度,该溶液的溶质质量分数为(计算结果精确到0.1%)。
③10
时,分别配制表中两种物质的饱和溶液,其中溶质质量分数较小的物质是。
(2)将足量的稀盐酸加入一定量的铁、铜混合物中,写出其中反应的化学方程式。图7是实验过程生成气体或剩余固体的质量随反应时间的变化关系,其中表示正确的是(填标号)。

A图为实验示意图,在室温情况下,烧杯中盛装的是甲物质的溶液,试管①中盛装的是乙物质的溶液,试管②中盛装的是丙物质的溶液。当它们由室温升到80℃时,发现烧杯中甲物质没有明显变化,而试管①中盛装的是乙物质全部溶解,试管②中有丙物质析出。B图表示三种物质的溶解度曲线。请你据此现象回答下列有关问题:
(1)室温时, (选填“烧杯”、“试管①”或“试管②”)中 溶液可能是不饱和溶液;
(2)上图能表示甲物质的溶解度曲线的是 (选填a、b或c);
(3)若乙物质溶液中混有少量的甲物质,提纯乙物质可采取的方法是
(4)对于甲、乙两物质饱和溶液,在温度 时,乙物质的溶质质量分数一定比甲物大.
试题篮
()