甲、乙两种固体物质的溶解度曲线如图所示:

(1)温度大于20℃时,甲物质的溶解度(填"<"">"或"=")乙物质的溶解度.
(2)40℃时,若将20g乙物质(不含结晶水)放入40g水中充分溶解,所得溶液中溶质的质量分数为(结果保留到0.1%).
(3)40℃时,将甲、乙两种物质的饱和溶液各100g降温至20℃,析出晶体(均不含结晶水)较多的物质是.
(4)如果甲物质中含有少量乙物质,应该采用方法提纯甲物质.
、
、
三种固体物质在水中的溶解度曲线如图所示,请回答:

(1)℃时,
、
两种物质在100
水中达到饱和状态时溶解的质量相等;
(2)若
中混有少量的
,最好采用的方法提纯
;
(3)现有接近饱和的
物质溶液,使其变成饱和溶液的方法有:①加入
物质;②恒温蒸发溶剂;③;
(4)
℃时将20
物质放入50
水中,充分搅拌,所得溶液中溶质的质量分数是;
(5)将
℃时等质量的
、
、
三种物质的饱和溶液降温至
℃时,所得溶液的质量由大到小的顺序是。
水和溶液在生产生活中重要的作用.
(1)自来水厂常用的净水方法有沉淀、吸附、消毒等;在日常生活中常用来降低水的硬度的方法是;水是一种宝贵的自然资源;我们必须爱护水资源.预防水污染的措施有(写一条即可).
(2)如图是甲、乙两种物质的溶解度曲线,回答下列问题:

①时,甲、乙两种物质的溶解度相等;
②若固体甲中含有少量乙时可用方法提纯甲(填"蒸发结晶"或"冷却结晶");
③
用等质量的甲、乙两种物质配置甲、乙的饱和溶液需要水的质量甲乙(填">""<"或"=");
④配置一定溶质质量分数的甲物质溶液,以下操作中会导致所配置溶液溶质质量分数偏低的是.
| A. |
量筒量取水时仰视读数 |
B. |
配合的溶液向细口瓶转移时溅出 |
C. |
固体甲中含有杂质 |
如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是()

| A. | 时,甲、乙两种物质的饱和溶液中溶质质量一定相等 |
| B. | 时,甲的溶解度大于乙的溶解度 |
| C. | 甲中含有少量乙,可以用冷却热饱和溶液的方法提纯甲 |
| D. | 时,向 甲固体中加入 水,充分搅拌后能得到 溶液 |
如图是甲、乙两固体物质的溶解度曲线,下列说法错误的是

| A. | 10 时,甲的溶解度小于乙的溶解度 |
| B. | 时,甲乙两物质的溶解度相等 |
| C. | 使甲物质从其饱和溶液中析出,可采取降温的方法 |
| D. | 甲、乙的饱和溶液从30 降温到10 时,析出的晶体质量甲一定大于乙 |
科学研究中常用图象来表示两个量(
)之间的关系,以使研究的间压变得直观明了.在某温度下.将少量氧化钙加入到一定量的饱和氢氧化钙溶液中.图甲表示整个过程中温度的变化,图乙表示氢氧化钙的溶解度与温度的关系.小阳同学要挟据观察和思考,作出了如图丙所示的图象,此图象反映了该过程中( )

| A. | 溶质的质量与时间的关系 |
| B. | 溶剂的质量与时间的关系 |
| C. | 溶质的溶解度与时间的关系 |
| D. | 溶质的质量分数与时间的关系 |
如图是A、B、C三种固体物质(固体组成与溶质相同)的溶解度曲线。在t1℃时,将质量为ag的A、B、C三种物质分别加入100g水中,根据图示回答下列问题: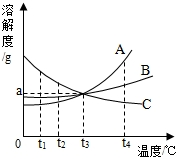
(1)三种物质中,随温度升高溶解度减小的物质是_______;
(2)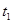 ℃时,所得三种物质的溶液中为不饱和溶液的是_______;
℃时,所得三种物质的溶液中为不饱和溶液的是_______;
(3)若使这三种溶液溶质的质量分数相等,则温度应由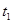 ℃升至 ℃;
℃升至 ℃;
(4)若将温度由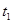 ℃升至
℃升至 ℃时,三种溶液中溶质质量分数的大小关系为 。
℃时,三种溶液中溶质质量分数的大小关系为 。
20℃时,将等质量的甲、乙固体(不含结晶水),分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2(不考虑水分蒸发),甲、乙固体的溶解度曲线如图3.

下列说法正确的是()
| A. | 图1中乙溶液一定不饱和 |
| B. | 图2中两溶液中溶质质量分数一定相等 |
| C. | 图3中 表示甲的溶解度曲线 |
| D. | 图2中两溶液降温至30℃一定都不会析出晶体 |
如图所示,
、
、
为三种物质的溶解度曲线,请根据图示信息回答下列问题。

(1)
℃时,
、
、
三种物质中溶解度最小的是。
(2)
℃时,将20
物质投入100
水中,充分溶解,温度不变,所得溶液为溶液(填"饱和"或"不饱和")。
(3)下列说法正确的是。
| A. |
℃时,将 和 的混合溶液(两者均已达到饱和),降温到 ℃,析出的晶体含有 和 |
B. | 从混有少量 的 物质中提取较纯净的 ,可通过冷却它们的热饱和溶液实现 |
| C. |
℃时,将 、 、 的饱和溶液分别降温到 ℃,所得溶液中溶质质量分数的大小关系是 > > |
D. | ℃时,欲用 的饱和溶液配制10%的 溶液,只需要烧杯、量筒、胶头滴管三种玻璃仪器 |
(4)如图所示,向放有镁条的试管中滴加稀盐酸后,锥形瓶中
的饱和溶液变浑浊。请解释原因。

年,我国著名化学家侯德邦先生创立了侯氏制碱法,促进了世界制碱技术的发展,以从海水中提取出来的食盐为主要原料制取纯碱.其生产过程中有下列反应:①
;②
;

试回答下列问题:
(1)在反应①的六种物质中,焙制糕点是时常用作发酵粉的是;
(2)胺盐水比食盐水更容易吸收二氧化碳的原因是.
(3)氯化钠和碳酸钠的溶解度如图
,
时,氯化钠饱和溶液溶质的质量分数碳酸钠饱和溶液溶质的质量分数(填"大于""小于""等于"之一).
(4)生活在盐碱湖附近的人们有一句谚语"夏天晒盐,冬天捞碱",请结合溶解度曲线,说明这句谚语的原理:.
如图是甲、乙两种固体物质的溶解度曲线.

(1)由图中可看出,甲乙两物质中,溶解度受温度影响较大的物质是;
(2)要使甲的饱和溶液变为不饱和溶液,可采取的方法是(写出一种即可);
(3)
℃时,将甲、乙各20
分别加入到两只盛有100
水的烧杯中,充分搅拌,所得乙溶液为溶液(填"饱和"或"不饱和");若将温度都降低到
℃,甲溶液中溶质的质量分数(填">"、"<"或"=")乙溶液中溶质的质量分数.
如图是甲、乙两种固体物质的溶解度曲线.

(1)在
时,甲、乙两种固体物质的溶解度(填相等或不相等);
(2)把甲物质的不饱和溶液变成饱和溶液,下列有关说法正确的是(填字母序号);
| A. |
溶剂的质量一定变小 |
| B. |
溶质的质量一定不变 |
| C. |
溶质的质量分数一定变大 |
| D. |
溶液的质量可能不变 |
| E. |
该饱和溶液还可以溶解其他物质 |
(3)在实验室中,用固体物质甲和水配制成一定溶质质量分数的溶液,需用到的仪器有:托盘天平、烧杯、药匙、胶头滴管和.
下图是 两种固体物质的溶解度曲线.下列说法正确的是()

| A. | 的溶解度大于 的溶解度 |
| B. | 的不饱和溶液由 ℃降低至 ℃时,变成饱和溶液 |
| C. | 阴影部分各点对应的溶液(不包括曲线上的点)是 的不饱和溶液, 的饱和溶液 |
| D. | ℃时,两物质各10克分别加水至恰好溶解,所得饱和溶液质量是 小于 |
在20℃时,刘冰同学向 水中依次加入 固体,充分溶解.实验过程如图所示.下列说法错误的是()
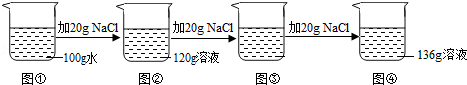
| A. | 20℃时, 的溶解度为 |
| B. | 图②中的溶液是不饱和溶液 |
| C. | 图③中溶液的溶质质量为 |
| D. | 图③和图④中 溶液的溶质质量分数相等 |
如图为A、B、C三种物质的溶解度曲线。
(1)t2℃时,A、B、C三种物质的溶解度由大到小顺序是________;
(2)m点的含义是:_______
(3)20℃时,将30g A物质放入50g水中,充分搅拌,所得溶液质量为____g;
(4)t2℃时,将等质量的A、B、C饱和溶液分别降温到00C时,析出溶质最多的是________,无溶质析出的是________;
试题篮
()