某兴趣小组取CaCO 3和CaCl 2的固体混合物7.5g,加入到盛有一定质量某浓度稀盐酸的烧杯中,恰好完全反应,气体全部逸出后,所得不饱和溶液的质量为41.8g。
烧杯及烧杯内物质质量随反应时间变化如表。
| 反应时间 |
0 |
t 1 |
t 2 |
t 3 |
| 烧杯及烧杯内物质质量 |
64 |
62.9 |
61.8 |
61.8 |
计算:
(1)生成CO 2的质量为 g。
(2)烧杯中原有稀盐酸的溶质质量分数是多少?
(1)探究小组欲从含有FeCl3、CuCl2的废液中回收金属铜,取一定量的废液样品加入少量铁粉,一段时间后铁粉完全溶解,但未发现红色固体沉积。
出现这种现象的可能原因是 ;
经查阅资料,铁粉在废液中发生两个化学反应:
①2FeCl3+Fe═3FeCl2②CuCl2+Fe═FeCl2+Cu
(2)探究小组另取废液,向废液中加入一定且足量的铁粉至充分反应,溶液变为浅绿色,过滤、干燥,称得固体沉积物质量与加入铁粉质量相等。
①固体沉积物质量与加入铁粉质量相等的原因是 ;
②经测定,反应后得到铜的质量为1.6g,其中,反应①消耗铁粉的质量是 ,反应②消耗铁粉的质量是 (计算结果精确到0.1)。
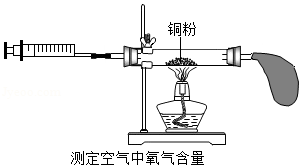
甲、乙、丙三个实验小组分别利用2g铜粉"测定空气中氧气的含量",实验装置见图。课外兴趣小组为研究实验中铜粉的氧化情况,又进行以下实验:
①兴趣小组将甲、乙、丙三个实验小组硬质玻璃管中的残留固体全部取出,称量后,置于烧杯中;
②在烧杯中加入足量稀硫酸使之充分反应,将剩余固体过滤、洗涤、干燥、称量;相关数据见下表:
| |
甲组 |
乙组 |
丙组 |
| 反应前固体质量 |
2.016g |
2.016g |
2.024g |
| 反应后固体质量 |
1.936g |
1.936g |
1.904g |
(1)烧杯中发生反应的化学方程式为 ;
(2)甲、乙两组实验数据相同,残留固体中氧化铜的质量为 ,丙组残留固体中氧化铜的质量为 。
(3)兴趣小组通过分析数据得出:甲、乙两组实验数据更接近实际空气中氧气的含量,丙组差异较大。你认为丙组在"测定空气中氧气的含量"实验中,可能存在的操作失误是 。
铝与氢氧化钠溶液反应时生成偏铝酸钠( NaAlO2)和氢气,反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑.向20g氢氧化钠溶液中加入足量的铝,充分反应后生成0.3g的氢气。
求:该氢氧化钠溶液中溶质的质量分数。
海水中蕴藏着丰富的资源,海水“晒盐”过程中可得到粗盐和卤水.粗盐中常含有多种杂质,必须对其分离和提纯,才能用于生产和生活;卤水经常用作工业制镁的原料.
(1)实验室除去粗盐中不溶性杂质的实验步骤为:溶解、过滤、蒸发结晶.在三步中都要用到的一种玻璃仪器是 .
2杂质,得到较为纯净的食盐晶体.请简述实验操作步骤: .
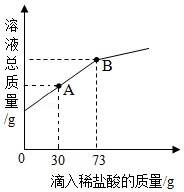
22的混合粉末6g,向其中加入20g水,经充分溶解后,再逐滴加入溶质质量分数为10%的稀盐酸.烧杯中溶液的溶液的总质量与加入稀盐酸的质量关系如图所示,请回答下列问题:
①当滴入稀盐酸30g时(即图中A点时),烧杯内溶液中的溶质是 (填写化学式).
②当滴入稀盐酸73g时(即图中B点时),试通过计算,求此温度时所得不饱和溶液中溶质的质量(计算结果精确至0.1g).
今天是某校实验室开放日,晓明同学用锌和稀硫酸反应制取氢气.先向气体发生装置中加入一定量的锌粒,然后将60克稀硫酸分三次加入,每次生成气体的质量如下表:
次数 |
第一次 |
第二次 |
第三次 |
加入稀硫酸质量/g |
20 |
20 |
20 |
生成氢气的质量/g |
0.08 |
0.08 |
0.04 |
试计算:
(1)共制得氢气 g.
(2)实验所用稀硫酸中溶质的质量分数.(写出计算过程)
某硫酸厂废水中含有少量的硫酸,技术员检测废水中硫酸的质量分数为1%,现有98t废水,为达标排放,需要加入熟石灰中和至中性。请计算所需熟石灰的质量。
向一定量的澄清石灰水中通入适量的二氧化碳,使氢氧化钙全部转化为碳酸钙沉淀,得到的沉淀质量为1.00g。计算澄清石灰水中氢氧化钙的质量(计算结果精确至0.01g)。
醋的主要成分是醋酸,其化学式为CH3COOH,醋不仅是调味品,而且还有较强的灭菌、抑毒的作用。

小明为判断家中的米醋含酸量是否合格,取100mL米醋(见标签)于锥形瓶中,然后再向锥形瓶中逐渐加入一定溶质质量分数的碳酸氢钠溶液,反应过程中,当加入碳酸氢钠溶液的质量至以下数值时,对充分反应后锥形瓶中剩余物质的质量进行了记录,测得的部分数据如下,请根据有关信息回答问题(提示:化学方程式为:CH3COOH+NaHCO3═CH3COONa+H2O+CO2↑)
加入碳酸氢钠溶液质量(g) |
25 |
50 |
100 |
155 |
175 |
锥形瓶内剩余物质质量(g) |
123.9 |
147.8 |
195.6 |
248.4 |
m |
(1)醋酸中碳、氢、氧三种元素的质量比为 。
(2)100mL米醋与足量碳酸氢钠溶液反应产生的二氧化碳质量为 g,表中m的数值为 。
(3)请通过计算判断该产品含酸量是否合格?(写出计算过程)
某袋装食品的脱氧剂由活性炭、铁粉和食盐混合而成,三者质量比为2:2:1.现用该脱氧剂进行实验,回答下列问题:
(1)将该脱氧剂加入盐酸中,发生反应的化学方程式为 。
(2)打开失效的脱氧剂小袋,发现里面出现了红褐色物质,该物质的主要成分是 (填化学式)。5.0g未经使用的该脱氧剂最多能够吸收氧气 g。
(3)用电子秤称取7.20g完全失效后的脱氧剂放入烧杯中,加入足量稀硝酸,充分溶解后过滤,滤渣为黑色粉末。向所得滤液中加入足量AgNO3溶液,充分反应产生的沉淀质量为2.87g。列式计算该失效脱氧剂中NaCl的质量分数(计算结果精确到0.1%)。
化学兴趣小组要测定制作叶脉书签所用氢氧化钠溶液的浓度。取40g该氢氧化钠溶液于锥形瓶中,加入数滴酚酞溶液后再滴加质量分数为10%的稀硫酸,当锥形瓶中液体由红色恰好变成无色时,消耗稀硫酸的质量为49g。试计算该氢氧化钠溶液中溶质的质量分数。
硫酸亚铁在工农业生产中有重要用途,也有较高的医用价值。工业上用废铁屑和含硫酸的废液来制取硫酸亚铁,变废为宝。现用5.6t铁屑与100t废液恰好完全反应(已知铁屑只和废液中的硫酸反应),请你计算:
(1)可生成硫酸亚铁的质量;
(2)所用废液中硫酸的溶质质量分数。
小滨同学为了测定某珍珠粉中碳酸钙的质量分数,称取12.5g珍珠粉样品,进行四次高温煅烧、冷却、称量剩余固体的重复操作(杂质不参加反应),记录数据如下:
操作次数 |
第1次 |
第2次 |
第3次 |
第4次 |
剩余固体质量(g) |
10.8 |
9.6 |
8.1 |
8.1 |
试计算:
(1)完全反应后生成二氧化碳的质量是 g.
(2)求珍珠粉中碳酸钙的质量分数.
为测定某赤铁矿中Fe2O3的含量,取10g该赤铁矿样品于烧杯中,向其中加入100g稀盐酸,恰好完全反应,测得剩余固体的质量为2g。(杂质不溶于水也不与酸反应)
请完成下列分析及计算:
(1)10g样品中杂质的质量为 g。
(2)计算稀盐酸中溶质的质量分数。
试题篮
()