铅蓄电池的工作原理为Pb+PbO2+2H2SO4 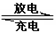 2PbSO4+2H2O ,
2PbSO4+2H2O ,
根据下图,下列判断不正确的是( )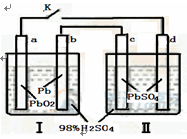
| A.K 闭合时,d电极反应式:PbSO4+2H2O-2e-= PbO2+4H++SO42- |
| B.K闭合时,Ⅱ中SO42-向d电极迁移 |
| C.当电路中转移0.2mol电子时,Ⅰ中消耗的H2SO4为0.4 mol |
| D.K闭合一段时间后,Ⅱ可单独作为原电池,d电极为正极 |
据报道,我国拥有完全自主产权的氢氧燃料电池车在北京奥运会期间为运动员提供服务.某种氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是
| A.正极反应式为:O2+2H2O+4e-==4OH- |
| B.工作一段时间后,电解液中KOH的物质的量不变 |
| C.该燃料电池的总反应方程式为:2H2+O2==2H2O |
| D.用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.1 mol电子转移 |
下列有关电池的说法不正确的是
| A.手机上用的锂离子电池属于二次电池 |
| B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 |
| C.氢氧燃料电池可把化学能转化为电能 |
| D.锌锰干电池中,锌电极是负极 |
已知铅蓄电池的充放电过程:Pb(s)+PbO2(s)+2H2SO4(aq) 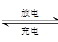 2PbSO4(s)+2H2O(l),则下列说法不正确的是( )
2PbSO4(s)+2H2O(l),则下列说法不正确的是( )
| A.放电时Pb为负极发生氧化反应生成PbSO4,负极质量减少 |
| B.放电时正极:PbO2+4H++2e-+ SO42-=PbSO4+2H2O,正极质量增加 |
| C.充电时蓄电池的负极接外电源负极:PbSO4(s) +2e- = Pb(s) + SO42- |
| D.充电时蓄电池的正极接外电源正极:PbSO4 (s)+2H2O -2e- = PbO2(s) + 4H++ SO42- |
下列化学电池不易造成环境污染的是
| A.甲烷燃料电池 | B.锌锰电池 | C.镍镉电池 | D.锂电池 |
下列有关电池的说法不正确的是
| A.手机上用的锂离子电池属于二次电池 |
| B.铅蓄电池放电时,负极的质量逐渐减小 |
| C.氢氧燃料电池可把化学能转化为电能 |
| D.锌锰干电池中,锌电极是负极 |
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O Cd(OH)2 + 2Ni(OH)2有关该电池的说法正确的是
Cd(OH)2 + 2Ni(OH)2有关该电池的说法正确的是
| A.充电时阳极反应:Ni(OH)2-e-+ OH- =" NiOOH" + H2O |
| B.充电过程是化学能转化为电能的过程 |
| C.放电时负极附近溶液的碱性不变 |
| D.放电时电解质溶液中的OH-向正极移动 |
汽车的启动电源常用铅蓄电池。放电时的电池反应如下:
PbO2 + Pb + 2H2SO4  2PbSO4↓+ 2H2O,根据此反应判断下列叙述中正确的( )
2PbSO4↓+ 2H2O,根据此反应判断下列叙述中正确的( )
| A.PbO2是电池的负极 |
B.负极的电极反应式为:Pb + SO - 2e— - 2e— PbSO4↓ PbSO4↓ |
| C.PbO2得电子,被氧化 |
| D.电池放电时,溶液酸性增强 |
汽车的启动电源常用铅蓄电池,放电时的电池反应如下:Pb+ PbO2 + 2H2SO4 2PbSO4 + 2H2O根据此反应判断下列叙述中正确的是
2PbSO4 + 2H2O根据此反应判断下列叙述中正确的是
| A.放电时PbO2是电池的负极 |
| B.放电时,负极的电极反应式为:Pb+SO42--2e-=PbSO4 |
| C.放电时,溶液中的H+向正极区移动,正极区域的溶液的酸性增强 |
| D.充电时,该电池的正极接电源的负极 |
在碱性锌锰干电池中,已知氢氧化钾为电解质,发生的电池总反应为:Zn+2MnO2+2H2O===2MnOOH+Zn(OH)2。下列该电池的电极反应,正确的是
| A.负极反应为Zn-2e-===Zn2+ |
| B.负极反应为Zn+2H2O-2e-===Zn(OH)2+2H+ |
| C.正极反应为2MnO2+2H2O+2e-===2MnOOH+2OH- |
| D.正极反应为2MnO2+2H++2e-===2MnOOH |
下列叙述不正确的是
| A.太阳能蓄电池只是将太阳能直接转化为电能的装置 |
| B.燃料电池是将化学能直接转化为电能的装置,所以能量利用率高 |
| C.碱性Zn-Mn干电池比酸性Zn-Mn干电池耐用,且不易漏液 |
| D.手机上用的锂离子电池属于二次电池 |
试题篮
()