根据下面三个化学方程式判断有关物质的性质比较正确的是
①I2+SO2+2H2O=H2SO4+2HI ②2FeCl2+Cl2 = 2FeCl3 ③2FeCl3+2HI= 2FeCl2+2HCl+I2
| A.氧化性:I2> H2SO4>Cl2> Fe3+ | B.还原性:Cl->Fe2+>SO2>I- |
| C.氧化性:Cl2> Fe3+ >I2> H2SO4 | D.还原性:SO2> Fe2+ > I- >Cl- |
利用下图装置进行实验(必要时可加热),不能得出相应结论的是
| |
溶液① |
固体② |
溶液③ |
实验结论 |
 |
| A |
稀硫酸 |
Na2CO3 |
Na2SiO3 |
非金属性:C>Si |
|
| B |
浓盐酸 |
MnO2 |
Na2S |
氧化性:Cl2>S |
|
| C |
盐酸 |
CaCO3 |
C6H5ONa |
酸性:碳酸>苯酚 |
|
| D |
稀硫酸 |
Na2CO3 |
CaCl2 |
CO2不与氯化钙反应 |
已知 2Fe3+ +2I-=2Fe2+ +I2 、 2Fe2+ +Cl2=2Fe3+ +2Cl-;则有关离子的还原性由强到弱的顺序为( )
| A.Cl->Fe2+>I- | B.Fe2+>I->Cl- | C.I->Fe2+>Cl- | D.Fe2+>Cl->I- |
溶液中可发生以下反应:①16H++10Z +2XO
+2XO =2X
=2X +5Z2+8H2O,②2M
+5Z2+8H2O,②2M +R2=2M
+R2=2M +2R-,③2R-+Z2=R2+2Z-由此判断下列说法错误的是
+2R-,③2R-+Z2=R2+2Z-由此判断下列说法错误的是
A.氧化性强弱: <Z2 <R2 <M <Z2 <R2 <M |
B.还原性强弱:X <Z <Z <R <R <M <M |
| C.Z元素在反应①中被氧化,在③中被还原 |
| D.常温下可发生反应2M2++Z2=2M3++2Z- |
已知:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O,MnO2+4HCl MnCl2+Cl2↑+2H2O。其中KMnO4和一般浓度的盐酸即可反应,K2Cr2O7需和较浓盐酸(>6 mol·L-1)反应,MnO2需和浓盐酸(>8 mol·L-1)反应。根据以上信息,下列结论中不正确的是 ( )。
MnCl2+Cl2↑+2H2O。其中KMnO4和一般浓度的盐酸即可反应,K2Cr2O7需和较浓盐酸(>6 mol·L-1)反应,MnO2需和浓盐酸(>8 mol·L-1)反应。根据以上信息,下列结论中不正确的是 ( )。
| A.上述反应均属于氧化还原反应 |
| B.生成1 mol Cl2时,三个反应中转移的电子数相等 |
| C.盐酸浓度越大,Cl-的还原性越强 |
| D.氧化性:KMnO4>K2Cr2O7>Cl2>MnO2 |
已知NH4CuSO3与足量的2mol/L硫酸溶液混合微热,产生下列现象:①有红色金属生成 ②产生刺激性气味的气体③溶液呈现蓝色。据此判断下列说法正确的是
A.反应中硫酸作氧化剂 |
B.NH4CuSO3中硫元素被氧化 |
C.1mol NH4CuSO3完全反应转移0.5mol电子 |
D.刺激性气味的气体是氨气 |
已知:(1)H2S+I2=2H++2I—+S¯;(2)H2SO3+2H2S=3S¯+3H2O;(3)2I—+Br2=2Br—+I2;(4)H2SO3+I2+H2O=H2SO4+2HI 。则Br—、I—、H2S和H2SO3还原性由强到弱的顺序是
| A.H2S>H2SO3>I—>Br— | B.Br—>I—>H2SO3>H2S |
| C.H2SO3>H2S>Br—>I— | D.I—>Br—>H2S>H2SO3 |
已知Co2O3在酸性溶液中易被还原成Co2+,且Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。下列反应在水溶液中不可能发生的是( )
| A.2Fe3++2I-===2Fe2++I2 | B.Cl2+FeI2===FeCl2+I2 |
| C.Co2O3+6HCl===2CoCl2+Cl2↑+3H2O | D.3Cl2+6FeI2===2FeCl3+4FeI3 |
根据下列反应的化学方程式,判断有关物质的还原性强弱顺序是( )
I2+SO2+2H2O=H2SO4+2HI
2FeCl2+Cl2=2FeCl3
2FeCl3+2HI=2FeCl2+2HCl+I2
| A.I->Fe2+>Cl->SO2 | B.Cl->Fe2+>SO2>I- |
| C.Fe2+>I->Cl->SO2 | D.SO2>I->Fe2+>Cl- |
常温下,在溶液中可发生以下反应:①2Fe2++ Br2= 2Fe3+ + 2Br-,
②2Br-+ Cl2=Br2 + 2Cl-, ③2Fe3+ + 2I-= 2Fe2++ I2;由此判断下列说法错误的是
| A.铁元素在反应①中被氧化,在③中被还原 |
| B.反应②中当有1 mol Cl2被还原时,有2 mol Br-被氧化 |
| C.氧化性强弱顺序为:Cl2 > I2 > Br2 > Fe3+ |
| D.还原性强弱顺序为:I- > Fe2+ > Br- > Cl- |
已知:①2FeCl3+2KI=2FeCl2+2KCl+I2;②2FeCl2+Cl2=2FeCl3。下列粒子的氧化性从强到弱的顺序正确的是
| A.Cl2>Fe3+>I2 | B.I2>Cl2>Fe3+ |
| C.Fe3+>Cl2>I2 | D.Cl2>I2>Fe3+ |
碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种微粒之间有如图所示关系,根据图示转化关系推测下列说法不正确的是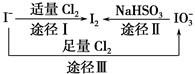
| A.可用KI淀粉试纸和食醋检验加碘盐中是否含有碘 |
| B.足量Cl2能使湿润的KI淀粉试纸变白的原因可能是: 5Cl2+I2+6H2O===2HIO3+10HCl |
| C.由图可知氧化性的强弱顺序为Cl2>I2>IO3- |
| D.途径Ⅱ中若生成1 mol I2,反应中转移的电子数为10NA |
根据下列反应,可以判断有关物质的氧化性由强到弱的顺序正确的是( )。
①Cl2+2KI=2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2FeCl3+2HI=2FeCl2+2HCl+I2
④H2S+I2=S↓+2HI
| A.H2S>I2>Fe3+>Cl2 | B.Cl2>Fe3+>I2>S |
| C.Fe3+>Cl2>H2S>I2 | D.Cl2>I2>Fe3+>H2S |
试题篮
()