X、Z、Y、W 均为四种金属, 根据下列事实:①X+Y2+=X2++Y;②Z+2H2O(冷水)=Z(OH)2+H2↑;③Z2+的氧化性比X2+弱;④由Y、W电极组成的原电池,电极反应为W2++2e-=W、Y-2e-=Y2+,可知X、Y、Z、W的还原性由强到弱的顺序为 ( )
| A.X﹥Z﹥Y﹥W | B.Z﹥W﹥X﹥Y |
| C.Z﹥Y﹥X﹥W | D.Z﹥X﹥Y﹥W |
制备单质硅时,主要化学反应如下
①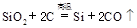 ②
② ③
③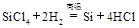 下列对上述三个反应的叙述中,不正确的是( )
下列对上述三个反应的叙述中,不正确的是( )
| A.①③为置换反应 | B.①②③均为氧化还原反应 |
| C.②为化合反应 | D.三个反应的反应物中硅元素均被氧化 |
甲乙两种非金属:①甲比乙容易与H2化合;②甲的氢化物比乙的氢化物稳定③
甲的最高价氧化物对应的水化物的酸性比乙的最高价氧化物对应的水化物酸性强;
④与某金属反应时甲原子得电子数目比乙的多;⑤甲的单质熔沸点比乙的低。能说
明甲比乙的非金属性强的是
| A.只要④ | B.只有⑤ | C.①②③④⑤ | D.①②③ |
下列变化必需加入氧化剂才能实现的是
| A.NH4+→NH3 | B.SO32-→SO42- | C.HNO3→NO | D.CO32-→CO2 |
氯和硫都是重要的非金属元素。下列叙述不能说明氯的非金属性比硫强的是
| A.氯化氢的沸点比硫化氢的沸点高 | B.与氢气反应时,氯气比硫更容易 |
| C.氯气可以从氢硫酸溶液中置换出硫 | D.高氯酸(HClO4)的酸性比H2SO4强 |
甲、乙两种非元素:①甲比乙容易与H2化合;②甲原子能与乙的阴离子发生置换反应;③甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强;④与某金属反应时,甲原子得电子数目比乙的多;⑤甲的单质熔、沸点比乙的低。能说明甲比乙的非金属性强的是( )
| A.只有④ | B.只有⑤ | C.①②③ | D.①②③④⑤ |
根据下列三个反应,判断物质的氧化性由强到弱的顺序正确的是
①2Fe3++2I-=2Fe2++I2
②2Fe2++C12=2Fe3++2C1-
③2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O
| A.Fe3+>C12>MnO4- | B.Fe3+>Cl2>I2 |
| C.I2>Cl2>Fe3+ | D.MnO4->Cl2>Fe3+ |
氢化钙可以作为生氢剂(其中CaH2中氢元素为-1价),反应方程式如下:CaH2+2H2O=Ca(OH)2+2H2↑,其中水的作用是( )
| A.既不是氧化剂也不是还原剂 | B.是氧化剂 |
| C.是还原剂 | D.既是氧化剂又是还原剂 |
已知反应式:①H2S+I2=S↓+2H++2I-②H2SO3+2H2S=3S↓+3H2O
③2I-+Br2=I2+2Br-④H2SO3+I2+H2O=SO42-+2I-+4H+,下列各组中还原性由强到的是( )
| A.H2S 、H2SO3、I-、Br- |
| B.I-、Br-、H2SO3、H2S |
| C.H2S 、I-、Br-、H2SO3 |
| D.I-、Br-、H2S、H2SO3 |
火法炼铜首先要焙烧黄铜矿,其反应为2CuFeS2 + O2 = Cu2S + 2FeS + SO2。下列说法不正确的是
| A.SO2既是氧化产物又是还原产物 | B.CuFeS2仅作还原剂,硫元素被氧化 |
| C.每转移0.8mol电子,有0.2mol硫被氧化 | D.每生成1molCu2S,有1mol硫被氧化 |
氢化钠(NaH)是一种生氢剂,可发生如下反应:NaH+H2O = NaOH+H2↑对这一反应的描述正确的是( )
| A.NaH是氧化剂 | B.NaH是氧化产物 |
| C.NaOH是还原产物 | D.氧化产物与还原产物的质量比是1:1 |
下列物质既具有氧化性又有还原性的是( )
①SO2 ②Fe3+ ③ Fe2+ ④ HCl ⑤ H2O2
| A.①②③ | B.①③ | C.①③⑤ | D.①③④⑤ |
试题篮
()