某溶液中含有Fe2+和I -。为了氧化I -而不使Fe2+被氧化,试根据下列三个反应判断,可选用的氧化剂是( )
①2Fe3++2I-=2Fe2++I2
②2Fe2++Cl2=2Fe3++2Cl-
③2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O
| A.FeCl2 | B.KMnO4 | C.Cl2 | D.FeCl3 |
已知氧化性:Br2>Fe3+>I2;还原性:I->Fe2+>Br-,则下列反应能发生的是( )
| A.I2+2Fe2+===2Fe3++2I- | B.2Br-+I2===Br2+2I- |
| C.2Fe3++2I-===2Fe2++I2 | D.2Fe3++2Br-===2Fe2++Br2 |
已知Co2O3在酸性溶液中易被还原生成Co2+。Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。下列反应在水溶液中不可能发生的是
| A. Co2O3+2Fe2++6H+===2Fe3++2Co2++3H2O |
| B.Cl2+FeI2===FeCl2+I2 |
| C.Co2O3+6HCl===2CoCl2+Cl2↑+3H2O |
| D.3Cl2+6FeI2===2FeCl3+4FeI3 |
已知还原性:Cl—<Br—<Fe2+<I—<SO2,由此判断下列反应必然发生的是
①2Fe3++SO2+2H2O=2Fe2++SO42—+4H+
②I2+SO2+2H2O=4H++ SO42—+2I—
③2Fe2++I2=2Fe3++2I—
④2Br—+4H++ SO42—=SO2↑+Br2+2H2O
| A.①② | B.②③ | C.③④ | D.①④ |
某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4 mL 0.5 mol/L的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式
(2)实验②中化学反应转移电子的物质的量是
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是________________
X、Y、Z为三种单质。已知:Y能将Z从其化合物的水溶液中置换出来,而Z又能将X从其化合物中置换出来。由此可以推断下列说法中可能正确的是
①单质的氧化性:Y>Z>X; ②单质的还原性:Y>Z>X;
③对应离子的氧化性:X>Z>Y;④对应离子的还原性:X>Z>Y
| A.只有① | B.只有②③ | C.只有①④ | D.①②③④ |
以下有关下列三个化学反应的说法不正确的是( )
| A.反应①②③都属于氧化还原反应 |
| B.反应②中氧化剂还原剂均为KClO3,其中氧元素化合价降低 |
| C.反应① H2作还原剂,在反应中被氧化 |
| D.反应①中还原性:H2>Cu |
向含S2—、Fe2+、Br—、I—各0.1mol的溶液中通入Cl2,通入Cl2的体积(标准状况)和溶液中相关离子的物质的量关系图正确的是 :
已知,Fe2+结合S2—的能力大于结合OH—的能力,而Al3+则正好相反,I2的氧化性比S强。在Fe2(SO4)3和AlCl3的混合溶液中,先加入过量的KI溶液,再加入足量的Na2S溶液,所得沉淀是( )
| A.FeS、Al(OH)3和S | B.Fe(OH)3和Al(OH)3 |
| C.Fe2S3和 Al(OH)3 | D.Al2S3、FeS和S |
在一定条件下,下列微粒的还原性顺序为Cl-<Br-<Fe2+<I-<SO2,由此判断以下各反应在溶液中不能发生的是
| A.2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ |
| B.2Fe2++Cl2=2Fe3++2Cl- |
| C.2Br-+4H++SO42-=SO2+Br2+2H2O |
| D.I2+SO2+2H2O=4H++SO42-+2I- |
下列实验操作与预期实验目的或所得实验结论一致的是
| 选项 |
实验操作 |
实验目的或结论 |
| A |
将NaOH溶液滴入该溶液中加热,放出的气体能使湿润的红色石蕊试纸变蓝 |
证明溶液中有NH4+ |
| B |
向某溶液中加入稀盐酸,放出无色刺激性气味气体,将气体通入澄清石灰水,石灰水变浑浊 |
证明该溶液中存在SO32- |
| C |
将Cl2通入品红溶液中,品红溶液褪色 |
证明Cl2的还原性 |
| D |
用硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 |
证明氧化性:H2O2比Fe3+强 |
铜、铁、锌等质量合成的合金W g,加入FeCl3和盐酸的混合液中,充分反应后: (1)若无固体剩余,则溶液中的阳离子一定有 ,还可能有 。
(2)若剩余固体为W/3 g,则溶液中的阳离子一定有 ,可能还有 。一定没有 。
(3)若剩余固体为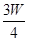 g,则溶液中的阳离子一定有 ,一定没有 .
g,则溶液中的阳离子一定有 ,一定没有 .
下述实验不能达到预期目的的是
| 选项 |
实验目的 |
实验方案 |
| A |
验证Ksp(AgCl)>Ksp(AgI) |
向NaCl溶液中滴加少量AgNO3溶液,产生白色沉淀,再滴加KI溶液,可观察到白色沉淀转化为黄色沉淀 |
| B |
检验Fe(NO3)2晶体是否已氧化变质 |
将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
| C |
验证Br2的氧化性强于I2 |
将少量溴水加入KI溶液中,再加入CCl4,振荡,静置。可观察到下层液体呈紫色 |
| D |
比较确定铜和镁的金属活动性强弱 |
用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液 |
I(1)在淀粉碘化钾溶液中通入少量氯气,立即会看到溶液变蓝色,反应的离子方程式是 。
(2)在碘和淀粉形成的蓝色溶液中通入SO2气体,发现蓝色逐渐消失,反应的离子方程是 。
(3)对比(1)和(2)实验所得的结果,将Cl 、I
、I SO2按还原性由强到弱顺序排列为 。
SO2按还原性由强到弱顺序排列为 。
II .(4) 除去铁粉中混有铝粉的试剂是 ,离子方程式为
(5) 1mol过氧化钠与2mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是
试题篮
()