已知一定温度下,2X(g)+Y(g)  mZ(g) ΔH=-a kJ/mol (a>0),现有甲、乙两容积相等且固定的密闭容器,在保持该温度恒定的条件下,向密闭容器甲中通入2 mol X和1 mol Y,达到平衡状态时,放出热量b kJ;向密闭容器乙中通入1 mol X和0.5 mol Y,达到平衡时,放出热量c kJ,且b>2c,则a、b、m的值或关系正确的是
mZ(g) ΔH=-a kJ/mol (a>0),现有甲、乙两容积相等且固定的密闭容器,在保持该温度恒定的条件下,向密闭容器甲中通入2 mol X和1 mol Y,达到平衡状态时,放出热量b kJ;向密闭容器乙中通入1 mol X和0.5 mol Y,达到平衡时,放出热量c kJ,且b>2c,则a、b、m的值或关系正确的是
| A.m=4 | B.a=b | C.a< | D.m≤2 |
如图所示,甲容器容积固定不变,乙容器有可移动的活塞。甲中充入2 mol SO2和1mol O2,乙中充入4 mol SO3和1mol He,在恒定温度和相同的催化剂条件下,发生如下反应:2SO3(g)  2SO2(g)+ O2 (g)。下列有关说法正确的是
2SO2(g)+ O2 (g)。下列有关说法正确的是
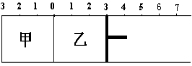
| A.若活塞固定在6处不动,达平衡时甲乙两容器中的压强:P乙=P甲 |
| B.若活塞固定在3处不动,达平衡时甲乙两容器中SO3的浓度: c(SO3)乙>2c(SO3)甲 |
| C.若活塞固定在3处不动,达平衡时甲乙容两器中SO2的体积分数:ψ(SO2)乙>2ψ(SO2)甲 |
| D.若活塞固定在7处不动,达平衡时两容器中SO3的物质的量分数相等 |
图中是可逆反应X2+3Y2 2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是
2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是
| A.t1时,只有正方向反应 |
| B.t1~t2,X2的物质的量越来越多 |
| C.t2~t3,反应不再发生 |
| D.t2~t3,各物质的浓度不再发生变化 |
恒温、恒压下,反应N2 (g)+3H2 (g)  2NH3 (g)从两条途径分别建立平衡:
2NH3 (g)从两条途径分别建立平衡:
Ⅰ.N2、H2的起始浓度分别为1 mol / L和3 mol / L;
Ⅱ.NH3的起始浓度为4 mol / L。下列有关叙述不正确的是:
| A.途径Ⅰ与途径Ⅱ所得混合气体的百分组成相同 |
| B.途径Ⅰ的平衡速率v (N2)与途径Ⅱ的平衡速率v (NH3)的比值为1∶2 |
| C.途径Ⅰ所得NH3的浓度与途径Ⅱ所得NH3的浓度之比为1∶2 |
| D.途径Ⅰ与途径Ⅱ所得平衡混合气体的物质的量之比为1∶2 |
SO2的催化氧化反应(2SO2+O2 2SO3)是一个放热的反应。如果反应在密闭容器中进行,下列有关说法中正确的是
2SO3)是一个放热的反应。如果反应在密闭容器中进行,下列有关说法中正确的是
| A.因为反应放热,所以升高温度会使反应速率减慢 |
| B.通过调控反应条件,SO2可以100%地转化为SO3 |
| C.当SO2与SO3的浓度相等时,反应达到平衡 |
| D.使用催化剂的目的是加快反应速率,提高生产效率 |
一定温度下,可逆反应2NO2 2NO+O2,在体积固定的密闭容器中反应,达到平衡状态的标志是( )
2NO+O2,在体积固定的密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n mol O2,同时生成2n mol NO2;
②单位时间内生成n mol O2,同时生成2n mol NO;
③NO2、NO、O2的浓度比为2:2:1;
④混合气体的压强不再改变;
⑤混合气体的颜色不再改变;
⑥混合气体的平均摩尔质量不再改变.
| A.①④⑤⑥ | B.①②③⑤ | C.②③④⑥ | D.以上全部 |
在一定温度下,向2L密闭容器中加入1mol X和2mol Y,发生如下反应:
X(g)+2Y(g)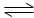 2Z(g),此反应达到平衡的标志是
2Z(g),此反应达到平衡的标志是
| A.容器内气体混合物的密度不随时间变化 |
| B.容器内X、Y、Z的浓度之比为1∶2∶2 |
| C.单位时间内消耗0.1mol X,同时生成0.2mol Y |
| D.单位时间内消耗0.1mol X,同时生成0.2mol Z |
某恒温密闭容器发生可逆反应Z(?)+W(?) X(g)+Y(?) ΔH ,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中不正确的是
X(g)+Y(?) ΔH ,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中不正确的是 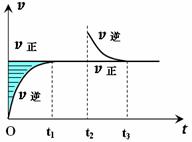
| A.Z和W在该条件下一定不为气态 |
| B.t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等 |
| C.若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X 浓度相等 |
| D.若该反应只在某温度T0以上自发进行,则该反应的平衡常数K随温度升高而增大 |
在一个体积为1 L的密闭容器中,充入2 mol A和1 mol B,发生如下反应:2A(g) + B(g) xC(g),平衡后,C的体积分数为w%,若维持容器容积和温度不变,0.6 mol A、0.3 mol B和1.4 mol C为起始物质,达到平衡后,C的体积分数也为w%。平衡后若缩小容器体积,C的浓度c(C)、C的体积分数C%、混合气体平均相对分子质量(
xC(g),平衡后,C的体积分数为w%,若维持容器容积和温度不变,0.6 mol A、0.3 mol B和1.4 mol C为起始物质,达到平衡后,C的体积分数也为w%。平衡后若缩小容器体积,C的浓度c(C)、C的体积分数C%、混合气体平均相对分子质量( )和正反应速率[v(正)],随压强(P)的变化,一定符合的是
)和正反应速率[v(正)],随压强(P)的变化,一定符合的是
A. B.
B.
C. D.
D.
炼铁高炉中冶炼铁的反应为:Fe2O3(s) + 3CO(g) 2Fe(s) +3CO2(g),下列说法正确的是
2Fe(s) +3CO2(g),下列说法正确的是
| A.升高温度,反应速率减慢 |
| B.当反应达到化学平衡时,υ(正)=υ(逆) = 0 |
| C.提高炼铁高炉的高度可减少尾气中CO的浓度 |
| D.某温度下达到平衡时,CO的体积分数基本不变 |
已知N2(g)+3H2(g) 2NH3(g);ΔH=-92.4kJ/mol。在一恒温恒压的密闭容器里充入2mol N2和8mol H2达到平衡时生成1mol NH3。现在相同条件下的同一容器中充入xmol N2,ymol H2和2mol NH3,达到平衡时,NH3的质量分数与原来相同,且放出热量46.2kJ。则x、y的值为
2NH3(g);ΔH=-92.4kJ/mol。在一恒温恒压的密闭容器里充入2mol N2和8mol H2达到平衡时生成1mol NH3。现在相同条件下的同一容器中充入xmol N2,ymol H2和2mol NH3,达到平衡时,NH3的质量分数与原来相同,且放出热量46.2kJ。则x、y的值为
| A.5,21 | B.3,13 | C.2,8 | D.1.5,6.5 |
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)  2C(g)。
2C(g)。
各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示:
下列说法正确的是
A.10min内甲容器中反应的平均速率v(A)=0.025mol/(L·min)
B.由图可知:T1<T2,且该反应为吸热反应
C.x=1,若平衡时保持温度不变,改变容器体积平衡不移动
D.T1℃,起始时甲容器中充入0.5molA、1.5molB,平衡时A的转化率为25%
还原沉淀法是处理含铬(含Cr2O72﹣和CrO42﹣)工业废水的常用方法,过程如下:
己知转化过程中反应为:2CrO42﹣(aq)+2H+(aq)  Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是
Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是
| A.溶液颜色保持不变,说明上述可逆反应达到达平衡状态 |
| B.若用绿矾(FeSO4·7H2O)(M=278)作还原剂,处理1L废水,至少需要917.4g |
| C.常温下转化反应的平衡常数K=1×1014,则转化后所得溶液的pH=6 |
| D.常温下Ksp[Cr(OH)3]=1×10﹣32,要使处理后废水中c(Cr3+)降至1×10﹣5mol/L,应调溶液的pH=5 |
已知一定温度下,2X(g)+Y(g) mZ(g) ΔH=-a kJ/mol(a>0),现有甲、乙两容积相等且固定不变的密闭容器,在保持该温度下,向密闭容器中通入2 mol X和1 mol Y,达到平衡状态时,放出热量b kJ,向密闭容器乙中通入1 mol X和0.5 mol Y,达到平衡时,放出热量c kJ,且b>2c,则a、b、m的值或关系正确的是
mZ(g) ΔH=-a kJ/mol(a>0),现有甲、乙两容积相等且固定不变的密闭容器,在保持该温度下,向密闭容器中通入2 mol X和1 mol Y,达到平衡状态时,放出热量b kJ,向密闭容器乙中通入1 mol X和0.5 mol Y,达到平衡时,放出热量c kJ,且b>2c,则a、b、m的值或关系正确的是
| A.m=4 | B.a=b | C.a< |
D.m≤2 |
试题篮
()