PCl3和PCl5都是重要的化工原料。将PCl3(g)和Cl2(g)充入体积不变的2 L密闭容器中,在一定条件下发生下述反应,并于10 min时达到平衡:PCl3(g)+Cl2(g) PCl5(g) ΔH<0。有关数据如下:
PCl5(g) ΔH<0。有关数据如下:
| |
PCl3(g) |
Cl2(g) |
PCl5(g) |
| 初始浓度/(mol/L) |
2.0 |
1.0 |
0 |
| 平衡浓度/(mol/L) |
c1 |
c2 |
0.4 |
下列判断不正确的是
A.10 min内,v(Cl2)="0.04" mol/(L·min)
B.升高温度,反应的平衡常数减小,则平衡时PCl3的转化率变大
C.当容器中Cl2为1.2 mol时,反应达到平衡
D.平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L
一定条件下,通过下列反应可以制备特种陶瓷的原料MgO,MgSO4(s) + CO(g) MgO(s) + CO2(g) +SO2(g) △H>0该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
MgO(s) + CO2(g) +SO2(g) △H>0该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
| 选项 |
x |
y |
| A |
温度 |
容器内混合气体的密度 |
| B |
CO的物质的量 |
CO2与CO的物质的量之比 |
| C |
SO2的浓度 |
平衡常数K |
| D |
MgSO4的质量(忽略体积) |
CO的转化率 |
密闭的真空容器中放入一定量CaO2固体,发生反应2CaO2(s) 2CaO(s)+O2(g)并达到平衡。保持温度不变,缩小容器容积为原来的一半,重新平衡后,下列叙述正确的是
2CaO(s)+O2(g)并达到平衡。保持温度不变,缩小容器容积为原来的一半,重新平衡后,下列叙述正确的是
| A.平衡常数减小 | B.CaO的量减少 | C.氧气浓度变大 | D.CaO2的量不变 |
已知A(g)+B(g) C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
| 温度/ ℃ |
700 |
800 |
830 |
1000 |
1200 |
| 平衡常数 |
1.7 |
1.1 |
1.0 |
0.6 |
0.4 |
830℃时,向一个2 L的密闭容器中充入0.2mol的A和0.8mol的B,反应初始4 s内A的平均反应速率v(A)=0.005 mol/(L·s)。下列说法正确的是
A.4 s时c(B)为0.76 mol/L
B.830℃达平衡时,A的转化率为80%
C.反应达平衡后,升高温度,平衡正向移动
D.1200℃时反应C(g)+D(g)  A(g)+B(g)的平衡常数的值为0.4
A(g)+B(g)的平衡常数的值为0.4
下列事实能用勒沙特列原理解释的是
①由H2、I2蒸气、HI组成的平衡体系加压后颜色变深
②实验室中用氯化钠固体与浓硫酸共热制取氯化氢气体
③用排饱和食盐水法收集Cl2
④温度控制在500℃有利于合成氨反应
⑤工业制取金属钾Na(l)+ KCl(l)  NaCl(l)+ K(g)选适宜的温度,使K成蒸气从反应混合物中分离出来
NaCl(l)+ K(g)选适宜的温度,使K成蒸气从反应混合物中分离出来
| A.②③⑤ | B.①③⑤ | C.②③④⑤ | D.①②③⑤ |
2NH3(g)+CO2(g) 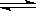 CO (NH2)2(s)+H2O(g) 在该可逆反应中,当化学平衡逆向移动时,体系气体的平均分子量会
CO (NH2)2(s)+H2O(g) 在该可逆反应中,当化学平衡逆向移动时,体系气体的平均分子量会
| A.不确定 | B.变小 | C.不变 | D.变大 |
已知NO2和N2O4可以相互转化:2NO2(g) N2O4(g) △H<0。在恒温条件下将一定量NO2和N2O4的混合气体通入容积为2 L的密闭容器中,反应物浓度随时间变化关系如图。下列说法正确的是
N2O4(g) △H<0。在恒温条件下将一定量NO2和N2O4的混合气体通入容积为2 L的密闭容器中,反应物浓度随时间变化关系如图。下列说法正确的是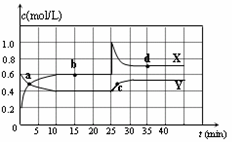
| A.图中Y曲线是表示NO2浓度随时间的变化曲线 |
| B.前10 min内v(N2O4)为0.1 mol/( L·min) |
| C.25 min时,导致平衡移动的原因是将密闭容器的体积缩小为1L |
| D.25 min时,导致平衡移动的原因是向容器通入适量NO2 |
在0.1 mol·L-1CH3COOH溶液中存在如下电离平衡:CH3COOH CH3COO-+H+,对于该平衡,下列叙述正确的是
CH3COO-+H+,对于该平衡,下列叙述正确的是
| A.加入水时,平衡向逆反应方向移动 |
| B.加入少量NaOH固体,平衡向正反应方向移动 |
| C.加入少量0.1 mol·L-1HCl溶液,溶液中c(H+)减小 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇: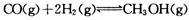 ,若在温度和容器相同的三个密闭容器中,按不同方式投人反应物,测得反应达到平衡吋的有关数据如下表,则下列关系正确的是
,若在温度和容器相同的三个密闭容器中,按不同方式投人反应物,测得反应达到平衡吋的有关数据如下表,则下列关系正确的是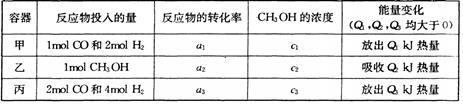
| A.a1+a3=1 | B.2Q1=Q3 | C.c1=c2 | D.2a1=a3 |
某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g) 2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中各物质的物质的量浓度、反应速率分别随时间的变化如下图所示:
2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中各物质的物质的量浓度、反应速率分别随时间的变化如下图所示: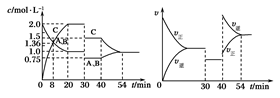
下列说法中正确的是
| A.30~40 min间该反应使用了催化剂 |
| B.反应方程式中的x=1,正反应为吸热反应 |
| C.8 min前A的平均反应速率为0.08 mol·L-1·min-1 |
| D.30 min时降低温度, 40 min时升高温度 |
在一定温度下,a的容积保持不变,b的上盖可随容器内气体压强的改变而上下移动,以保持容器内外压强相等。在a、b中分别加入2 mol A和2 molB,起始时容器体积均为V L,发生反应2A+B  x C,并达到化学平衡状态,平衡时两容器中A、B、C的物质的量之比均为1:3:6。下列说法一定正确的是
x C,并达到化学平衡状态,平衡时两容器中A、B、C的物质的量之比均为1:3:6。下列说法一定正确的是

A.x的值为2
B.B物质可为固体或液体
C.平衡时,a容器的体积小于V L
D.a、b容器中从起始到平衡所需时间相同
在一定条件下,对于反应mA(g)+n(B) cC(g)+dD(g),C的百分含量(C%)与温度、压强的关系如图所示,
cC(g)+dD(g),C的百分含量(C%)与温度、压强的关系如图所示,
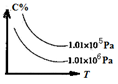
下列该反应的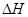 、
、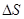 判断正确的是
判断正确的是
A.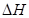 >0,
>0,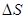 <0 B.
<0 B.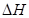 <0,
<0,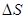 >0
>0
C.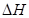 >0,
>0,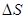 >0 D.
>0 D.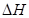 <0,
<0,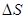 <0
<0
下列变化不能用勒夏特列原理解释的是
| A.红棕色的NO2气体加压后颜色先变深再变浅 |
| B.打开汽水瓶,看到有大量的气泡逸出 |
| C.二氧化硫转化为三氧化硫时增加空气的量以提高二氧化硫的转化率 |
| D.H2、I2、HI混合气体加压后颜色变深 |
已知:25℃时, Ksp(FeS)=6.3×10-18;Ksp(CuS)=1.3×10-36;Ksp(ZnS)=1.6×10-24.下列叙述正确的是
| A.25℃时,FeS、ZnS、CuS的溶解度依次增大 |
| B.ZnS饱和溶液这加入少量Na2S固体,平衡后溶液中c(Zn2+)·c(S2-)=Ksp,c(Zn2+)=c(S2-) |
| C.除去工业废水中的Cu2+,可用FeS作为沉淀剂 |
| D.某溶液中含有Fe2+、Cu2+和Zn2+,浓度均为0.010mol/L。向该溶液中逐滴加入0.010mol/L的Na2S溶液时,Fe2+最先沉淀出来 |
在体积一定的密闭容器中,给定物质A、B、C的量,在一定条件下发生反应,建立如下化学平衡:aA(g)+ bB(g) xC(g),符合图(1)所示的关系(C%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图(2)中,Y轴是指
xC(g),符合图(1)所示的关系(C%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图(2)中,Y轴是指

A.反应物A的百分含量 B.反应物B的平衡转化率
C.平衡混合气的密度 D.平衡混合气的总物质的量
试题篮
()