反应4NH3+5O2 4NO+6H2O在一定体积的密闭容器中进行,20s后NO的物质的量浓度增加了2mol/L,则下列反应速率正确的是
4NO+6H2O在一定体积的密闭容器中进行,20s后NO的物质的量浓度增加了2mol/L,则下列反应速率正确的是
| A.v (NO)="0.02" mol•(L•s)﹣1 |
| B.v (NO)=0.2mol•(L•s)﹣1 |
| C.v (NH3)="0.1" mol•(L•s)﹣1 |
| D.v (NH3)="0.01" mol•(L•s)﹣1 |
下面四个选项是四位同学在学习过化学反应速率和化学平衡理论以后,联系化工生产实际所发表的看法,你认为不正确的是
| A.化学反应速率理论可指导怎样提高原料的转化率 |
| B.化学反应速率理论可指导怎样在一定时间内快出产品 |
| C.化学平衡理论可指导怎样使用有限原料多出产品 |
| D.正确利用化学反应速率和化学平衡理论都可提高化工生产的综合经济效益 |
将0.05molSO2(g)和0.03molO2(g)放入容积为1L的密闭容器中,反应2SO2(g)+O2(g) 2SO3(g),在一定条件下2min时达到平衡,测得c(SO3)=0.04mol·L-1。以下表述正确的是
2SO3(g),在一定条件下2min时达到平衡,测得c(SO3)=0.04mol·L-1。以下表述正确的是
| A.若恒容下,充入氮气,则c(SO3)小于0.04mol·L-1 |
| B.该条件下反应的平衡常数为1.6×103 |
| C.v(O2)= 0.02 mol·L-1.min-1 |
| D.使用催化剂若平衡没有移动,则该反应达到化学平衡状态 |
将4 mol A 气体和2 mol B 气体在2 L 的密闭容器中混合并在一定条件下发生如下反应2A(g)+B(g) 2C(g);△H <0。4 s(秒)后反应达到平衡状态,此时测得 C 的浓度为0.6 mol·L-1。下列说法中正确的是
2C(g);△H <0。4 s(秒)后反应达到平衡状态,此时测得 C 的浓度为0.6 mol·L-1。下列说法中正确的是
A.当A、B、C物质的量浓度之比为 2:1:2时,反应即达到平衡状态
B.4s内用物质B表示的反应速率为0.075 mol·L-1·s-1
C.达平衡后若通入一定量氦气,A的转化率降低
D.达平衡后若升高温度,C的浓度将增大
对反应4A+5B 4C+6D,以下化学反应速率的表示中,所表示反应速率最快的
4C+6D,以下化学反应速率的表示中,所表示反应速率最快的
A.v (A)=0.40mol•L-1•s-1 B.v (B)=0.48mol•L-1•s-1
C.v (C)=0.36mol•L-1•s-1 D.v (D)=0.55mol•L-1•s-1
反应4A(s)+3B(g)  2C(g)+D(g),经2min,B的浓度减少0.6 mol•L-1。对此反应速率的表示,正确的是
2C(g)+D(g),经2min,B的浓度减少0.6 mol•L-1。对此反应速率的表示,正确的是
①用A表示的反应速率是0.4 mol•L-1•min-1
②分别用B、C、D表示的反应速率其比值为3:2:1
③在2 min末的反应速率,用B表示是0.3 mol•L-1•min-1
④反应的过程中,只增加A的量,反应速率不变
A.①② B.③ C.① D.②④
反应4A(g)+5B(g) 4C(g)+6D(g) 在5L的密闭容器中进行反应,30min后,C的物质的量增加了0.30mol.下列叙述正确的是
4C(g)+6D(g) 在5L的密闭容器中进行反应,30min后,C的物质的量增加了0.30mol.下列叙述正确的是
A.30min中A的平均反应速率是0.010mol·L﹣1·min﹣1
B.容器中D的物质的量一定增加了0.45mol
C.容器中A、B、C、D的物质的量的比一定是4:5:4:6
D.容器中A的物质的量一定增加0.30mol
将固体NH4Br置于密闭容器中,在某温度下,发生下列可逆反应:NH4Br(s) 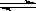 NH3(g)+HBr(g) 2HBr(g)
NH3(g)+HBr(g) 2HBr(g) 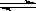 Br2(g)+H2(g),2min后,测得c(H2)=0.5mol/L,c(HBr)=4mol/L,若上述反应速率用
Br2(g)+H2(g),2min后,测得c(H2)=0.5mol/L,c(HBr)=4mol/L,若上述反应速率用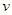 (NH3)表示,下列反应速率正确的是
(NH3)表示,下列反应速率正确的是
| A.0.5mol/(L·min) | B.2.5 mol/(L·min) |
| C.2 mol/(L·min) | D.5 mol/(L·min) |
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列描述正确的是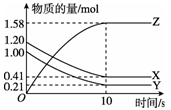
| A.反应开始到10 s时,用Z表示的反应速率为0.158 mol·(L·s)-1 |
| B.反应开始到10 s时,X的物质的量浓度减少了0.79 mol·L-1 |
| C.反应开始到10 s时,Y的转化率为39.5% |
D.反应的化学方程式为X(g)+Y(g) 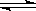 2Z(g) 2Z(g) |
在不同条件下,分别测得反应2SO2+O2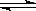 2SO3的速率如下,其中最快的是
2SO3的速率如下,其中最快的是
| A.v(SO2)=4 mol/(L·min) | B.v(O2)=2 mol/(L·min) |
| C.v(SO2)=0.1 mol/(L·min) | D.v(SO2)=0.1 mol/(L·s) |
一定温度时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,发生反应:PCl5(g)⇌Cl2(g)
+PCl3(g)经一段时间后反应达到平衡。反应过程中测得的部分数据见下表:
下列说法正确的是
| A.反应在前50 s内的平均速率为v(PCl3)="0.0032" moI·L-l·s-l |
| B.保持其他条件不变,若升高温度,反应重新达到平衡,平衡时c(PCl3)=0.11moI·L-l, 则正反应的△H<0 |
| C.相同温度下,若起始时向容器中充入1.0 molPCl5、0.20mol PCl3和0.20 mol Cl2,则反应达到平衡前v(正)<v(逆) |
| D.相同温度下,若起始时向容器中充入1.0mol PCl3、1.0 mol Cl2,则反应达到平衡时PCl3的转化率为80% |
在密闭容器中进行反应:X2(g)+Y2(g) 2Z(g),已知X2、Y2、Z的平衡浓度分别为0.1 mol/L、
2Z(g),已知X2、Y2、Z的平衡浓度分别为0.1 mol/L、
0.3 mol/L、0.2 mol/L,各物质的起始不可能是
| A.Z为0.3 mol/L | B.Y2为0.1 mol/L |
| C.X2为0.2 mol/L | D.Z为0.35mol/L |
对于化学反应3W(g)+2X(g) 4Y(g)+3Z(g),下列反应速率关系中,正确的是
4Y(g)+3Z(g),下列反应速率关系中,正确的是
| A.v(W)=3v(Z) | B.2v(X)=3v(Z) |
| C.2v(X)=v(Y) | D.3v(W)=2v(X) |
反应A+3B=2C+D在四种不同情况下的反应速率分别为:①v(A) =0.15mol/(L·s) ;②v(B)=0.6mol/(L·min);③v(C)=0.5mol/(L·s);④v (D) =0.45mol/(L·s) ,则反应进行由快到慢的顺序为
A.④>③>①>② B.②>④>③>①
C.②>③>④>① D.④>③>②>①
试题篮
()