已知:



下列说法不正确的是
| A.该反应原理可用于设计氢氧燃料电池 |
| B.破坏1molH-O键需要的能量是463.4kJ |
| C.H2O(g)=H2(g)+1/2O2(g)△H="+241.8" kJ/mol |
| D.H2(g)中的H-H键比H2O(g) 中的H-O键牢固 |
下列关于原电池说法正确的是(C )
| A.由Al、Mg、稀硫酸组成的原电池,其负极反应式为:Al-3e—=Al3+ |
| B.由Al、Mg、NaOH组成的原电池,其负极反应式为:Al-3e—+3OH—=Al(OH)3↓ |
| C.由Al、Cu、浓硝酸组成的原电池,其负极反应式为:Cu-2e—=Cu2+ |
| D.由Fe、Cu、FeCl3组成的原电池,其正极反应式为:Cu-2e—=Cu2+ |
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下: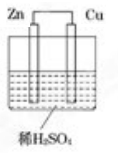
①Cu为负极,Zn为正极
②Cu极上有气泡产生,发生还原反应
③若有0.5mol电子流经导线,则可产生5.6LH2
④SO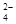 向Zn极移动
向Zn极移动
⑤电子的流向是:Cu→Zn
⑥正极反应式:Cu-2e-====Cu2+,
发生氧化反应则卡片上的描述合理的是
| A.②④ | B.②③ | C.③④ | D.④⑥ |
如图所示是一个燃料电池的示意图,当此燃料电池工作时,下列分析中正确的是
| A.如果a极通入H2,b极通入O2,NaOH溶液作电解质溶液,则通H2的电极上发生的反应为:H2-2e-=2H+ |
| B.如果a极通入H2,b极通入O2,H2SO4溶液作电解质溶液,则通O2的电极上发生的反应为:O2+4e-+2H2O=4OH- |
C.如果a极通入CH4,b极通入O2,NaOH作电解质溶液,则通CH4的电极上发生的反应为:CH4-8e-+10 OH-=CO +7H2O +7H2O |
| D.如果a极通入H2,b极通入O2,NaOH溶液作电解质溶液,则溶液中的OH-离子向b极附近移动 |
关于下图所示装置的说法中,不正确的是
| A.锌片是该装置的负极,该电极反应为Zn—2e—=Zn2+ |
| B.电子由锌片通过导线流向铜片 |
| C.该装置能将化学能转化为电能 |
| D.铜片上发生氧化反应 |
下列说法中,正确的是( )
| A.原电池是将电能转化为化学能的装置 |
| B.在原电池中,负极上发生氧化反应 |
| C.在原电池中,电子从原电池的正极流向负极 |
| D.由于生铁中含有碳,所以生铁比纯铁耐腐蚀 |
氢氧燃料电池已用于航天飞机。以30%KOH溶液为电解质的这种电池在使用时的电极反应如下:2H2+4OH--4e- ==4H2O O2+2H2O+4e-==4OH-下列说法错误的是
| A.氢气通入正极,氧气通入负极 |
| B.燃料电池的能量转化率不能达到100% |
| C.供电时的总反应为:2H2+O2 ="===" 2H2O |
| D.产物为无污染的水,属于环境友好电池 |
原电池产生电流的本质原因是( )
| A.原电池中溶液能电离出自由移动的离子 |
| B.有导线将两个活动性不同的电极连接 |
| C.正极发生了氧化反应,而负极发生了还原反应 |
| D.电极上进行的氧化还原反应中会有电子的转移 |
图为番茄电池,下列说法正确的是
| A.一段时间后,锌片质量会变小 | B.一段时间后,铜片质量会变小 |
| C.电子由铜通过导线流向锌 | D.锌电极是该电池的正极 |

来自法国格勒诺布尔(Grenoble)约瑟夫·傅立叶大学的研究小组发明了第一块可为人体人造器官提供电能的可植入的葡萄糖生物燃料电池,其基本原理是葡萄糖和氧气在人体中酶的作用下发生的总反应为C6H12O6+6O2=6CO2+6H2O(酸性环境),下列对该电池说法不正确的是
| A.该生物燃料电池不可以在高温下工作 |
| B.电池的负极反应为:C6H12O6+6H2O-24e-=6CO2+24H+ |
| C.消耗1mol氧气则转移4mole-,H+会向负极移动 |
| D.今后的研究方向是怎样提高葡萄糖生物燃料电池的效率,从而在将来达到可以利用葡萄糖生物燃料电池为任何可植入医疗设备提供电能 |
如果把2FeCl3 + Cu → 2FeCl2 + CuCl2设计成原电池,则在正极上生成的离子是
| A.Cl- | B.Fe2+ | C.Cu2+ | D.Fe3+ |
心脏起搏器中使用的新型电池Li-I2电池使用寿命已超过10年,其反应简化为:2Li+I2===2LiI,下列说法不正确的是 ( )
| A.负极反应:Li→Li++e- |
| B.该电池以LiI水溶液为电解质 |
| C.该电池以有机碘化物为电解质 |
| D.Li-I2电池是一种高能长寿的固体电池 |
将氢气(H2)、甲烷(CH4)、乙醇(C2H5OH)等物质在氯气(O2)中燃烧时的化学能直接转化为电能的装置叫燃料电池。燃料电池的基本组成为电极、电解质、燃料和氧化剂。此种电池能量利用率可高达80%(一般柴油发电机只有40%左右).产物污染也少。人们已将它用于航天飞行器上。下图为氢氧燃料电池反应的完整过程。关于上述氢氧燃料电池的说法不正确的是
| A.负极发生的反应:H2-2e-===2H+ |
| B.正极发生的反应:O2+2H2O+4e-===4OH- |
| C.燃料电池有很高的质量比能量(质能比).所以用于航天飞行器上 |
| D.燃料电池的产物为水,经过处理之后正好可供宇航员使用,更可减少携带重量 |
根据下图,下列判断中正确的是( )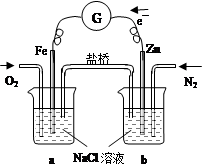
| A.烧杯b中发生还原反应 |
| B.烧杯a中的溶液pH升高 |
| C.烧杯a中发生的反应为2H++2e-=H2 |
| D.烧杯b中发生的反应为2Cl-−2e-=Cl2 |
下列说法错误的是( )
| A.钢铁发生析氢腐蚀时,负极电极反应是Fe-2e-=Fe2+ |
| B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
| C.将pH=4的盐酸和醋酸稀释成pH=5的溶液,盐酸所需加入的水多 |
| D.一定温度下,反应MgCl2(l)=Mg(l)+ Cl2(g)的△H>0△S>0 |
试题篮
()