关于由锌片、铜片和稀硫酸组成的原电池的说法中,正确的是
| A.锌片质量逐渐减少,铜片上有气泡产生 | B.电流方向是由锌片流向铜片 |
| C.锌片作正极,发生还原反应 | D.电解质溶液的pH保持不变 |
关于下图所示装置,下列叙述中正确的是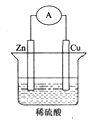
| A.铜是负极,锌片上有气泡产生 |
| B.锌片逐渐减轻,铜片逐渐增重 |
| C.电流从锌片经导线流向铜片 |
| D.氢离子在铜片表面得电子被还原 |
下列各组的电极材料和电解液,不能组成原电池的是
| A.铜片、石墨棒,蔗糖溶液 | B.锌片、石墨棒,硫酸铜溶液 |
| C.锌片、铜片,稀盐酸 | D.铜片、银片,硝酸银溶液 |
下图为铜锌原电池示意图,下列说法正确的是
| A.锌片逐渐溶解 |
| B.烧杯中溶液逐渐呈蓝色 |
| C.电子由铜片通过导线流向锌片 |
| D.该装置能将电能转变为化学能 |
如图所示,在用锌片、铜片和稀硫酸组成的原电池装置中,下列说法正确的是
| A.铜电极上的反应为Cu-2e-==Cu2+ |
| B.放电时溶液中的阳离子向锌片移动 |
| C.电池工作一段时间后溶液的pH值减小 |
| D.该电池的负极材料是锌片 |
根据下图,下列判断中正确的是
| A.烧杯a中的溶液pH升高 |
| B.烧杯b中发生还原反应 |
| C.烧杯a中发生的反应为2H++2e-=H2↑ |
| D.烧杯b中发生的反应为2Cl--2e-=Cl2↑[ |
将锌片和铜片用导线连接置于同一稀硫酸中,下列叙述正确的是
| A.锌片是正极 | B.电流方向从锌片流向铜片 |
| C.氢气在锌片上产生 | D.若锌片、铜片同时有气泡冒出,则说明锌片不纯 |
下列叙述正确的是
| A.原电池中阳离子向负极移动 | B.用铝质铆钉接铁板,铁易被腐蚀 |
| C.马口铁(镀锡)表面一旦破损,铁腐蚀加快 | D.白铁(镀锌)表面一旦破损,铁腐蚀加快 |
电子表和电子计算器的电源常用微型银锌原电池,其电极分别为Ag2O和Zn,电解质溶液为一定浓度的KOH溶液,放电时锌极上的电极反应式为:Zn-2e—+2OH—==Zn(OH)2;氧化银电极上的反应式为:Ag2O+2e—+H2O==2Ag+2OH-,总反应式为:Ag2O+H2O+Zn==Zn(OH)2+2Ag。下列说法正确的是
| A.溶液中OH— 向正极移动,K+、H+向负极移动 |
| B.锌发生还原反应,氧化银发生氧化反应 |
| C.锌是负极,氧化银是正极 |
| D.随着电极反应的不断进行,电解质的碱性减弱 |
下列关于实验现象的描述错误的是
| A.铜锌原电池中铜是正极 |
| B.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁 |
| D.把锌粒放入盛有盐酸的试管中,加几滴氯化铜溶液,气泡放出速率加快 |
将铁棒和锌棒用导线连接插入硫酸铜溶液中,当电池中有0.4 mol电子通过时,负极的质量变化是
| A.增加6.5g | B.减少5.6g | C.增加11.2g | D.减少13g |
对于铁、铜和稀硫酸组成的原电池(如图),下列有关说法正确的是
①Fe是负极 ②电子由Fe经外电路流向Cu,后再通过溶液流回到Fe
③Fe -2e-=Fe2+ ④ H+ 在溶液中由Cu棒向Fe棒迁移
⑤一段时间后溶液的PH变大 ⑥一段时间后溶液由无色变为浅绿色
| A.①② | B.①③⑤⑥ | C.②③④ | D.①②③④ |
将镁片和铁片用导线连接置于同一稀盐酸溶液中,经过一段时间后,下列叙述正确的是
| A.正极附近Cl-的浓度逐渐增大 |
| B.溶液中Cl-的浓度总体上基本不变 |
| C.负极上有Cl2逸出,正极上有H2逸出 |
| D.溶液的pH在电池工作过程中基本不变 |
试题篮
()