在一定条件下,甲、乙、丙、丁四种物质在一密闭容器中充分反应,测得反应前后 各物质的质量如下表所示。关于此反应下列认识不正确的是
| 物质 |
甲 |
乙 |
丙 |
丁 |
| 反应前质量/g |
1[ |
20 |
15 |
2 |
| 反应后质量/g |
m |
29 |
0 |
8 |
A.m的值是1 B.甲可能是该反应的催化剂
C.该反应是分解反应 D.反应中乙、丁的质量比是20:2
氯酸钾和二氧化锰的混合物15g,加热充分反应后剩余固体的质量为10.2g,则原混合物中氯酸钾的质量为( )
| A.10.2g | B.2.75g | C.4.8g | D.12.25g |
将氮气、一氧化碳、二氧化碳的混合气体先通过足量澄清石灰水,再通过足量灼热的氧化铜,最后剩余的气体是( )
| A.氮气 | B.二氧化碳 | C.一氧化碳 | D.二氧化碳和氮气 |
计算题:某化学兴趣小组为测定一种石灰石样品中碳酸钙的质量分数,进行如下实验:
①称取25.0g石灰开佯品,平均分成两份,并分别加工成块状和粉末状;
②将两份样品分别投入两个锥形瓶中,各加入足量的相同溶质质量分数的稀盐酸(样品所含杂质不溶于水也不与酸反应),测得生成二氧化碳的质量与反应时间的关系如下图所示:

请回答:每份样品充分反应后.生成二氧化碳的质量为 g;该样品中碳酸钙的质量分数为多少呢
由于涉嫌铬超标,国家食品药品监督管理局4月16日发出紧急通知,要求对13个药用空心胶囊产品暂停销售和使用。下列有关铬(Cr)的化合物的叙述错误的是( )
| A.在Cr(OH)3中铬、氧、氢三种元素的原子个数比1︰3︰3 |
| B.K2Cr2O7由三种元素组成 |
| C.在K2Cr2O7中铬元素的化合价为+6价 |
| D.在K2Cr2O7中铬元素的含量最高 |
某校化学实验室废液桶中收集了溶解大量FeSO4、CuSO4的废水,若直接排放到下水道不仅造成重金属污染而且造成浪费。初三(2)班的同学,准备运用刚学到的“常见金属活动性顺序表”结合其他有关化学知识对废水进行处理。
(1)设计除去铜离子,回收硫酸亚铁晶体和铜的实验方案,讨论有关问题:

①废水在加入金属X前需进行过滤,目的是将其中__________性杂质除去。进行过滤的操作所需的仪器有:________、________、________、________(请从下图中选择合适仪器,并用仪器名称填写)。

②金属X是_____________,其加入废水后发生反应的化学方程式为___ ____溶液Y是________利用其除去铜中杂质,有关反应的化学方程式为______________
将等质量、颗粒大小相同的X、Y、Z三种金属分别投入到相同浓度的足量的稀硫酸中,生成氢气的质量与时间的关系如图所示。已知它们在化合物中均显+2价,则下列说法不正确的是( )
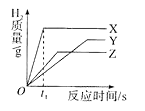
| A.在时间为t1时,生成氢气的质量为:X>Z>Y |
| B.金属活动性:X>Z>Y |
| C.相对原子质量:X>Y>Z |
| D.X、Y和Z可能分别是常见金属中的Mg、Fe、Zn |
某班同学用下图装置测定空气里氧气的含量。先用弹簧夹夹住乳胶管。点燃红磷伸入瓶中并塞上瓶塞。待红磷熄灭并冷却后,打开弹簧夹,观察广口瓶内水面变化情况。实验完毕,甲同学的广口瓶内水面上升明显小于瓶内空气体积的1/5,乙同学的广口瓶内水面上升明显大于瓶内空气体积的1/5。下列对这两种现象解释合理的是( )

①甲同学可能使用的红磷燃烧没有消耗完瓶内的氧气
②甲同学可能没夹紧弹簧夹,红磷燃烧时瓶内空气受热从导管逸出
③乙同学可能未塞紧瓶塞,红磷熄灭冷却时外界空气进入瓶内
④乙同学可能插入燃烧匙太慢,塞紧瓶塞之前,瓶内空气受热逸出
| A.只有①③ | B.只有①④ | C.只有①②③ | D.①②④ |
研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
【假设】H2O2生成O2的快慢与 有关。
【实验方案】常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量MnO2红砖粉后测量各生成一瓶(相同体积)O2所需要的时间。
【进行实验】如图是他们进行实验的装置图,气体发生装置中A仪器名称是 ,此实验中B处宜采用的气体收集方法是

【结论】该探究过程得出的结论是 。
【反思】H2O2在常温下分解缓慢,加入MnO2或红砖粉后反应明显加快,若要证明MnO2和红砖粉是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的 和 是否改变。

某实验创新小组对木炭还原氧化铜的实验进行了改进,其操作步骤如下:
①取一片铜片,用砂纸除去其表面的氧化物使其表面呈光亮的紫红色;
②用酒精灯将上述铜片烧到红热后,立即伸入到集满氧气的集气瓶中,观察到的现象为:
铜片表面变成 色;
③在一支干燥的大试管中装入一定量的经烘干处理过的木炭粉,再将经②处理过的铜片部分埋入木炭粉中;
④按照右图所示的装置图连接好各种仪器;

⑤加热大试管,其中发生的反应的化学热方程式为: 当观察到澄清石灰水 后,先移走导管,后停止加热;
⑥待试管冷却后,用镊子取出铜片,洗净后观察。回答下列问题:
(1)填写上述各空;
(2)②中用到的夹持仪器是 (填名称)
(3)⑤中“先”、“后”颠倒,造成的后果是: 。
(4)⑥中观察到的现象是:铜片表面埋入木炭粉的部分 。
为探究燃烧的条件,某同学查阅资料得知:白磷为白色蜡状固体,剧毒,不溶于水,着火点为40oC;红磷的着火点为240oC。然后按下图所示A装置进行实验。

(1)观察到的现象为:1铜片上的白磷和红磷分别是 ②水下的白磷 ;
(2)在使用组装好的B装置前,首先应该进行的操作是 ,然后加入药品并将B和C装置连接,滴入双氧水,B装置中反应的化学方程式为 ,C装置中的白磷燃烧。
(3)从以上实验分析可得出燃烧的条件为:可燃物、 和 。
A—H是学过的一些物质,其中A是暗紫色固体,B是人体生命活动离不开的气体, E是淡黄色固体,G是白色固体。它们之间有如下图所示的转化关系: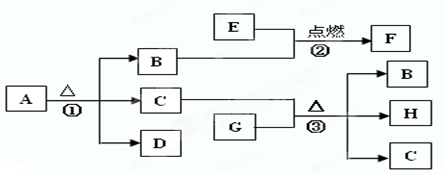
回答下列问题:
(1)写出下列物质的化学式:
C______________;G______________。
(2)反应②的实验:可以观察到的实验现象为:发出____________的火焰,生成一种有刺激性气味的气体。
(3)写出下列反应的化学方程式:
①________________________;②_________________________。
在一个密闭容器内有四种物质,在一定条件下充分反应后,测得反应前后各物质的质量如下:
| 物质 |
X |
Y |
Z |
Q |
| 反应前质量/g |
4 |
10 |
1 |
21 |
| 反应后质量/g |
0 |
12 |
15 |
待测 |
且X的相对分子质量为n,Q的相对分子质量为2n,则下列推理正确的是( )
A.反应物是Y和Z,生成物是X和Q
B.反应后生成15gZ
C.参加反应的Y与Q的质量比是1:1
D.该反应方程式中X与Q的化学计量数比为2:3
为减少污染、提高煤的利用率,可将其转化为可燃性气体,其微观示意图如下所示:
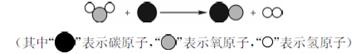 下列说法正确的是
下列说法正确的是
A.图中表示化合物的是 |
| B.该反应类型为化合反应 |
| C.该反应中反应物两种分子的个数比为3∶1 |
| D.反应前后原子的种类和数目保持不变 |
实验室利用下图所示装置进行相关实验,请回答问题:

A B C D E F
(1)写出有标号仪器的名称:① ;② 。
(2)若用A装置制取氧气,A中发生反应的化学方程式是 , 该反应属于 反应(填“化合”或“分解”)。
(3)写出实验室用石灰石和稀盐酸反应制取二氧化碳的化学方程式 ,可选用的发生装置是 (填字母)。
(4)选用装置 (填字母)收集二氧化碳,将燃着的木条放在瓶口,观察到 ,说明瓶中已充满二氧化碳。小林同学取一张用石蕊试液染成紫色的干燥纸片,将纸片的一半喷上水,喷水的那一半为 色;将这一纸片放入盛有二氧化碳的集气瓶中,观察到干燥的一边呈紫色,潮湿的一边呈红色。小林通过实验现象说明 不能使紫色石蕊变色。
(5)利用装置F(集气瓶中预先装满CO2气体)来验证CO2的性质,加入足量澄清石灰水,观察到的现象是气球 (填“变大”、“变小”或“不变”)。
试题篮
()