为了探究影响锌与盐酸反应剧烈程度的因素,某学习小组设计了下列实验
下列说法正确的是( )
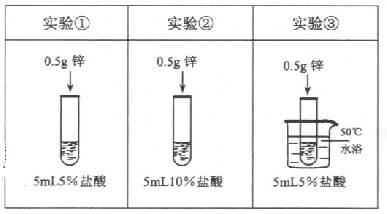
| A. | 对比实验①和②,可研究盐酸的浓度对反应剧烈程度的影响 |
| B. | 对比实验②和③,可研究盐酸的浓度对反应剧烈程度的影响 |
| C. | 对比实验②和③,可研究温度对反应剧烈程度的影响 |
| D. | 对比实验①和②,可研究温度对反应剧烈程度的影响 |
科学探究的一个重要环节是"猜想",猜想是依据已有知识、经验,对提出的问题进行合理的假设。下列对"影响食物腐败快慢的因素"的猜想不合理的是( )
| A. | 温度高低 | B. | 氧气含量 | C. | 食物多少 | D. | 食物种类 |
下列实验设计合理的是()
| A. | 粗盐提纯中蒸发时用玻璃棒是为了受热均匀 |
| B. | 除去一氧化碳中混有的二氧化碳可以通过灼热的氧化铜 |
| C. | 配制100g10﹪的氯化钠溶液需要10g氯化钠和80g水 |
| D. | 碳酸氢铵与草木灰混合使用可以增加肥效 |
下列每组对比实验不能达到实验目的是
| 选项 |
实验设计 |
实验目的 |
|
| 实验一 |
实验二 |
||
| A |
将带火星的木条伸入装有5
5%的过氧化氢溶液的试管中 |
将带火星的木条伸入装有少量
和5
5%的过氧化氢溶液的试管中 |
探究催化剂对化学反应速率的影响 |
| B |
将铁丝放入2
10%的硫酸铜溶液中 |
将银丝放入2
10%的硫酸铜溶液中 |
探究铁、铜、银三种金属的活动性顺序 |
| C |
将5
氯化钠加入20
20℃的水中 |
将5
硝酸钾加入20
10℃的水中 |
比较两种物质溶解度大小 |
| D |
将植物嫩叶浸泡在10
蒸馏水中 |
取10
蒸馏水,通入过量二氧化硫气体,再将植物嫩叶浸泡其中 |
模拟酸雨的危害 |
小黄同学在化学课上提出,可用澄清石灰水检验人呼出的气体是否是二氧化碳,这一过程属于科学探究环节的
| A.提出假设 | B.收集证据 | C.设计实验 | D.作出结论 |
点燃一支蜡烛,把一个冷碟子放在蜡烛火焰的上方(如图所示),过一会儿后,在冷碟子的底部会收集到新制的炭黑。这个实验说明了
| A.蜡烛在一定条件下燃烧可生成炭黑 |
| B.挥发的蜡烛遇冷后凝结而成炭黑 |
| C.蜡烛的燃烧有新物质生成,是物理变化 |
| D.蜡烛中本身不含有碳元素,但燃烧后生成了碳单质 |
通过下列实验可以得出的结论,其中不合理的是( )
| A.甲实验中黄铜片能在铜片上刻画出痕迹,说明黄铜的硬度比铜片大 |
| B.乙实验既可以说明分子在不停地运动着,又可以说明氨水显碱性 |
| C.丙实验既可以将粗盐提纯,又可以说明氯化钠的溶解度随温度的升高而增大 |
| D.丁实验既可以说明一氧化碳具有还原性,又可以说明一氧化碳具有可燃性 |
下列应用化学科学对物质进行研究的基本方法或所得的结论,错误的是 ( )
| A. | 氢气和甲烷的密度都比空气的小,所以都可用向下排气法收集 |
| B. | 配制溶质质量分数一定的溶液时,所用的烧杯必须是干燥的 |
| C. | 蜡烛燃烧后质量变小,说明质量守恒定律不是普遍规律 |
| D. | 通过测定两种稀盐酸的 ,可以比较它们的酸性强弱 |
小亮利用蜡烛进行实验,下列有关说法不正确的是( )
| A. | 用扇子可扇灭蜡烛火焰,说明物质燃烧必须达到着火点 |
| B. | 切一小块蜡烛放入水中,蜡烛浮于水面,说明石蜡的密度小于水 |
| C. | 取冷而干燥的小烧杯罩在火焰上方,有水雾出现,说明石蜡中含有氢、氧元素 |
| D. |
在密闭容器中,石蜡燃烧一段时间后熄灭,说明物质通常燃烧需
 要氧气 要氧气
|
如右图所示装置,将 滴加到 中, 形管中的液面变得左高右低,则 、 对应的试剂组可能是()

| 试剂\选项 | A | B | C | D |
| 盐酸 | ||||
| 生石灰 |
过氧化氢( )是一种无色液体,常用作氧化剂、漂白剂和消毒剂。为了贮存、运输和使用的方便,工业上将过氧化氢转化为固态的过碳酸钠晶体( ),该晶体具有碳酸钠和过氧化氢的双重性质。下列物质不会使过碳酸钠失效的是
| A. | 二氧化锰 | B. | 澄清石灰水 | C. | 盐酸 | D. | 氯化钠 |
比较、推理是化学学习常用的方法,以下是根据一些反应事实推导出的影响化学
反应的因素,其中推理不合理的是 ( ) 
下列是某化学学习小组在“人吸入的空气和呼出的气体中有什么不同”的探究活动中提出的一些说法,其中错误的是 ( )
| A.证明呼出的气体含二氧化碳多的证据是:呼出的气体能使澄清石灰水变得更浑浊 |
| B.判断呼出的气体含氮气的依据是:空气中含有氮气,而氮气不为人体吸收 |
| C.证明呼出的气体含水蒸气多的证据是:呼出的气体在玻璃片上结下水珠 |
| D.证明呼出的气体含氧气的证据是:呼出的气体能使木条燃烧更旺 |
试题篮
()