下列实验操作中,能达到实验目的是( )
选项 |
实验目的 |
实验操作 |
A |
除去H2中少量水蒸气 |
通过盛有浓硫酸的洗气瓶洗气 |
B |
除去NaNO3溶液中少量的Na2SO4 |
加过量Ba(OH)2溶液,过滤 |
C |
鉴别厨房里的白酒和白醋 |
观察颜色 |
D |
鉴别实验室里的食盐水和蔗糖水 |
品尝味道 |
A.AB.BC.CD.D
下列实验方案中,实验设计能达到实验目的是( )
序号 |
实验目的 |
实验设计 |
A |
探究稀盐酸与氢氧化钠溶液是否恰好完全反应 |
向反应后所得的溶液中滴加酚酞溶液 |
B |
鉴别氯化钡、硫酸钾、碳酸钾、稀盐酸四种溶液 |
将组内物质相互混合,观察现象 |
C |
除去氧化钙中少量的碳酸钙 |
加入足量的水,溶解,过滤 |
D |
验证某可燃性混合气体中是否有一氧化碳 |
点燃气体,在火焰上方罩一个内壁涂有澄清石灰水的烧杯,观察石灰水是否变浑浊 |
A.AB.BC.CD.D
化学是一门以实验为基础的自然科学。根据所学知识回答以下问题:
(1)实验室制取二氧化碳,应选用以下药品①块状石灰石②碳酸钠粉末③稀盐酸④稀硫酸中的 (填序号)。现有大理石粉末和稀硫酸,你认为 (填“能”或“否”)用于实验室制取二氧化碳。
(2)实验室有如图1装置,根据要求回答问题:
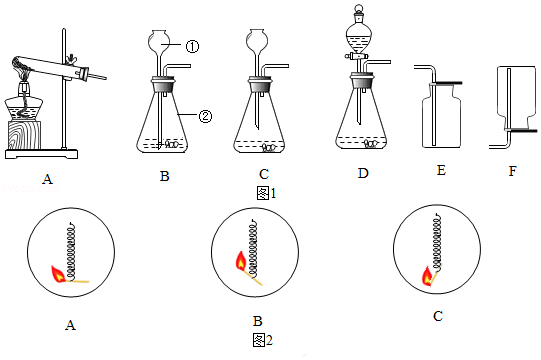
Ⅰ.写出标号仪器的名称① ,② 。
Ⅱ.对比装置B、C,有错误的是 (填序号,下同)。
Ⅲ.实验室要制取二氧化碳应选择的发生装置是 ,收集装置是 ;利用制取二氧化碳的发生和收集装置还能制取另外一种常见气体,利用此装置制取该气体的化学方程式是 。
Ⅳ.图2是同学们进行“铁丝在氧气中燃烧的性质实验”时的几种操作方式,更能提高实验成功率的方式是 (填序号)。
(3)有的同学完成上述实验后,提出“铁丝能否在二氧化碳中燃烧呢?”,他们设计了如下方案:(已知:在点燃的条件下,镁带能在二氧化碳中剧烈燃烧。)
方案①:将弯成螺旋状的细铁丝系上一根火柴,点燃火柴,待火柴快燃尽时,插入装有二氧化碳的集气瓶中,观察铁丝能否被引燃。
方案②:将弯成螺旋状的细铁丝系上一段镁带,点燃镁带,待镁带快燃尽时,插入装有二氧化碳的集气瓶中,观察铁丝能否被引燃。
你认为方案 (填①或②)更为科学,理由是 。
下列实验操作、现象与结论一致的是( )
序号 |
实验操作 |
现象 |
结论 |
A |
向久置空气中的NaOH固体滴加盐酸 |
产生气泡 |
NaOH已部分变质 |
B |
向某无色溶液滴入紫色石蕊试液 |
溶液变蓝 |
该溶液一定是碱溶液 |
C |
将燃着的木条伸入盛满某气体的集气瓶中 |
木条熄灭 |
该气体是CO2 |
D |
向碘化钾、稀硫酸和淀粉的混合液中加入某食用盐 |
溶液变蓝 |
该食用盐为加碘食盐 |
A.AB.BC.CD.D
中和反应在日常生活中应用广泛,下列是稀盐酸和氢氧化钠溶液反应的微观示意图。回答以下问题:
(1)分析图中反应前后没有发生变化的微粒是 、 ;反应的实质是 。
(2)如果规定上述反应后溶液的pH<7,显酸性。请你设计一个实验方案证明溶液显酸性:
实验操作 |
实验现象 |
实验结论 |
①
|
②
|
显酸性 |
日常生活中的下列做法可行的是( )
| A. |
将鲜奶发酵制成酸奶 |
B. |
在家具生产过程中大量使用甲醛 |
| C. |
将燃气热水器安装在浴室内 |
D. |
用NaNO 2溶液浸泡海鲜,防止变质 |
下列实验设计或结论合理的是( )
| A. |
向某固体滴加稀盐酸,有气泡产生,则该固体一定是碳酸盐 |
| B. |
除去MgCl 2溶液中混有的少量CuCl 2,可加入适量的Mg(OH) 2充分搅拌后过滤 |
| C. |
CO 3 2 ﹣、Na +、NO 3 ﹣、K +四种离子可在pH=12的溶液中大量共存 |
| D. |
将带火星的木条伸入到装有气体的集气瓶中,木条不复燃,证明该气体中不含氧气 |
下列实验目的对应实验方案正确的是( )
实验目的 |
实验方案 |
|
A |
除去氯化钾溶液中的氯化铜 |
加入氢氧化钠溶液至不再产生沉淀 |
B |
鉴别碳酸铵、硫酸铵、硝酸铵三种氮肥 |
用氢氧化钡溶液 |
C |
除去CO中少量H2O和CO2 |
先通过浓硫酸,再通过氢氧化钠溶液 |
D |
鉴别纯铝和硬铝 |
将两者相互刻画,比较硬度 |
A.AB.BC.CD.D
工业上以黄铁矿(主要成分是二硫化亚铁FeS2)为原料,生产硫酸。将黄铁矿(FeS2)粉碎,加入沸腾炉中瓶鼓入空气进行高温煅烧,得到气体和炉渣,气体经过一系列变化得到硫酸。请回答下列问题:
Ⅰ.FeS2中硫元素的化合价为 。
Ⅱ.将黄铁矿粉碎,目的是 。
Ⅲ.已知炉渣的主要成分为铁的某一种氧化物,甲同学对炉渣中铁的氧化物进行探究。
【查阅资料】
1.Fe3O4+8HCl═FeCl2+2FeCl3+4H2O
2.向FeCl2溶液中滴加铁氰化钾溶液,产生蓝色沉淀,而向FeCl3溶液中滴加铁氰化钾溶液不产生蓝色沉淀。
3.向FeCl3溶液中滴加无色的硫氰化钾溶液时,溶液变成红色,而向FeCl2溶液中滴加无色的硫氰化钾溶液时,溶液不变成红色。
【提出猜想】猜想1:炉渣中铁的氧化物为FeO 猜想2:炉渣中铁的氧化物为Fe2O3
猜想3:炉渣中铁的氧化物为 。(填化学式)
【方案设计】
1.取少量炉渣于烧杯中,加入过量的稀盐酸(杂质不溶于稀盐酸),充分搅拌,过滤。
2.取上述滤液少许于A、B两试管中,向A试管中滴入铁氰化钾溶液,设想有两种可能的实验现象:①产生蓝色沉淀;②不产生蓝色沉淀。向B试管中滴入少量无色的硫氰化钾溶液,设想也有两种可能的实验现象:③溶液变为红色;④溶液不变红色。
请你帮助甲同学填写猜想成立时,A、B两试管中的实验现象(用①②③④填空):
若猜想1成立,则实验现象为 。
若猜想2成立,则实验现象为 。
若猜想3成立,则实验现象为 。
【实验验证】甲同学取滤液少许于试管中,向试管中滴加铁氰化钾溶液或无色的硫氰化钾溶液中的一种试剂就证明了猜想2成立,甲同学滴加的试剂为 。
对如图所示实验的分析不正确的是( )
A. 燃着的木条熄灭,说明气体X一定是二氧化碳
燃着的木条熄灭,说明气体X一定是二氧化碳
B. 试管外壁发烫,说明生石灰与水的反应放出热量
试管外壁发烫,说明生石灰与水的反应放出热量
C. 二极管发光,说明水果电池提供了电压
二极管发光,说明水果电池提供了电压
D. 穿旱冰鞋的小红用力推墙却向后运动,说明物体间力的作用是相互的
穿旱冰鞋的小红用力推墙却向后运动,说明物体间力的作用是相互的
实验是进行科学研究的重要手段,实验方案的设计是实验成功的基本保证.下列实验方案设计不合理的是( )
| 选项 |
实验目的 |
试验方法 |
| A |
检验一瓶气体是否为氧气 |
将带火星的木条伸入瓶中 |
| B |
鉴别NaOH溶液和稀H 2SO 4 |
分别滴加紫色石蕊溶液 |
| C |
除去CO中混有的CO 2 |
将混合气体通过灼热的氧化铜粉末 |
| D |
比较Fe、Cu和Ag的金属活动性 |
将Fe和Ag分别加入CuSO 4溶液中 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
下列实验方案设计中,不能达到实验目的的是( )
| 选项 |
实验目的 |
实验方案 |
| A |
除去硫酸钾溶液中的氯化钾 |
加入适量硝酸银溶液,过滤 |
| B |
证明铝的金属活动性强于铜 |
将打磨过的铝丝浸入硫酸铜溶液中 |
| C |
鉴别稀盐酸和氢氧化钾溶液 |
分别滴加酚酞溶液 |
| D |
鉴别氢氧化钠、氯化钠、硝酸铵固体 |
分别加入适量蒸馏水溶解 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
到19世纪末,经几代科学家对光合作用的不断探索,得到结论:光合作用反应物是H2O和CO2,产物是O2和有机物。为了探究产物O2中的O元素来源,科学兴趣小组从元素守恒的角度进行了猜想。
猜想一:O2全部来源于CO2;
猜想二:O2全部来源于H2O;
猜想三:O2同时来源于两者。
为了求证,他们查阅资料如下:
资料1 19世纪末,科学家普遍认为气体之间更容易转化,认为CO2在光的作用下被分解成CO和O2,所以O2来自于同为气体的CO2。
资料2 1937年,英国化学家希尔通过实验发现:离体叶绿体在光照条件下使水分解,释放出O2,并还原电子受体。
资料3 1939年,已经发现了氧的同位素。美国科学家鲁宾、卡门利用 O标记的H2 O和C O2分别培养小球藻,光照相同时间后,检测甲、乙两试管中产生的氧气是否含 O,如图所示。
根据所学知识,结合资料回答下列问题:
(1)资料2的实验结论 (填“支持”或“不支持”)资料1的观点。
(2)根据资料3的实验结果,分析可得猜想 成立。

除去下列物质中的少量杂质(括号内为杂质)的方法,正确的是( )
选项 |
物质(杂质) |
试剂或方法 |
A |
铜(氧化铜) |
在空气中灼烧 |
B |
二氧化碳(一氧化碳) |
通入氧气,点燃 |
C |
硫酸亚铁溶液(硫酸) |
加过量的铁粉,过滤 |
D |
氯化钠(泥沙) |
加水溶解、过滤、洗涤、干燥 |
A.AB.BC.CD.D
试题篮
()