下列实验目的对应实验方案正确的是( )
实验目的 |
实验方案 |
|
A |
除去氯化钾溶液中的氯化铜 |
加入氢氧化钠溶液至不再产生沉淀 |
B |
鉴别碳酸铵、硫酸铵、硝酸铵三种氮肥 |
用氢氧化钡溶液 |
C |
除去CO中少量H2O和CO2 |
先通过浓硫酸,再通过氢氧化钠溶液 |
D |
鉴别纯铝和硬铝 |
将两者相互刻画,比较硬度 |
A.AB.BC.CD.D
下列有关实验方案设计正确的是( )
选项 |
实验目的 |
实验方案 |
A |
配制6%的氯化钠溶液50g |
称取3g氯化钾固体溶于47mL水中 |
B |
证明氢氧化钠溶液与稀盐酸能反应 |
取氢氧化钠溶液于烧杯中,滴入几滴酚酞溶液,振荡,再滴入稀盐酸至溶液变为无色 |
C |
除去CaCl2溶液中的少量盐酸 |
加入适量的铁粉 |
D |
除去CO2中含有的少量CO |
点燃 |
A.AB.BC.CD.D
某化学活动小组在一次实验中进行了如图1所示实验,先向A中注入一定量氯化铁溶液。再注入一定量硫酸钠溶液,此过程中观察到的现象是(1) 。小组同学对无色溶液B产生了浓厚的兴趣,进行了进一步的探究活动。
【提出问题】B中含的离子有什么?
【实验探究】
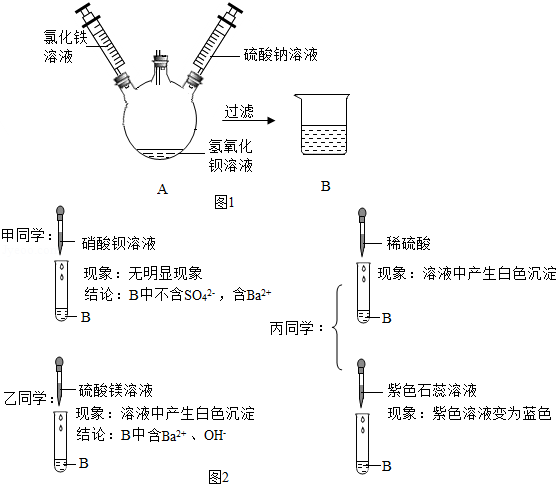
【评价交流】甲同学结论(2) (填"正确"或"错误");乙同学的探究过程不正确,理由是(3) 。
【实验结论】结合上述实验最终确定B中含有(4) (填离子符号),不含(5) (填离子符号)。
【归纳总结】由甲、乙、丙同学实验对比得出,确定溶液中可能存在的不同离子是否存在的方法是:可根据待测离子与所加试剂反应(6) 。确定出存在的离子,同时推测出与(7) 。
下列实验事实不成立的是( )
| A. |
用酚酞溶液可鉴别稀盐酸、氢氧化钠溶液和氯化钠溶液 |
B. |
除去炭粉中混有的少量氧化铜粉末,可加足量稀硫酸后过滤 |
| C. |
Ba 2+、OH ﹣、NO 3 ﹣、Na +四种离子在溶液中可以同时存在 |
D. |
分离氯化钠和碳酸钠两种固体,先加适量的稀盐酸,再蒸发 |
化学与生活紧密相联,以下源自生活的实验不能达到目的是( )
| A. |
用两片金属相互刻划比较硬度大小 |
B. |
用食盐水制作叶脉书签 |
| C. |
用肥皂水鉴别硬水和软水 |
D. |
用紫甘蓝叶和酒精溶液制酸碱指示剂 |
2018年“世界水日”的宣传主题为“Nature for water”。
(1)爱护水资源,一方面要防治水体污染,另一方面要
(2)“直饮水机”可将自来水净化为饮用水,其内部使用的活性炭主要起 ,生活中常用 检验饮用水是硬水还是软水,常用的 方法降低水的硬度,并起到消毒杀菌的作用。
(3)图1为电解水的实验装置图。通电一段时间后,玻璃管b中收集到的气体是 ,该实验说明水是由
组成的。
(4)ClO2是饮用水常用的消毒剂,制取ClO2的化学方程式为:Cl2+2NaClO2═2C1O2+2X,X的化学式
(5)下列图2是初中化学中常见的实验。相关说法错误的是 (填序号)。
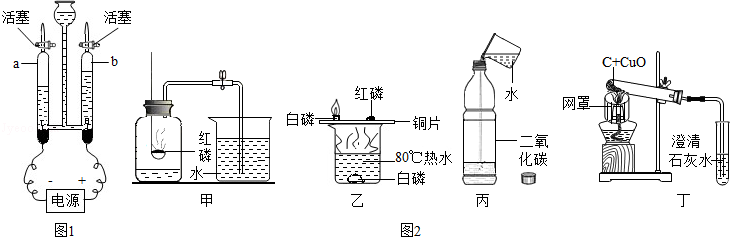
①甲实验的目的是测定空气中氧气的含量
②乙实验,水中的白磷没有燃烧,是因为温度没有达到着火点
③丙实验加水后,立即旋紧瓶盖,振荡,看到的现象是软塑料瓶向内凹陷
④丁实验,酒精灯上放的金属网罩是为了提高温度
实验是进行科学研究的重要手段,实验方案的设计是实验成功的基本保证.下列实验方案设计不合理的是( )
| 选项 |
实验目的 |
试验方法 |
| A |
检验一瓶气体是否为氧气 |
将带火星的木条伸入瓶中 |
| B |
鉴别NaOH溶液和稀H 2SO 4 |
分别滴加紫色石蕊溶液 |
| C |
除去CO中混有的CO 2 |
将混合气体通过灼热的氧化铜粉末 |
| D |
比较Fe、Cu和Ag的金属活动性 |
将Fe和Ag分别加入CuSO 4溶液中 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
下列实验方案设计中,不能达到实验目的的是( )
| 选项 |
实验目的 |
实验方案 |
| A |
除去硫酸钾溶液中的氯化钾 |
加入适量硝酸银溶液,过滤 |
| B |
证明铝的金属活动性强于铜 |
将打磨过的铝丝浸入硫酸铜溶液中 |
| C |
鉴别稀盐酸和氢氧化钾溶液 |
分别滴加酚酞溶液 |
| D |
鉴别氢氧化钠、氯化钠、硝酸铵固体 |
分别加入适量蒸馏水溶解 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
到19世纪末,经几代科学家对光合作用的不断探索,得到结论:光合作用反应物是H2O和CO2,产物是O2和有机物。为了探究产物O2中的O元素来源,科学兴趣小组从元素守恒的角度进行了猜想。
猜想一:O2全部来源于CO2;
猜想二:O2全部来源于H2O;
猜想三:O2同时来源于两者。
为了求证,他们查阅资料如下:
资料1 19世纪末,科学家普遍认为气体之间更容易转化,认为CO2在光的作用下被分解成CO和O2,所以O2来自于同为气体的CO2。
资料2 1937年,英国化学家希尔通过实验发现:离体叶绿体在光照条件下使水分解,释放出O2,并还原电子受体。
资料3 1939年,已经发现了氧的同位素。美国科学家鲁宾、卡门利用 O标记的H2 O和C O2分别培养小球藻,光照相同时间后,检测甲、乙两试管中产生的氧气是否含 O,如图所示。
根据所学知识,结合资料回答下列问题:
(1)资料2的实验结论 (填“支持”或“不支持”)资料1的观点。
(2)根据资料3的实验结果,分析可得猜想 成立。

除去下列物质中的少量杂质(括号内为杂质)的方法,正确的是( )
选项 |
物质(杂质) |
试剂或方法 |
A |
铜(氧化铜) |
在空气中灼烧 |
B |
二氧化碳(一氧化碳) |
通入氧气,点燃 |
C |
硫酸亚铁溶液(硫酸) |
加过量的铁粉,过滤 |
D |
氯化钠(泥沙) |
加水溶解、过滤、洗涤、干燥 |
A.AB.BC.CD.D
下列关于物质的鉴别、除杂所选用的试剂或方法错误的是( )
| 选项 |
实验目的 |
试剂或方法 |
| A |
鉴别FeCl 3、NaCl、NaOH、MgCl 2四种溶液 |
不另加试剂 |
| B |
鉴别CaCO 3、NaOH、NaCl、NH 4NO 3四种固体 |
水 |
| C |
除去MgCl 2溶液中少量的CuCl 2 |
加入过量铁粉、充分反应、过滤 |
| D |
除去N 2中的少量CO |
将气体缓缓通过灼热的氧化铜 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
已知金属钴(Co)的活动性与铁相似,请预测氯化钴(CoCl2)的化学性质,说明预测的依据,并设计实验验证。经查阅资料,钴的化合物相关性质如下:
物质 |
CoO |
Co(OH)2 |
CoCl2 |
CoSO4 |
Co(NO3)2 |
CoCO3 |
在水中的溶解性 |
难溶于水的灰绿色固体 |
难溶于水的粉红色固体 |
易溶于水形成粉红色溶液 |
易溶于水形成粉红色溶液 |
易溶于水形成粉红色溶液 |
难溶于水的粉红色固体 |
限选试剂:CoCl2溶液、(NH4)2CO3溶液、Na2SO4溶液、AgNO3溶液、NaOH溶液、稀硫酸、镁条、铜片。
预测 |
预测的依据 |
验证预测的实验操作与预期现象 |
①能够与含Ag+的 可溶性盐反应 |
CoCl2 溶液中含Cl﹣, AgCl难溶于水。 |
取少量CoCl2溶液于试管中, ,如果观察到 ,则预测成立。 |
②能够与 (填物质类别)反应 |
|
取少量CoCl2溶液于试管中, ,如果观察到 ,则预测成立。 |
③能够与 (填物质类别)反应 |
|
取少量CoCl2溶液于试管中, ,如果观察到 ,则预测成立。 |
实验室里区分下列物质的两种实验方法都正确的是( )
| |
物质 |
方法1 |
方法2 |
| A |
甲烷和一氧化碳 |
将气体点燃,观察现象 |
分别通入灼热的氧化铜,观察现象 |
| B |
碳酸钠和硫酸铵 |
取样,溶解后分别滴入无色酚酞溶液,观察现象 |
取样,分别加Ca(OH) 2固体,研磨后闻气味 |
| C |
酒精和白醋 |
取样,品尝二者的味道 |
取样后分别点燃,观察现象 |
| D |
木炭粉和氧化铜 |
取样,分别加入稀H 2SO 4,观察现象 |
观察物质的颜色 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
硫酸氢钠(NaHSO4)溶于水形成无色溶液,小明预测其化学性质并设计实验验证。下列有关说法不正确的是( )
A.依据Ba2+与SO42﹣反应生成BaSO4沉淀,预测NaHSO4能与含Ba2+的盐反应
B.向NaHSO4溶液中滴入BaCl2溶液,若有白色沉淀生成,则证明NaHSO4能与含Ba2+的盐反应
C.向少量NaOH溶液中滴入NaHSO4溶液,通过观察溶液颜色的变化,验证NaHSO4与碱反应的预测是否正确
D.向NaHSO4溶液中滴入Na2CO3溶液,有气泡产生,证明NaHSO4溶液呈酸性
氢氧化镍是某种混合动力汽车电池的一种材料。镍原子结构示意图为Ni
(1)镍原子最外层电子数是 ;
(2)氢氧化镍的化学式为 ,从组成上看,它属于 (选填"氧化物"、"酸"、"碱"、"盐"),预测该物质能与稀硫酸发生反应。
(3)按实验方案设计的路径,寻找两物质发生反应的证据。
查阅资料:①氢氧化镍:蓝绿色微溶于水的固体
②硫酸镍溶液呈绿色
③碳酸镍:浅绿色难溶于水的固体
| 路径 |
步骤 |
现象 |
结论 |
| 反应物角度 |
取少量氢氧化镍(新制)悬浊液于试管中,向其中滴加过量稀硫酸,振荡 |
① |
氢氧化镍和稀硫酸反应的化学方程式 ④ |
| 生成物角度 |
② |
③ |

试题篮
()