一定条件下,某物质溶解于水的实验数据如下表,请回答有关问题。
| 实验序号 |
温度/℃ |
水的质量/g |
所加物质质量/g |
溶液质量/g |
| ① |
20 |
10 |
2 |
12 |
| ② |
20 |
15 |
2.5 |
a |
| ③ |
20 |
20 |
7 |
26 |
| ④ |
30 |
20 |
7 |
27 |
(1)表中a= 。
(2)20℃时,该物质的溶解度为 。
(3)右图中,能表示该物质溶解度的曲线是 (填字母)。 
(4)所得溶液一定为饱和溶液的是 (填实验序号,下同); 所得溶液中溶质质量分数最大的是 。
(5)温度不变,将①、②所得溶液混合后,向其中再加入 g该物质,能使溶液恰好达到饱和。
右图为氯化钠、碳酸钠在水中的溶解度曲线。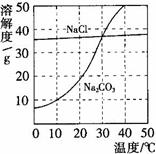
(1)氯化钠溶液中的溶剂是 。
(2)10℃时,碳酸钠的溶解度为 g。
(3)30℃时,氯化钠的溶解度 碳酸钠的溶解度。(填写“>”、“<”或“=”)
(4)10℃时,向两只盛有100g水的烧杯中,分别加入氯化钠、碳酸钠两种物质,至不再溶解为止,所得溶液的溶质质量分数最大的是 溶液。(填化学式)
(5)如右图所示,20℃时,将盛有饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是____________。(填字母序号)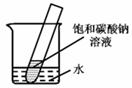
| A.干冰 | B.氢氧化钠固体 | C.生石灰 | D.硝酸铵 E.浓硫酸 |
右图是氯化钠和硝酸钾两种固体物质的溶解度曲线。
(1)硝酸钾溶液中的溶剂是 。
(2) 图中b表示 的溶解度曲线。
(3)某兴趣小组为了研究NaCl和KNO3的溶解和结晶,做了两组实验(室温下),其过程如下:
【第一组】
【第二组】
上述实验过程中所得溶液一定达到饱和的是(填数字序号,下同)__________;溶质质量分数一定相等的是 。
(4分)下列数据是硝酸钾固体在不同温度时的溶解度。
| 温度/℃ |
0 |
20 |
40 |
60 |
80 |
| 溶解度/g |
13.3 |
31.6 |
63.9 |
110 |
169 |
⑴硝酸钾溶液中的溶剂是 。
⑵观察上述表格,可以总结出的规律是 (答出一条即可)。
⑶ 40℃时,向50g水中加入30g硝酸钾,充分溶解后得到 (填“饱和”或“不饱和”)溶液。
⑷右图所示,小烧杯中盛放的是底部有未溶解硝酸钾的溶液(20℃),若使其固体继续溶解,在大烧杯的水中可以加入的物质有 (用字母序号表示)。
A.干冰 B.硝酸铵 C.生石灰 D.熟石灰 E.氢氧化钠
右图是常见固体物质的溶解度曲线,根据图示回答:
(1)曲线上M点表示 ,t3℃时,A、B、C三种物质的溶解度由大到小的顺序为 。
(2)t1℃时,将10g A物质放入100g水中,充分溶解后所得的溶液是 (填“饱和”或“不饱和”)溶液。欲使t2℃时C物质的饱和溶液变为不饱和溶液,可采取的方法是
(任填一种方法)。
(3)现有30℃的不饱和KNO3溶液,与该溶液有关的量有:
①水的质量 ②溶液中KNO3的质量 ③KNO3的质量分数
④30℃时KNO3的溶解度 ⑤溶液的质量
Ⅰ.在该不饱和溶液中加硝酸钾至饱和,不变的量有 (填序号,下同)。
Ⅱ.将该不饱和溶液恒温蒸发至饱和,不变的量有 。
根据图1和图2回答问题:

图1 图2
(1)甲、乙溶液中的溶剂是 。
(2)在t1℃时,等质量的甲、乙两种固体物质在水中的溶解现象如图1所示,要使剩余的甲固体继续溶解可采用的方法是 。
(3)图2中a、b分别表示上述两种物质的溶解度曲线,在 ℃时,这两种物质的溶解度相等;b表示的是 物质(填“甲”或“乙”)的溶解度曲线。
(4)右图所示,小烧杯中盛放的是t2℃时所得的甲物质的饱和溶液。若将适量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,一定能够使小烧杯中有固体析出的是 (填字母)。
| A.冰 | B.浓硫酸 | C.硝酸铵 | D.干冰 |
E.氢氧化钠 F.氧化钙
下图是a、b、c三种物质(均不含结晶水)的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答:
(1)P点的含义是 ;
(2)欲将t2℃时c物质的饱和溶液变为不饱和溶液,可采用的方法是 和 ;
(3)t2℃时将50g a物质加入到80g水中充分溶解,所得溶液质量是 g;
(4)t2℃时,将a、b、c三种物质的饱和溶液各100g,分别降温到t1℃,所得三种溶液的质量大小关系是 (填序号)。
Ⅰ.b>a=c Ⅱ.a=b>c
Ⅲ.b>a>c Ⅳ.c>b>a
食盐在生活中具有广泛的用途。
(1)常温下,用氯化钠和水配制100 g溶质质量分数为5%的溶液时,必须用到的仪器有:托盘天平、药匙、胶头滴管、玻璃棒、量筒和 ,其中玻璃棒的作用是 。
(2)上述氯化钠来自于粗盐提纯,粗盐提纯的主要步骤是溶解、 和蒸发。在蒸发过程中,待蒸发皿中出现较多固体时,停止加热,这样操作的目的是 。
(3)海水晒盐能够得到粗盐和卤水。卤水中含有MgCl2、KCl和MgSO4等物质,下图是它们的溶解度曲线。
t1℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液中,溶质质量分数最大的是 。将t2℃的MgCl2、KCl和MgSO4三种物质的饱和溶液降温至t1℃时,可能会析出的晶体有 (填字母序号)。
A.MgCl2和KCl B.只有MgSO4 C.MgCl2、KCl和MgSO4
下图为A、B、C三种固体物质的溶解度曲线。
(1)在______℃时,A、B两物质饱和溶液的溶质质量分数相等。
(2)在t3℃时,10g水最多能溶解3gB物质,则10g水最多能溶解A物质的质量______3g(填“>”、“<”或“=”)。
(3)三种物质的溶解度关系为B>A>C时的温度为 t℃,则t的取值范围是_____。
(4)将t3℃时A、B、C的饱和溶液降温到t1℃,溶质质量分数保持不变的是 。
下图是A、B、C三种物质的溶解度曲线,据图回答:
(1)P点表示t1℃时 物质的溶解度相等。
(2)溶解度随温度升高而减少的物质是 。
(3)t2℃时,三种物质的溶解度由大到小的顺序是 。
(4)t1℃时A的溶解度 t2℃时A的溶解度;(填“大于”、“小于”或“等于”,下同)
(5)t2℃时,B的饱和溶液中溶质的质量分数 A的饱和溶液中溶质的质量分数。
结合如图的溶解度曲线图回答问题.

(1)欲配制100g 0.9%的生理盐水,需要
的质 量为g.
(2)由右图可知,硝酸钾的溶解度随温度升高而;P点表示的意义是.
(3)若从氯化钠和硝酸钾的饱和溶液中提取硝酸钾,应采用下列方法中的(填字母代号).
a.冷却结晶 b.蒸发结晶.
如图a所示,是甲、乙两种物质的溶解度曲线图,图b中所示两个烧杯中各盛有20℃时上述两种物质的饱和溶液。请你通过分析,回答下列问题:
⑴溶解度随温度升高而增大的物质是 ;填“甲”或“乙”)
⑵40℃时,甲物质与乙物质的溶解度 ;(填“相等”或“不相等”)
⑶80℃时,100g水中最多可溶解甲物质 g;
⑷当温度由20℃升高到60℃时(不考虑水分蒸发),B烧杯中固体质量增加,则B烧杯溶液中的溶质是 (填“甲”或“乙”)。
(4分)如图是A、B、C三种物质的溶解度曲线。看图回答问题:
(1)在 ℃时,A、B两种物质的溶解度相同。
(2)在t1℃时,将40 g A物质放入l00 g水中充分搅拌,所得溶液的质量是 g.
(3)当B中混有少量A时,可用 的方法得到较纯净的B。
(4)在t2℃,将一定质量A物质的饱和溶液降温至t1℃,该过程中没有发生改变的是
(填序号)。
①溶质的质量 ②溶剂的质量 ③溶液的质量 ④溶质的质量分数
右图为氯化钠、碳酸钠在水中的溶解度曲线。
请回答下列问题:
(1)氯化钠溶液中的溶剂是 ;
(2)10℃时,碳酸钠的溶解度为 g;
(3)30℃时,氯化钠的溶解度 碳酸钠的溶解度(填写“>”、“<”或“=”);
(4)10℃时,向两只盛有100g水的烧杯中,分别加入氯化钠、碳酸钠两种物质,至不再溶解为止,所得溶液的溶质质量分数大的是 溶液(填化学式);
(5)如右图所示,20℃时,将盛有饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是________(填字母序号)。
| A.氢氧化钠 | B.生石灰 | C.硝酸铵 | D.浓硫酸 |
试题篮
()