我省多个城市濒临南海,有丰富的海洋资源。海洋是一个巨大的资源库,我们可以从海水中提取食盐,并以此为原料制得具有广泛用途的烧碱。制取的主要工艺流程如下:
(1)利用风吹日晒可以从海水中提取粗盐,风吹日晒的主要作用是 。
(2)常用过滤的方法除去食盐中混有的泥沙,该操作中玻璃棒的作用是 。
(3)粗盐中还含有Na2SO4、CaCl2、MgCl2等可溶性杂质,除杂质时所加的四种试剂是NaOH溶液、Na2CO3溶液、BaCl2溶液、盐酸(均过量),其中加入NaOH溶液的目的是 ,除杂质时先加BaCl2溶液后加Na2CO3溶液的理由是 。
(4)该化工厂将副产品氢气和氯气加以利用:氢气在氢气中燃烧生成氯化氢,氯化气溶于水得到盐酸。写出氢气在氯气中燃烧的化学方程式 ,通过这个化学反应你对燃烧的新认识是 。
、
两种固体物质的溶解度曲线如图所示,请根据曲线图回答下列问题。
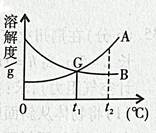
(1)现有常温下
的不饱和溶液,在只要求保持其中溶剂质量不变的条件下,将其变成饱和溶液,可行的方法有。
(2)现有一杯
时含
、
两种物质且均饱和的混合溶液,若要从中分离出少量A的纯净物,其操作方法是。
(3)下列说法正确的是。
①
时,
的溶液中溶质的质量分数一定比B的溶液中溶质的质量分数大;
② 将
,
、
的饱和溶液分别降温至
,此时两溶液中的质量分数相等;
③ 在
时,用两份等量的水分别配制成
、
的饱和溶液,这两种溶液的质量相等;
④ 在
时,用等量的
、
分别配制成两种饱和溶液,测得其质量依次为
和
,则
。
有一种固体混合物质
,其中只可能含有
、
、
、
、
中的一种或几种。请根据以下实验操作回答下列问题。
操作① 取少量
放入足量的水中充分搅拌、静置,得到白色沉淀和无色溶液,过滤。
操作② 向滤出的沉淀中加入足量稀盐酸,沉淀全部溶解,此时所得溶液仍为无色。
(1)
中一定不含的物质是,不能确定是否含有的物质是。
(2)上述实验过程中,发生反应的化学方程式为、。
(3)向操作①后所得的无色溶液中滴加溶液
溶液,一定能发生的反应的化学方程式为。
自然界中有多种多样的物质,如下图:

(1)构成物质的微粒有等。
(2)上图物质中属于有机物的是,常温下呈液态的金属单质是;属于碱的是,用
试纸测定其酸碱度的操作是。
(3)下图是硫酸铜溶液与锌粒反应前后溶液中主要离子变化示意图。

反应中过量的物质是(写化学式)。
已知某固体混合物A中可能含有
、
、
、
、
五种物质中的两种或多种。按下述步骤进行实验探究,观察实验现象,并加以分析推理(设过程中所有发生的反应都恰好完全反应)。
I.取一定质量的该固体混合物A放入一洁净烧杯中,向其中加入适量
溶液,搅拌,待烧杯中物质充分反应后,过滤,得红褐色沉淀
和滤液
。
Ⅱ.另取一定质量的该固体混合物A放入另一洁净烧杯中,向其中加入适量
溶液,搅拌,待烧杯中物质充分反应后,过滤,得白色沉淀
和滤液
。
III.将所得滤液C和滤液E充分混合,再向混合后的溶液中加入适量
溶液,待充分反应后,过滤,得白色沉淀
和滤液
。
Ⅳ.根据上述实验过程和发生的现象做出相应推理,填写以下空白:
(1)在固体混合物A里,上述五种物质巾肯定存在的物质是(写化学式)
(2)写出步骤III中生成白色沉淀F的1个化学方程式
(3)在滤液
中,含有的金属阳离子共有种,该滤液中肯定存在的酸根离子。
(4)在混合物
里,上述五种物质中肯定不存在的物质是(写化学式)。得出此结论的理由是。
含锌废渣和各种锌矿(如菱锌矿)都有着重要的用途
I.以含锌废渣(主要成分为
,杂质为
﹑
)为原料制备七水硫酸锌(
)的流程如下。

(1)粉碎的目的是。
(2)若实验室用质量分数为98%的硫酸配制200g25%的硫酸,需要的玻璃仪器有胶头滴管﹑玻璃棒﹑和,此处玻璃棒的作用是。
(3)物质X是,滤渣中含有的金属单质有,除铜时发生的反应属于反应(填基本反应类型)。
(4)流程中获得七水硫酸锌前省略的操作是﹑冷却结晶﹑洗涤和低温烘干。
(5)某温度下,
分解得到一种铁﹑氧质量比21:8的氧化物,该氧化物的化学式。
(6)除铁过程中,温度pH对除铁效果的影响分别对如图所示。由图可知,除铁时温度应控制在℃为宜,pH应控制在为宜。

II.以某菱锌矿(
含量为62.5%)为原料制备锌的原理如下(假设杂质不参加反应):
则100吨这样的菱锌矿理论上最多制得锌多少吨?(写出计算过程)
一定条件下, 与 反应会生成三种氧化物。某兴趣小组用如下装置探究该反应。
已知
,
均能使澄清石灰水变浑浊。

(1)仪器的名称是
。
中
的化合价是。
(2)装置
中
的分解会生成一种气体和一种相对分子质量为100的盐,则
中反应的反应化学方程式。
(3)实验时观察到装置
中紫红色褪去,装置
中溶液变浑浊,则在
和
中反应的气体分别是﹑。
(4)装置
中反应的化学方程式是。装置
的作用是。
(5)该装置的明显不足之处是。
食盐是一种重要的化工原料。请回答下列问题。
(1)请完善实验室除去粗盐中泥沙等难溶性杂质的实验步骤。
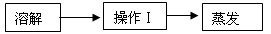
①操作Ⅰ所用的玻璃仪器有:烧杯、玻璃棒和。
②在蒸发过程中,待时,停止加热,利用余热将滤液蒸干。
(2)由于粗盐中含有少量
,
、
等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如下图。
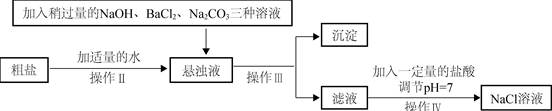
①加入稍过量的
溶液除了能除去粗盐中的
外,它还有一个作用是(用化学方程式表示)。
②通过操作Ⅲ所得滤液中的溶质有(用化学式表示)。
(3)若有溶质质量分数为10%的氯化钠不饱和溶液100 kg,要将其变成20 ℃时氯化钠的饱和溶液,以满足化工生产的需要,可采用的最简便方法是。已知:20 ℃时氯化钠的溶解度为36g。
、
、
在不同溶剂中的溶解度如下表所示。
表1
、
、
分别在水中的溶解度(
)
|
/℃ |
|||
| 0 |
42 |
7.1 |
35.7 |
| 10 |
51 |
12.2 |
35.8 |
| 20 |
109 |
21.8 |
36.0 |
| 30 |
119 |
39.7 |
36.3 |
表2 常温下,
、
、
分别在乙醇中的溶解度(
)
| 17.3 |
<0.01 |
0.1 |
根据表1和表2提供的数据回答下列问题:
(1)
在水中的溶解度随温度升高而(填"增大"或"减小")
(2)20℃时,饱和食盐水中溶质的质量分数为(计算结果精确到0.1﹪);
(3)为证明
能与
发生反应,小明同学将
通入饱和
的乙醇溶液中。请推测该实验可观察到的现象,推测依据是。
溶解度是物质溶解性的定量表示,溶解度曲线可表示物质在不同温度下的溶解度。甲、乙两种物质的溶解度曲线如图所示,根据图示回答下列问题:

(1)甲、乙两种物质中溶解度受温度影响较大的是 物质。
(2)若甲物质中混有少量的乙物质,提纯甲物质最好采取的方法是 (填“降温结晶”或“蒸发结晶”)。
(3)t2℃时,乙物质的溶解度为 g;t2℃时,若将30g乙物质加入到50g水中,所得溶液的溶质质量分数是 (计算结果精确到0.1%)。
(4)将t1℃的甲、乙两物质的饱和溶液(均无固体物质剩余)升温到t2℃时,所得甲物质溶液的溶质质量分数 乙物质溶液的溶质质量分数(填“大于”“小于”“等于”之一)。
某校化学兴趣小组的同学,开展了测定Na2CO3和NaCl的固体混合物中Na2CO3质量分数的探究实验。他们设计了如下实验方案:
(1)“操作Ⅰ”的名称是 ,溶液M中的溶质是 (写化学式)。
(2)滴加CaCl2溶液应“过量”,否则会使测定的结果 (填“偏大”或“偏小”)。
(3)计算该混合物中Na2CO3的质量分数(写出计算过程,计算结果精确至0.1%)。
K2SO4是无氯优质钾肥,Mn3O4是生产软磁铁氧体材料的主要原料。以硫酸工业的尾气联合制备K2SO4和Mn3O4的工艺流程如下:
【相关资料】(1)含水结晶盐受热时通常先失去结晶水;
(2)图2中物质B就是工业产品Mn3O4 ;
(3)Mn3O4在高温时会被氧化,且锰的化合价从+1到+7变化时逐级升高,如+2的锰先氧化到+3的锰,再从+3氧化到+4分别是对应的氧化物为三氧化二锰和二氧化锰。
【问题解答】
(1)反应II中加入的NH4HCO3中氮元素的化合价为 ;
(2)反应Ⅲ中,向(NH4)2SO4溶液中加入KCl溶液充分反应后,进行蒸发浓缩、结晶、 、洗涤、干燥等操作即得K2SO4晶体;
(3)试分析反应Ⅲ后有K2SO4析出的原因是____________________________;
(4)加热MnSO4·H2O固体时第一次质量减少的原因是 (用化学方程式表示);
(5)煅烧过程中固体锰元素的质量分数随温度的升高而增大。但当温度超过1000℃时,再冷却后,测得产物中的锰元素的质量分数反而减小。试分析产物中锰元素的质量分数减小的原因: 。
下表为两种物质在不同温度时的溶解度
| 温度/℃ |
0 |
20 |
40 |
60 |
80 |
100 |
|
| 溶解度/ | 27.6 |
34.0 |
40.0 |
45.5 |
51.1 |
56.7 |
|
| 13.3 |
31.6 |
63.9 |
110 |
169 |
246 |
请回答:
(1)60 ℃时,
的溶解度是
;
(2)40 ℃时,将30
加入到50
水中,充分溶解后所得溶液是溶液(填写"饱和"或"不饱和");
(3)将20 ℃时
和
的两种饱和溶液升温至60 ℃,则两种溶液的溶质质量分数大小关系是:
(填写">"、"<"或"=")。
根据如图回答问题:
(1)若选用A装置加热氯酸钾和二氧化锰制取氧气,还需补充的一种仪器是 反应的化学方程式为
(2)实验室若选用装置B制取二氧化碳,则需要改正的一点是 ,请你写出用石灰石与稀盐酸反应制取二氧化碳的化学方程式 ,将产生的二氧化碳气体通入澄清石灰水,可观察到的现象是
(3)用制取的二氧化碳进行试验:
①实验(Ⅱ)中溶液变 色;②实验(Ⅲ)中加热之后,溶液又变为 色,解释出现此现象的原因
(4)在装置B中用石灰石与稀盐酸反应制二氧化碳时,气体中可能的杂质有 (除空气外,写出两种物质的名称)。 将气体依次通过下列试剂可以除去这两种杂质,能达到目的的是(已知二氧化碳在饱和碳酸氢钠溶液中的溶解度很小) (填序号)
①硝酸银溶液 浓硫酸
②饱和碳酸氢钠溶液 浓硫酸
③硝酸银溶液 无水氯化钙固体
④硝酸银溶液 氢氧化钠和氧化钙固体
(1)冬季,大雪覆盖路面,给交通造成很多麻烦,散撒融雪剂可以使雪很快融化,有效地清除交通雪障。除使用融雪剂外,常使用铲雪车铲雪,铲雪车的铲斗是用锰钢制造的,锰钢属于 (填写序号字母)。
| A.合成材料 | B.合金 | C.金属材料 | D.复合材料 |
(2)氯化钙是常用的融雪剂。工业上以碳酸钙(含有少量Na+、Mg2+、Fe3+等杂质)生产氯化钙的主要流程如下:
①滤渣的主要成分是 、 (填化学式);
②加盐酸酸化,其目的之一是除去未反应的氢氧化钙,写出反应的化学方程式 ,该反应属于 反应(填基本反应类型)。
(3)已知盐酸盐(金属氯化物)跟AgNO3溶液反应生成白色沉淀。某公司生产的融雪剂由NaCl、NaNO3、MgCl2、CuSO4中的两种物质组成。小明为探究其成分,设计并完成下列实验:
请你推断:融雪剂中一定不含的物质是 (填写名称),融雪剂中一定含有的物质是 (填化学式)。
试题篮
()