如图所示的是实验室制取蒸馏水的简易装置,烧瓶和烧杯中都是自来水.

(1)酒精(C2H5OH)燃烧的化学方程式:.
(2)实验中消耗的40g酒精完全燃烧放出的热量为J.(酒精热值为3.0×107J/kg)
(3)实验结束后从试管和烧杯中各取10mL水,分别加入等量肥皂水,震荡.观察到的现象是:.
用如图实验方法分离
和
两种固体的混合物A,根据操作流程完成下列问题:
(1)B物质是.
(2)过滤操作中玻璃棒的作用是.
(3)经分析上述方法分离出的F含杂质,请对该设计方案加以完善.
(4)若用原操作方法,要测出混合物A中
和
的质量比,不称量D,可通过称量和的质量求解.
请按要求完成下列金属性质的实验:
研究一:金属与酸反应过程中的能量变化.
(1)打磨后的镁条与稀盐酸反应,试管外壁发烫,说明该反应(填"吸热"或"放热"),反应的化学方程式为.
(2)实验测得反应中产生的气体的速率(
)与时间(
)的关系如图,请根据时间
段反应速率变化,说明化学反应速率受等因素影响.

研究二:金属与盐溶液反应过程中的相关变化.
(1)某同学用硫酸铜溶液把"铁勺"变"铜勺",其反应的化学方程式为.
(2)在一定量
和
的混合溶液中加入铁粉,充分反应后,下图描述相关变化曲线,一定不正确的是.

溶解度是解决溶液相关问题的重要依据.
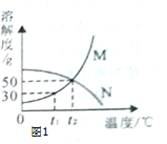
Ⅰ.根据图1解决下列问题:(
,
均不含结晶水)
(1)温度为
时,
,
两种物质的溶解度相等;
(2)
时,将20g
加入50g水中,充分溶解,形成溶液的质量为g.保持温度不变,向该溶液中再加入10g水充分搅拌,溶液的溶质质量分数将(填"变大"、"变小"或"不变");
(3)
时,将25g
加入50g水中,完全溶解后要提高该溶液的溶解质量分数,其操作方法是.
Ⅱ.根据表格解决实际问题:
| 温度/ | 20 |
30 |
50 |
80 |
90 |
|
| 溶解度/g |
|
31.6 |
45.8 |
85.5 |
100 |
169 |
|
|
110 |
114 |
121 |
126 |
139 |
某
样品中含有少量
,其提纯过程如图2: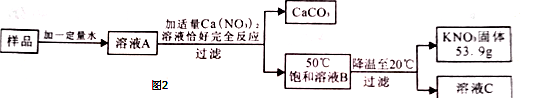
(1)图2中溶液
是(填"饱和"或"不饱和")溶液;
(2)样品中钾元素的质量为g(结果保留整数).
小明同学利用已使用过的生石灰干燥剂和敞口放置在空气中的烧碱固体进行了一系列实验,如下是他的实验记录:
①取干燥剂和烧碱固体同时放入水中,搅拌后过滤,得到白色固体甲和滤液乙。
②把白色固体甲分成两份,一份放入水中,搅拌后过滤,向滤液中滴加无色酚酞,滤液为无色;另一份加入溶液丙,产生气泡。
③向滤液乙中加入过量溶液丁,充分反应后过滤,得到白色固体甲和滤液,向滤液中滴加无色酚酞,滤液为无色。
④试根据以上的实验记录,回答下列问题:
(1)①步骤中的白色固体甲来源于
(2)滤液乙、溶液丙、溶液丁三种溶液的溶质所属的物质种类有 (填序号)
A.酸 B.碱 C.盐
(3)写出步骤③中发生的化学反应方程式:
(4)下列说法正确的是( )
A.生石灰干燥剂仍有干燥作用
B.生石灰干燥剂已完全失效
C.烧碱固体部分变质
D.烧碱固体完全变质
某兴趣小组设计的趣味小实验装置如图所示。A、B是两个系在玻璃导管一端的气球,C是胶头滴管。经检验该装置气密性良好。若锥形瓶和胶头滴管中分别装入相应的试剂组合(假设药品均足量),充分振荡后,气球会发生相应的变化。
(请写出符合要求的试剂组合(仅写两种),但所用方案的原理不能重复!)
(1)若A球迅速膨胀而B球无明显变化,则锥形瓶与滴管中的试剂可能的组合是:① 、 ,② 、 。
(2)若B球迅速膨胀而A球无明显变化,则锥形瓶与滴管中的试剂可能的组合是:
① 、 ,② 、 。
根据下面部分金属的活动性顺序回答:

(1)上述金属中活动性最强的是;
(2)按年代最早被广泛使用的金属是;
(3)已知:①
②
③
与稀硫酸不反应。则符合要求的
、
、
分别是(填字母序号)。
| A. |
、 、 |
B. |
、 、 |
C. |
、 、 |
下图为甲、乙两种物质的溶解度曲线,请回答下列问题:
(1)20℃时,为使接近饱和的甲物质溶液变为饱和溶液的方法是: (任写一种方法即可);
(2)40℃时,乙物质的溶解度是____g。此温度下,该饱和溶液中乙物质的质量分数是 (精确到0.1%)。
金属材料在生产、生活与科学研究中应用广泛。
(1)钢铁是使用最多的金属材料,钢的硬度比纯铁的硬度(填"大"或"小")。
(2)自行车构件中的支架是铁制品,为防止它锈蚀,在其表面刷漆,其防锈原理是。
(3)某废旧站回收的混合金属中含有铜、金和少量的镍,经过初步处理成粉末后,随意将三种金属编号成X、Y、Z,进行如下回收流程:

①操作a的名称是。
②铜、金、镍三种金属的活动性由强到弱的顺序是。
③写出步骤IV反应的化学方程式。
水是宝贵的自然资源。
(1)下列常用净水方法,可以降低水的硬度的是(填字母序号)。
A.过滤 B.吸附 C.蒸馏
(2)下图表示氯化钠、硝酸钾、硫酸镁三种物质的溶解度曲线。请回答:
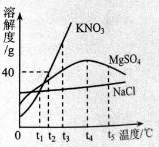
①
时,饱和溶液的溶质质量分数相同的两种物质是。
②
时,将40g硝酸钾放入60g水中,充分溶解后,所得溶液的质量为g。
③
时,溶解度最大的是。
④
时,其它条件不变,把硫酸镁饱和溶液升温到
,观察到的现象是。
⑤氯化钠溶液中含有少量硝酸钾杂质,提纯的方法是(填"蒸发溶剂"或"冷却热饱和溶液")。
如图是A、B两种物质的溶解度曲线,请回答:

(1)在40℃时A、B的溶解度大小关系是;
(2)a点是A、B两条曲线的交点,其含义是;
(3)20℃时将20g A固体放入50g水中,充分溶解后,所得溶液的质量是g;
(4)若A中含有少量的B杂质,提纯A的方法是结晶。
已知:镁在空气中燃烧生成氧化镁和氮化镁(
),氮化镁与水反应生成氢氧化镁和氨气。
(1)写出氮化镁与水反应的化学方程式 ;
(2)a 克镁在空气中完全燃烧生成固体的总质量m为;(用含a 的式子表示m 的取值范围)
(3)某学生对该混合物中氮化镁的质量分数进行测定,设计如下实验装置
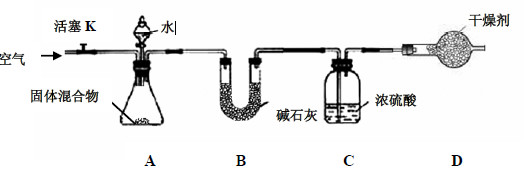
【查阅资料】
I.碱石灰是固体氧化钙和氢氧化钠的混合物,常用作干燥剂,不与
反应。
II.
III.
是一种极易溶于水的气体。
【实验步骤】①检查装置的气密性;②精确称量镁在空气中燃烧后的固体5.00g 放入锥形
瓶中,称量装置C,连接好装置;③关闭活塞K,打开A 中分液漏斗活塞,逐滴加入水,
至样品恰好完全反应;④打开活塞K,鼓入空气;⑤再次称量装置C,装置C 增重0.34g。
请回答:
(一)装置B 的作用是;
(二)装置D 的作用是;
(三)实验步骤④中鼓入空气的目的是;
(四)固体混合物中
的质量分数为;
(五)实验证明此方法测定的结果偏低,可能原因是(写一条)
(1)等质量的
、
两种物质分别与等质量的同浓度的稀盐酸充分反应,反应产生气体的质量与反应时间的关系如甲图所示。请回答下列问题:
①若
、
为
中的一种,则
是,反应结束后只有一种金属剩余,则剩余金属为。
②若
、
为碳酸钠粉末和碳酸钙块状固体中的一种,反应结束后,则它们消耗的酸(填"
多"、"
多"或"相等")。
反应至
点时,所得溶液的溶质为(写化学式)。
(2)如图所示,
、
、
、
、
分别是铁、硝酸铜溶液、二氧化碳、稀硫酸溶液、氢氧化钠溶液中的一种,
是硝酸铜溶液。("-"相连两物质能发生反应)请回答:

①
的化学式为,
物质的一种用途:。
②
与
反应的化学方程式,基本反应类型是。
下列是实验室制备CO2,并验证CO2性质的实验装置图,按要求回答下列问题:

(1)写出标号仪器的名称:①②
(2)在检查装置A的气密性操作时,当关闭活塞M和N,向仪器②中注水,观察到的现象,说明装置漏气。
(3)关闭活塞N,打开活塞M,向仪器②中加入稀盐酸,装置B处观察到的现象是:、,当观察到C处的石灰水变浑浊时,则C中发生的化学反应方程式是:
(4)关闭活塞M,打开活塞N。用A、D、E、F制取纯净干燥的CO2气体,装置D的作用是:,装置E中盛装溶液,用于出去CO2气体中的水分;当观察到,说明F中已收满二氧化碳气体。
(5)若关闭活塞M,打开活塞N。实验室要制取干燥的氧气用A、D、E、F、G中,只需选用的装置是(填编号),化学反应方程式是:
下表列出了KNO3与NaCl在不同温度时的溶解度:
| 温度(℃) |
0 |
10 |
20 |
40 |
60 |
80 |
100 |
| KNO3的溶解度(g) |
13.3 |
20.9 |
31.6 |
63.9 |
110 |
169 |
246 |
| NaCl的溶解度(g) |
35.7 |
35.8 |
36.0 |
36.6 |
37.3 |
38.4 |
39.8 |
(1)现有含123gKNO3与17.9gNaCl的混合物,某同学设计了以下实验除去KNO3中的NaCl(操作过程中不考虑额外的水损失).
①向混合物中加入适量水,加热溶解;
②继续加热溶液至100℃并恒温蒸发浓缩;
③将溶液降温至10℃,仅得到KNO3晶体,过滤,将所得KNO3晶体洗涤并干燥.
A.步骤②中,为确保没有晶体析出,溶液中至少要保留 g水;
B.步骤③中,最多可得到KNO3晶体 g;
C.根据上述实验可概括出除去KNO3中少量NaCl的主要步骤:加热溶解→蒸发浓缩→ →过滤→洗涤→干燥;
D.洗涤时,应选用少量 (选填“热水”或“冷水”).其目的是: ;
(2)除去NaCl中少量KNO3的一种方法是:将NaCl和KNO3的混合物置于适量水中,加热,搅拌,待KNO3全部溶解,趁热过滤,将过滤所得的NaCl晶体进行洗涤和干燥.上述方法中,趁热过滤的目的是: .
(3)取23.4gNaCl和40.4gKNO3,加70g水,加热溶解.在100℃时蒸发掉50g水,维持该温度过滤,得到的晶体质量为 g;将滤液冷却至10℃,充分结晶,写出析出的晶体的化学式: .
试题篮
()