(Ⅰ)某钠盐溶液中通入足量氨气,无明显现象。再在所得溶液中通入过量CO2,产生大量白色沉淀。
(1)写出氨气的电子式 。
(2)该钠盐溶液中一定不可能含有下列哪种微粒 (填编号)。
| A.Cl- | B.Fe2+ | C.SiO32- | D.AlO2- |
(3)写出一个通入过量CO2时生成白色沉淀的离子方程式 。
(Ⅱ)电镀工业中往往产生大量的有毒废水,必须严格处理后才可以排放。某种高浓度有毒的含A离子(阴离子)废水在排放前的处理过程如下:
已知:9.0g沉淀D在氧气中灼烧后,产生8.0g黑色固体,生成的气体通过足量澄清石灰水时,产生10.0g白色沉淀,最后得到的混合气体除去氧气后,还剩余标况下密度为1.25g/L的气体1.12L。
(4)沉淀D的化学式是 。
(5)写出沉淀D在氧气中灼烧发生的化学方程式 。
(6)滤液C中还含有微量的A离子,通过反应②,可将其转化为对环境无害的物质,试用离子方程式表示该原理 。
(7)反应①为制得某种元素的低价X离子,试从氧化还原反应的角度分析,是否可以用Na2SO3溶液来代替B溶液 ,
并设计实验证明所用Na2SO3溶液是否变质 。
最近,科学家在甲烷的低温活化与二氧化碳加氢研究上取得了突破,其反应原理如下: 。下列说法错误的是
。下列说法错误的是
| A.CO2、CH3COOH均为共价化合物 |
| B.每生成1molCH3COOH,要消耗22.4LCO2 |
| C.CO2、CH3COOH分子中均含σ键和π键 |
D. 属于氧化反应 属于氧化反应 |
二氯化二硫(S2C12)是广泛用于橡胶工业的硫化剂,其分子结构如图所示。常温下,S2C12是一种橙黄色液体,遇水易水解,并产生能使品红褪色的气体,化学方程式为:2S2C12+2H2O=SO2↑+3S↓+4HCl。下列说法中错误的是
| A.S2C12的结构式为Cl—S—S—Cl |
| B.反应中SO2是还原产物,S是氧化产物 |
| C.S2C12为含有极性键和非极性键的分子 |
| D.反应中,生成1molSO2,转移电子为3mol |
NA代表阿伏伽德罗常数。已知C2H4和C3H6的混合物的质量为ag,则该混合物
| A.所含共用电子对数目为(a/7+1)NA | B.所含碳氢键数目为aNA/7 |
| C.燃烧时消耗的O2一定是33.6a/14 L | D.所含原子总数为aNA/14 |
酚酞是中学阶段常用的酸碱指示剂,结构简式如图所示:下列关于酚酞的说法错误的是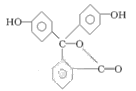
| A.酚酞与水可以形成氢键 |
| B.酚酞的分子式为C20H14O4 |
| C.酚酞结构中含有羟基(—OH),故酚酞属于醇 |
| D.酚酞在一定条件下能够发生加成反应 |
下列说法不正确的是:
① CO2分子的比例模型示意图:
②-OH与 组成元素相同,含有的电子数也相同
组成元素相同,含有的电子数也相同
③HCN分子的结构式:H-C≡N;
④NaHCO3在水中的电离方程式:NaHCO3 Na++H++CO32—;
Na++H++CO32—;
⑤Na2O的水溶液能导电,这不能说明Na2O是电解质;
⑥铝既能与盐酸反应又能与NaOH溶液反应,故铝是两性元素;
⑦风化、干馏、裂化都是化学变化
| A.①②⑤ | B.③④⑦ | C.①④⑥ | D.④⑤⑥ |
下列化学用语的书写,正确的是
A.氯原子的结构示意图: |
| B.6个质子8个中子的碳元素的核素符号:12C |
C.氯化镁的电子式: |
D.用电子式表示氯化氢的形成过程:  |
X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,R与Y处于同一主族,Z是短周期中金属性最强的金属元素, W的最高价氧化物对应水化物能与Z、R的最高价氧化物对应水化物均反应生成盐和水。下列说法正确的是
| A.元素Y、Z、W离子具有相同的电子层结构,其半径依次增大 |
| B.元素X与元素Y能形成两种化学键类型完全相同的化合物 |
| C.元素Y、R分别与元素X形成的化合物的热稳定性: XmY>XmR |
D.元素X、Z形成化合物的电子式可以表示成 |
短周期A、B、C、D 4种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上电子数之和。
(1)A的原子结构示意图是___________ E的电子式为___________;
(2)D在周期表中的位置是 ______。它的下一周期同族元素最高价氧化物对应的水化物的分子式为___________;
(3)C与水反应的化学方程式是_________________________________,写出所得溶液中含有10个电子的微粒符号___________。
将下列晶体熔化:氢氧化钠、二氧化硅、氧化钙、四氯化碳,需要克服的微粒间的相互作用
①共价键 ②离子键 ③分子间作用力,正确的顺序是
| A.①②②③ | B.②①②③ | C.②③②① | D.①①②③ |
五种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。
| X |
Y |
|
|
| |
Z |
W |
M |
请按要求回答下列问题:
(1)X元素名称 ,W的离子结构示意图 ;
(2)元素Z位于周期表中的位置是 ;
(3)元素Z可以形成多种单质,请任意写出一种常见单质的名称 ;
(4)Y的最高价氧化物的化学式为____ _;M的最高价氧化物水化物名称为_______;
(5)Z、W、M三种元素中,原子半径最大的是 (填元素符号);这三者与氢元素形成的化合物中,最稳定的是 (填:氢化物的化学式),它的电子式为 ;
(6)X与M可形成XM4型化合物,是一种常见的溶剂,其中的化学键类型是 (填:“离子键”或“共价键”)。
(7)W的氧化物有两种A和B,已知在某一定条件下,A和B能同时相互转化。则在该条件下A 完全转化为B(填:“能”或“不能”)
在A、B、C、D、E五种短周期元素中,A、B、C三种元素的原子序数依次增大,A、C都能与B按原子个数比为1:1或2:1形成化合物,但常温时A、B形成的化合物呈液态,C、B形成的化合物呈固态。D的原子最外层电子数最多,E的核电荷数最大,D与E能形成气态物质ED4。
(1)画出D的原子结构示意图: ,五种元素原子半径从大到小的顺序是 (填元素符号);
(2)A与B形成的化合物中,含非极性键的化合物的结构式为 ;
(3)C与B按原子个数比为1:1形成化合物的电子式是 ;
(4)D、E所形成氢化物的稳定性由强到弱的顺序是 (填具体的化学式);
(5)由短周期元素组成的某些微粒,如SO2、O3、NO2-,可互称为等电子体,则与B、D同周期的元素组成的微粒中,能与N3-互称为等电子体的微粒是 (填符合要求所有微粒的名称);
(6)写出工业上制E单质的化学方程式: 。
下图是常温下,部分短周期元素最高价氧化物对应水化物的等物质的量浓度稀溶液的pH值与原子序数的关系图,Z的氧化物是两性氧化物。下列说法正确的是
| A.L对应的氢化物比E对应的氢化物更稳定、熔沸点更高的原因是L的氢化物可以形成两种化学键 |
| B.W、R两种元素的最高价氧化物对应的水化物的pH后者较大 |
| C.元素E、W对应的单质,其晶体类型可能相同、也可能不同,这是由于它们形成晶体的化学键类型不同造成的 |
| D.元素X、Y、W形成的化合物溶液可能能与W的最高价氧化物反应,既生成沉淀,又产生气体 |
A~I都是由短周期元素组成的常见物质,它们之间的转化关系如下图所示。已知:A为气体,其水溶液呈碱性;D、F均能与人体血液中的血红蛋白结合而使人中毒;E可作为半导体材料。
(1)化合物A的电子式为_______________________。
氧化物I中化学键类型:_____________________。
组成E单质的元素在元素周期表中的位置是____________________________。
图中物质所含元素原子的半径由大到小依次是(写元素符号)_____________。
(2)反应④的化学方程式为______________________________________________。
(3)将F与B按体积比2:1混合生成气体M,常温下测定M相对分子质量时,得到的实验值总是比理论值偏大,其原因是(用化学方程式表示)___________________。
(4)某容积为V L的试管中充满F气体(标准状况下),若将该气体完全被水吸收,需通入B的物质的量为(写含V的表达式)_______________mol,此时所得溶液中再通入气体A,恰好完全反应后所得溶液中各离子浓度由大到小依次为:_________________________。
试题篮
()