用惰性电极实现电解,下列说法正确的是
| A.电解氢氧化钠稀溶液,溶液浓度增大pH变小 |
| B.电解氯化钠溶液,溶液浓度减小pH不变 |
| C.电解硝酸银溶液,要消耗OH--溶液pH变小 |
| D.电解稀硫酸,实质是电解水,溶液pH不变 |
常温时,将a1 mL、b1 mol·L-1的CH3COOH溶液加入到a2 mL、b2 mol·L-1的NaOH溶液中,下列结论中正确的是 ( )。
| A.如果a1b1=a2b2,则混合溶液的pH=7 |
| B.如果混合液的pH=7,则混合溶液中c(CH3COO-)=c(Na+) |
| C.如果a1=a2,b1=b2,则混合溶液中c(CH3COO-)=c(Na+) |
| D.如果a1=a2,且混合溶液的pH>7,则b1<b2 |
常温下,向0.25 mol·L-1的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液,下列有关说法中正确的是
| A.硫酸溶液的体积为30 mL |
| B.b时刻溶液中SO42-的浓度约为0.125 mol·L-1 |
| C.d时刻溶液的pH约为13 |
| D.溶液的导电能力:c<d=b<a |
下列说法中,正确的是( )
| A.25℃时,1L pH=3的盐酸和醋酸能消耗等质量的镁粉 |
| B.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)将增大 |
| C.V1L pH=12的NaOH溶液与V2L pH=2的HA溶液混合,若混合液显中性,则V1≤V2 |
| D.在0.1mol·L-1 NaHCO3溶液中,加入少量NaOH固体,Na+和CO32-的离子浓度均增大 |
下列物质中属于强电解质的是( )
①NaOH ②NH3·H2O ③CaCO3 ④CH3COOH ⑤NaHCO3 ⑥氢氧化铝
⑦氯化铵 ⑧二氧化碳 ⑨乙醇⑩铜
| A.①③⑤⑦ | B.②④⑥⑦ | C.①③⑥⑦ | D.除⑧⑨⑩ |
下列有关实验的操作正确的是( )
| |
实验 |
操作 |
| A |
配制稀硫酸 |
先将浓硫酸加入烧杯中,后倒入蒸馏水 |
| B |
排水法收集 分解产生的 |
先熄灭酒精灯,后移除导管 |
| C |
浓盐酸与 反应制备纯净 |
气体产物先通过浓硫酸,后通过饱和食盐水 |
| D |
萃取碘水中的 |
先从分液漏斗下口放出有机层,后从上口倒出水层 |
| A. | A |
B. | B |
C. | C |
D. | D |
下列说法正确的是
| A.KClO3和SO3溶于水后均能导电,故KClO3和SO3都是电解质 |
| B.常温下将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
| C.常温下,等浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
| D.25℃时,用pH=3的盐酸滴定等浓度的氨水至溶液的pH=7,V(氨水)<V(盐酸) |
对于常温下pH为4的醋酸溶液,下列叙述正确的是
A.该溶液的c(H+)为1×10-4 mol·L-1 |
B.该溶液lmL稀释至100mL后,pH等于6 |
C.向该溶液中加入等体积、pH为10的氢氧化钠溶液恰好完全中和 |
D.该溶液中醋酸电离出的c(H+)与水电离出的c(H+)的比值为106 |
室温下,下列关于pH均为9、体积均为10mL的NaOH溶液和CH3COONa溶液比较的说法,正确的是
| A.两种溶液中的c(Na+)相等 |
| B.分别加热到相同温度时,CH3COONa溶液的pH小 |
| C.分别加水稀释到100mL时,两种溶液的pH依然相等 |
| D.两溶液中由水电离出的c(OH-)之比为10-9/10-5 |
下列有关说法正确的是
A.一定条件下反应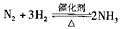 ,达到平衡时, ,达到平衡时,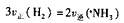 |
| B.10mL浓度为1mol/L的盐酸与过量的Zn粉反应,若加入适量的CH3COONa溶液,既能减慢反应这率,又不影响H2的生成 |
C.将PH=a十l的氨水稀释为pH=a的过程中,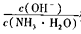 变小 变小 |
| D.常温下,向浓度为0.1 mol/L的CH3COONa溶液中加入等体积等浓度的CH3COOH,混合溶液的pH=7 |
下列有关电解质溶液中粒子浓度关系正确的是
| A.CO2的水溶液中:c(H+)>c(HCO3-)=2c(CO32-) |
| B.pH=1的NaHSO4溶液:c(H+)=c(SO42-)十c(OH-) |
| C.含有AgCl和AgI固体的悬浊液:c(Ag+)>c(C1-)=c(I-) |
| D.等物质的量浓度的NH4HSO4溶液和NH4Cl溶液,c(NH4+)前者小 |
下列说法正确的是:
| A.将AlCl3溶液、Na2SO3溶液蒸干并灼烧可分别得到Al2O3、Na2SO3 |
| B.在溶液的稀释过程中,离子浓度有的可能增大,有的可能减小,有的可能不变 |
| C.0.1 mol/L CH3COOH溶液在稀释过程中将变小 |
| D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
已知25℃时有关
弱酸的电离平衡常数:则下列有关说法正确的是
| 弱酸化学式 |
CH3COOH |
HCN |
H2CO3 |
| 电离平衡常数(25℃ ) |
1.8×l0-5 |
4.9×l0-10 |
K1=4.3×l0-7 K2=5.6×l0 -11 |
A.等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B.a mol·L—1 HCN溶液与b mol·L—1 NaOH溶液等体积混合后,所得溶液中
c(CN-)>c(Na+),则a一定大于b
C.冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离度、pH均先增大后减小
D.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+ c(H+)=c(OH-)+ c(HCO3-) +2c(CO32-)
用0.01 mol/L H2SO4滴定0.01mol/L NaOH溶液,中和后加水至100ml,若滴定时终点判断有误差:①多加1滴H2SO4;②少加1滴H2SO4;(设1滴为0.05ml)则①和②c(H+)的比值是( )
| A.10 | B.50 | C.5×103 | D.104 |
试题篮
()